工业合成氨的反应为N2(g)+3H2(g)2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60 mol H2(g),2min在某温度下达到平衡,此时NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。请计算(写出计算过程):
(1)2min内N2的平均速率;
(2)该条件下此反应的平衡常数K。
高二化学计算题简单题
工业合成氨的反应为N2(g)+3H2(g)2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60 mol H2(g),2min在某温度下达到平衡,此时NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。请计算(写出计算过程):
(1)2min内N2的平均速率;
(2)该条件下此反应的平衡常数K。
高二化学计算题简单题
工业合成氨的反应为N2(g)+3H2(g)2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60 mol H2(g),2min在某温度下达到平衡,此时NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。请计算(写出计算过程):
(1)2min内N2的平均速率;
(2)该条件下此反应的平衡常数K。
高二化学计算题简单题查看答案及解析
工业合成氨的反应为N2(g)+3H2(g)2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60 mol H2(g),2min在某温度下达到平衡,此时NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。请计算(写出计算过程):
(1)2min内N2的平均速率;
(2)该条件下此反应的平衡常数K。
高二化学计算题困难题查看答案及解析
(8分)工业合成氨的反应为N2(g)+3H2(g)2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
计算:
(1)该条件下N2的平衡转化率;(小数点后保留一位)
(2)该条件下反应2NH3(g)N2(g)+3H2(g)的平衡常数。(不带单位)
高二化学计算题中等难度题查看答案及解析
工业合成氨的反应为N2(g)+3H2(g)2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
计算:
(1)该条件下N2的平衡转化率;(小数点后保留一位)
(2)该条件下反应2NH3(g)N2(g)+3H2(g)的平衡常数。(不带单位)
高二化学选择题中等难度题查看答案及解析
工业合成氨的反应如下:N2 + 3H2 2NH3。
某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50s内的平均反应速率 v(N2) = 。
(2)250s时,H2的转化率为 。
(3)已知的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化 kJ。下图能正确表示该反应中能量变化的是________。
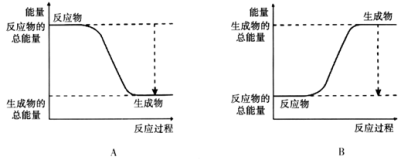
(4)为加快反应速率,可以采取的措施
a.降低温度
b.增大压强
c.恒容时充入He气
d.恒压时充入He气
e.及时分离NH3
(5)下列说法错误的是
A.使用催化剂是为了加快反应速率,提高生产效率
B.上述条件下,N2不可能100%转化为NH3
C.为了提高N2的转化率,应适当提高H2的浓度
D.250~350s生成物浓度保持不变,反应停止
高二化学填空题困难题查看答案及解析
工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为1.0 L的密闭容器中充入0.5 mol N2(g)和1.0mol H2(g),某温度下反应达到平衡时容器内压强为原来的2/3,则该反应的平衡常数
A .4 B.16 C.32 D.64
高二化学选择题中等难度题查看答案及解析
(10分)工业上合成氨的反应:N2(g)+3H2(g)2NH3(g)ΔH=-92.60 kJ·mol-1。
(1)在绝热、容积固定的密闭容器中发生反应:N2(g)+3H2(g)2NH3(g),下列说法能说明上述反应向正反应方向进行的是____________________(填序号)。
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N—H键的同时生成2n mol H—H键
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
④混合气体的平均摩尔质量增大
⑤容器内的气体密度不变
(2)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
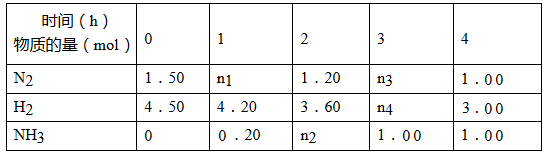
根据表中数据计算:
①反应进行到2 h时放出的热量为_________________kJ。
②此温度下该反应的化学平衡常数K=_________________(保留两位小数)。
③反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________________方向移动(填“正反应”或“逆反应”或“不移动”)。
④有甲、乙两个完全相同的容器,向甲容器中加入1 mol N2 (g)和6mol H2 (g),在一定条件下达到平衡时的热效应(吸热或放热)为Q,在相同条件下向乙容器中加入2 mol NH3 (g)和3mol H2 (g),达到平衡时的热效应(放热或吸热)为4Q。则甲容器中H2的转化率为________________。
高二化学填空题极难题查看答案及解析
合成氨是重要的化学工业,为了研究合成氨的反应原理,在一密闭容器内充入1 mol N2和2 mol H2,在一定条件下,使之发生如下反应:N2+3H2 2NH3 。
Ⅰ:若维持温度不变,且密闭容器的容积固定为1 L。
(1) 当此反应经过2 min达到平衡状态时,测得反应混合物中NH3的物质的量为0.2 moL,则H2在2 min内的平均反应速率为__________________。
(2)如果开始时,向该容器内加入0.5 moL N2 ,要使反应混合物中三种气体的物质的量分数仍与上述平衡时的完全相同,则还必须加入H2 _______mol和NH3 _______mol。
(3)如果开始时加入N2、H2、NH3的物质的量分别为a mol 、b mol 、c mol ,要使反应达到平衡状态时,反应混合物中三种气体的物质的量分数仍与(1)平衡时完全相同,则a、b、c应满足的一般条件是(a、b分别用含c的方程式表示)________ 。
Ⅱ:若温度维持不变,体系压强维持与Ⅰ相同,密闭容器的容积由1 L随反应进行而改变。
(4)开始时加入1 mol N2和2 mol H2,经过一段时间,容器中三种气体的物质的量分数不再发生变化时,则NH3的物质的量为__________(选填一个编号)
(甲)大于0.2 mol (乙)等于0.2 mol
(丙)小于0.2 mol (丁)可能大于、等于或小于0.2mol
作出此判断的理由是__________________________________________。
高二化学填空题简单题查看答案及解析
氨在国民生产中占有重要的地位。工业合成氨的反应为:N2(g)+3H2(g)2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
(1)反应进行到2小时时放出的热量为____________kJ。
(2)此条件下该反应的化学平衡常数K=____________(保留两位小数)。
(3)有两个密闭容器A和B,A容器保持恒容,B容器保持恒压,起始时向容积相等的A、B中分别通入等量的NH3气体,均发生反应:2NH3(g)3H2(g)+N2(g)。则:
①达到平衡所需的时间:t(A)_____t(B),平衡时,NH3的转化率:a(A)______a(B) (填“>”、“=”或“<”)。
②达到平衡后,在两容器中分别通入等量的氦气。A中平衡向_________移动,B中平衡向_________移动。(填“向正反应方向”、“向逆反应方向”、“不”)。
(4)在三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数[φ(NH3)]随时间变化的曲线如图所示.下列说法中正确的是_____(填字母,下同)。
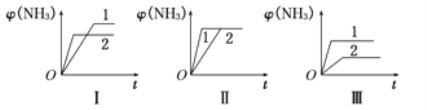
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
高二化学综合题中等难度题查看答案及解析
工业合成氨的反应如下:3H2+N22NH3。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol N2和2.0 mol H2,一段时间后反应达平衡状态,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50 s内的平均反应速率 v(N2)=_______________。
(2)250 s时,H2的转化率为_______________。
(3)已知N≡N的键能为946 kJ·mol-1,H-H的键能为436 kJ·mol-1,N-H的键能为391 kJ·mol-1,则生成1 mol NH3过程中的热量变化为_______kJ。下图能正确表示该反应中能量变化的是_____(填字母)。
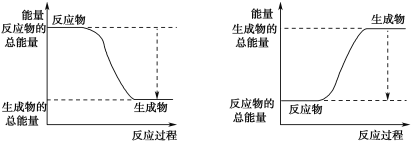
A B
(4)为加快反应速率,可以采取的措施______________。
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离出NH3
(5)下列说法错误的是____________。
a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.在一定条件下,合成氨反应有一定的限度
d.250~350 s时,生成物浓度保持不变,反应停止
高二化学综合题简单题查看答案及解析