-
CO2加氢可转化为高附加值的CO、CH4、CH3OH等C1产物。该过程可缓解CO2带来的环境压力,同时可变废为宝,带来巨大的经济效益。CO2加氢过程,主要发生的三个竞争反应为:
反应i:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.01kJ•mol-1
CH3OH(g)+H2O(g)△H=-49.01kJ•mol-1
反应ii:CO2(g)+4H2(g) CH4(g)+2H2O(g)△H=-165.0kJ•mol-1
CH4(g)+2H2O(g)△H=-165.0kJ•mol-1
反应iii:CO2(g)+H2(g) CO(g)+H2O(g)△H=+41.17kJ•mol-1
CO(g)+H2O(g)△H=+41.17kJ•mol-1
回答下列问题:
(1)由CO、H2合成甲醇的热化学方程式为_____。
(2)反应iii为逆水煤气变换反应,简称RWGS。以金属催化剂为例,该反应历程的微观示意和相对能量(eV)变化图如图所示( 为催化剂,
为催化剂, 为C原子,
为C原子, 为O原子,o为H原子)
为O原子,o为H原子)
历程I:
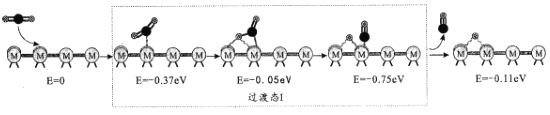
历程II:

历程III:
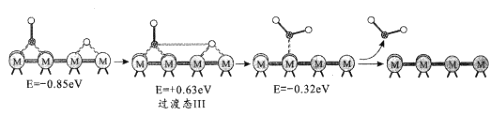
①历程1方框内反应的方程式为CO2*+*=CO*+O*(*为催化剂活性位点)。根据图示,其反应热△H_____0(填“>”或“<”)。
②反应历程II方框内的方程式是_____。
③反应历程中_____(填“历程I”、“历程II”或“历程III”)是RWGS的控速步骤。
(3)我国科学家研究了不同反应温度对含碳产组成的影响。在反应器中按 =3:1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):
=3:1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):

①1MPa时,表示CH4和CO平衡组成随温度变化关系的曲线分别是_____、_____。M点CO平衡组成含量高于N点的原因是_____。
②当CH4和CO平衡组成为40%时,该温度下反应iii的平衡常数Kp为_____。
-
CO2是一种常用的化工原料,经常可以用来转化成高附加值的CO、CH4、CH3OH、CO(NH2)2等一碳(C1)产物。
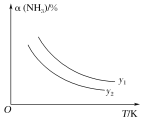
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)。在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH___(填“>”、“<”或“=”,下同)0,若y表示压强,则y1___y2,若y表示反应开始时的氨碳比[
CO(NH2)2(s)+H2O(g)。在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH___(填“>”、“<”或“=”,下同)0,若y表示压强,则y1___y2,若y表示反应开始时的氨碳比[ ],则y1__y2。
],则y1__y2。
Ⅱ.CO2加氢过程,主要发生的三个竞争反应为:
反应i:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H=-49.01kJ•mol-1
CH3OH(g)+H2O(g) ∆H=-49.01kJ•mol-1
反应ii:CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H=-165.0kJ•mol-1
CH4(g)+2H2O(g) ∆H=-165.0kJ•mol-1
反应iii:CO2(g)+H2(g) CO(g)+H2O(g) ∆H=+41.17kJ•mol-1
CO(g)+H2O(g) ∆H=+41.17kJ•mol-1
回答下列问题:(1)由CO、H2合成甲醇的热化学方程式为__。
(2)如图是某甲醇燃料电池工作的示意图。

质子交换膜(只有质子能够通过)左右两侧的溶液均为1L2mol·L-1H2SO4溶液。电极a上发生的电极反应为___,当电池中有1mole−发生转移时左右两侧溶液的质量之差为___g(假设反应物耗尽,忽略气体的溶解)。
(3)我国科学家研究了不同反应温度对含碳产物组成的影响。在反应器中按 =3∶1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):
=3∶1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):
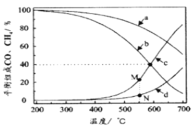
则表示1MPa时CH4和CO平衡组成随温度变化关系的曲线分别是___、___。M点所表示物质的平衡组成高于N点的原因是___。
-
CO2是主要的温室气体,也是一种工业原料。回收利用CO2有利于缓解温室效应带来的环境问题。
(1)我国科学家通过采用一种新型复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。
已知:2H2 (g)+O2 (g) =2H2O(l) ΔH = -571.6 kJ/mol
2C8H18(l)+25O2(g) =16CO2(g)+18H2O(l) ΔH = -11036 kJ/mol
25℃、101kPa条件下,CO2与H2反应生成辛烷(以C8H18表示)和液态水的热化学方程式是_________。
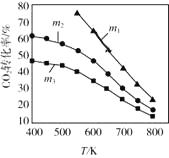
(2)CO2催化加氢合成乙醇的反应原理是:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m= 。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
(3)在Cu/ZnO催化剂存在下,将CO2与H2混合可合成甲醇,同时发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
反应Ⅱ CO2(g)+H2(g)  CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
控制一定的CO2和H2初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
| 实验序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
| 实验1 | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
| 实验2 | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
| 实验3 | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
| 实验4 | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比实验1和实验3可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因_______________;
②对比实验1和实验 2可发现:在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因____________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有_______。
a.使用Cu/ZnO纳米棒做催化剂
b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度
d.投料比不变,增加反应物的浓度
e.增大 的初始投料比
的初始投料比
(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2,电解,在阴极可制得低密度聚乙烯 (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是_____________。
②工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下______L 的CO2。
-
CO2是主要的温室气体,也是一种工业原料。回收利用CO2有利于缓解温室效应带来的环境问题。
(1)我国科学家通过采用一种新型复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。
已知:2H2 (g)+O2 (g) =2H2O(l) ΔH = -571.6 kJ/mol
2C8H18(l)+25O2(g) =16CO2(g)+18H2O(l) ΔH = -11036 kJ/mol
25℃、101kPa条件下,CO2与H2反应生成辛烷(以C8H18表示)和液态水的热化学方程式是_________。
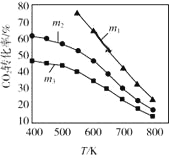
(2)CO2催化加氢合成乙醇的反应原理是:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m= 。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
(3)在Cu/ZnO催化剂存在下,将CO2与H2混合可合成甲醇,同时发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
反应Ⅱ CO2(g)+H2(g)  CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
控制一定的CO2和H2初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
| 实验序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
| 实验1 | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
| 实验2 | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
| 实验3 | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
| 实验4 | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比实验1和实验3可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因_______________;
②对比实验1和实验 2可发现:在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因____________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有_______。
a.使用Cu/ZnO纳米棒做催化剂
b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度
d.投料比不变,增加反应物的浓度
e.增大 的初始投料比
的初始投料比
(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2,电解,在阴极可制得低密度聚乙烯 (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是_____________。
②工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下______L 的CO2。
-
将CH4、CO2催化重整为可用的化学品,对缓解能源危机、改善环境意义重大。
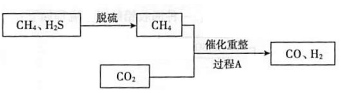
(l)以Fe(OH)3为脱硫剂,通过复分解反应吸收H2S,产物是H2O和___________。
(2)过程A主要涉及以下反应:
i. CH4(g)+CO2(g) 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
ii. CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ/mol
CO2(g)+H2(g) △H=-41kJ/mol
①反应i的化学平衡常数K随温度的变化关系是____。
②分析反应iixt反应i中CO2转化率可能的影响并说明理由:____(写出一种即可)。
(3)某科研团队利用Ni、CaO、Fe3O4三种催化剂在850℃下“超干重整”CH4和CO2;
过程I.通入CO2和CH4,所得CO被吸收,H2O被分离出体系,如下面左图所示。
过程Ⅱ.H2O被分离后,向该装置中再通入He气,使催化剂再生并获得CO,如下面右图所示。
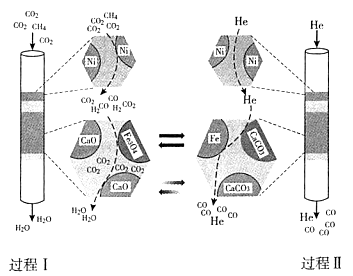
①CH4和CO2重整为CO、H2O的热化学方程式是____________。
②结合反应方程式简述Fe3O4的催化作用:___________。
③CaO对Fe3O4是否起到催化作用至关重要,实验研究结果如下表:
| 编号 | 催化剂 | 是否添加CaO | 还原产物 |
| 1 | Fe3O4 | 添加 | 有Fe |
| 2 | Fe3O4 | 不添加 | 无Fe |
运用有关化学原理解释实验结果:____。
-
CO2的转化和重整受到越来越多的关注,它是有效应对全球气候变化、促进低碳社会构建的重要方法。
(1)热化学转化法。
CO2催化加氢合成CH4,其过程中主要发生下列反应:
反应Ⅰ:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
反应Ⅱ:CO(g)+H2O (g)=CO2(g)+H2(g);ΔH=+2.8 kJ·mol-1
反应Ⅲ:2CO(g)+O2(g)=2CO2(g);ΔH=-566.0 kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(g) 的ΔH=________kJ·mol-1。
(2)CO2催化还原法。
图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当有1 mol CO2反应时,直接传递的电子物质的量为________mol。
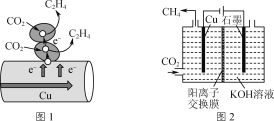
(3)CO2电化学催化重整法。
①图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为______________________,电解一段时间后,阳极区溶液pH减小,其原因是__________________。
②CO2与CH4在催化剂作用下合成乙酸,反应的化学方程式为________。
(4)CO2与丙烯通过金属杂多酸盐[CoxH(3-2x)PW12O40] 催化合成甲基丙烯酸。
①研究发现金属杂多酸盐中x对CO2转化率的影响如图3所示,由图3得出催化效果最好的金属杂多酸盐化学式是________。
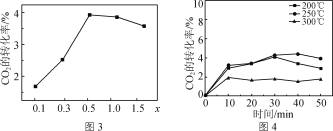
②催化剂在温度不同时对CO2转化率的影响如图4所示,300 ℃催化效果远不如200 ℃ 和250 ℃的原因为__________________________________。
-
CO2的转化和重整受到越来越多的关注,它是有效应对全球气候变化、促进低碳社会构建的重要方法。
(1)热化学转化法。
CO2催化加氢合成CH4,其过程中主要发生下列反应:
反应Ⅰ:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
反应Ⅱ:CO(g)+H2O (g)=CO2(g)+H2(g);ΔH=+2.8 kJ·mol-1
反应Ⅲ:2CO(g)+O2(g)=2CO2(g);ΔH=-566.0 kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(g) 的ΔH=________kJ·mol-1。
(2)CO2催化还原法。
图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当有1 mol CO2反应时,直接传递的电子物质的量为________mol。
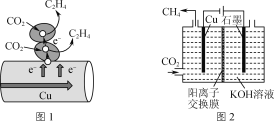
(3)CO2电化学催化重整法。
①图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为______________________,电解一段时间后,阳极区溶液pH减小,其原因是__________________。
②CO2与CH4在催化剂作用下合成乙酸,反应的化学方程式为________。
(4)CO2与丙烯通过金属杂多酸盐[CoxH(3-2x)PW12O40] 催化合成甲基丙烯酸。
①研究发现金属杂多酸盐中x对CO2转化率的影响如图3所示,由图3得出催化效果最好的金属杂多酸盐化学式是________。
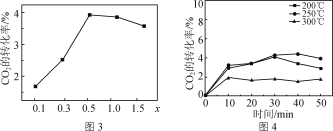
②催化剂在温度不同时对CO2转化率的影响如图4所示,300 ℃催化效果远不如200 ℃ 和250 ℃的原因为__________________________________。
-
中科院兰州化学物理研究所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图
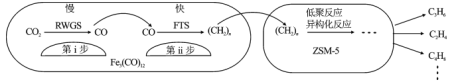
下列说法正确的是
A.第i步反应为CO2+H2=CO+H2O
B.第i步反应的活化能低于第ii步
C.Fe3(CO)12/ZSM-5使CO2加氢合成低碳烯的△H减小
D.添加不同助剂后,反应的平衡常数各不相同
-
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下,则下列说法正确的是( )
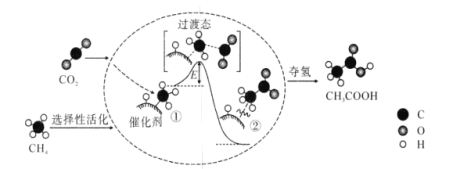
A.E为该反应的反应热
B.①→②吸收能量
C.CH4→CH3COOH过程中,有极性键的断裂和非极性键的形成
D.加入催化剂能改变该反应的能量变化
-
随着能源与环境问题越来越被人们关注,碳-化学(C1化学)成为研究的热点。“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.
(1)将CO2转化成有机物课有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2O C6H12O6+6O2
C6H12O6+6O2
b.CO2+3H2O CH3OH+H2O
CH3OH+H2O
c.CO2+CH4 CH3COOH
CH3COOH
d.2CO2+6H2 CH2=CH2+4H2O
CH2=CH2+4H2O
在以上属于人工转化的反应中,原子利用率最高的是_______(填序号)。
(2)CO可用于合成甲醇。在压强0.1MPa条件下,在体积为bL的密闭容器中充入 和
和 ,在催化剂作用下合成甲醇:CO(g)+2H2(g)
,在催化剂作用下合成甲醇:CO(g)+2H2(g)  CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图。
CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图。
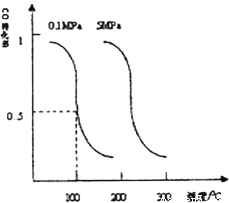
①该反应属于_______反应(填“吸热”或“放热”)。若一个可逆反应的平衡常数K值很大,对此反应的说法正确的是____(填序号)。
a.反应使用催化剂意义不大
b.该反应发生将在很短时间内完成
c.该反应达到平衡时至少有一种反应物百分含量很小
d.该反应一定是放热反应
②100℃时,该反应的平衡常数K=________(用a,b的代数式表示)。
(3)二甲醚(CH3OCH3)被称为21世纪的新型燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
①工业上利用水煤气合成二甲醚的三步反应如下:
a.2H2(g)+CO(g)⇌CH3OH(g) △H1=-90.8kJ•mol-1
b.2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H2=-23.5kJ•mol-
c.CO(g)+H2O(g)⇌CO2(g0+H2(g)△H3=-41.3kJ•mol
总反应:3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2(g)的△H=___.
②对于反应b,在温度和容积不变的条件下,能说明该反应已达到平衡状态的是_____(填字母)。
a.n(CH3OH)=n(CH3OCH3)=n(H2O)
b.容器内压强保持不变
c.H2O(g)的浓度保持不变
d.CH3OH的消耗速率与CH3OCH3的消耗速率之比为2:1
(4)以KOH溶液为电解质,用二甲醚-空气组成燃料,其中负极的电极反应式为_______。
(5)碳化合物在治理汽车尾气方面也大有可为,如CO、CH4等在一定条件下均可以与氮氧化物生成无污染的物质。写出CO与氮氧化物(NOx)在有催化剂的条件下反应的化学方程式____________。
CH3OH(g)+H2O(g)△H=-49.01kJ•mol-1
CH4(g)+2H2O(g)△H=-165.0kJ•mol-1
CO(g)+H2O(g)△H=+41.17kJ•mol-1
 为催化剂,
为催化剂,为C原子,
为O原子,o为H原子)



=3:1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):














