二茂铁[(C2H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁的熔点是173℃(在100℃以上能升华),沸点是249℃,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法不正确的是( )
A.二茂铁属于分子晶体
B.在二茂铁中,C5H5-与Fe2+之间形成的化学键类型是离子键
C.已知环戊二烯的结构式为 ,则其中仅有1个碳原子采取sp3杂化
,则其中仅有1个碳原子采取sp3杂化
D. C5H5-中一定含有键
高三化学单选题中等难度题
二茂铁[(C2H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁的熔点是173℃(在100℃以上能升华),沸点是249℃,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法不正确的是( )
A.二茂铁属于分子晶体
B.在二茂铁中,C5H5-与Fe2+之间形成的化学键类型是离子键
C.已知环戊二烯的结构式为 ,则其中仅有1个碳原子采取sp3杂化
,则其中仅有1个碳原子采取sp3杂化
D. C5H5-中一定含有键
高三化学单选题中等难度题
二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法不正确的是( )
A.二茂铁属于分子晶体
B.在二茂铁结构中,C5H与Fe2+之间形成的化学键类型是离子键
C.已知:环戊二烯的结构式为: ,则其中仅有1个碳原子采取sp3杂化
,则其中仅有1个碳原子采取sp3杂化
D.C5H中一定含π键
高三化学选择题困难题查看答案及解析
二茂铁[(C2H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁的熔点是173℃(在100℃以上能升华),沸点是249℃,不溶于水,易溶于苯、乙醚等有机溶剂。下列说法不正确的是( )
A.二茂铁属于分子晶体
B.在二茂铁中,C5H5-与Fe2+之间形成的化学键类型是离子键
C.已知环戊二烯的结构式为 ,则其中仅有1个碳原子采取sp3杂化
,则其中仅有1个碳原子采取sp3杂化
D. C5H5-中一定含有键
高三化学单选题中等难度题查看答案及解析
过渡金属元素及其化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁熔点是173℃(在100℃时开始升华),沸点是249℃。
(1)基态Fe2+离子的价电子排布式为_______________________________
(2)二茂铁属于___________________晶体;测定表明二茂铁中所有氢原子的化学环境都相同,则二茂铁的结构应为下图中的________________(选填“a”或“b”)

(3)环戊二烯()中C的杂化方式 _______________。1mol环戊二烯中含有σ键的数目为___________。
(4)分子中的大π键可用符号πmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),在C5H5—中的每个碳原子上都有一个未参与σ键的电子,这些电子占据与环的平面垂直的p轨道上。C5H5—的大π键可以表示为______________。
(5)如图,铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法正确的是_______
A.γ﹣Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
B.α﹣Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
C.若δ﹣Fe晶胞边长为acm,α﹣Fe晶胞边长为bcm,则两种晶体密度比为2b3:a3
D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型相同

(6)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体性质会产生重大影响。由于晶体缺陷,晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm-3,晶胞边长为4.28×10-10 m,则FexO中x=_____(用代数式表示,不要求算出具体结果)。
高三化学综合题中等难度题查看答案及解析
过渡金属元素及其化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁熔点是173℃(在100℃时开始升华),沸点是249℃。
(1)基态Fe2+离子的价电子排布式为_______________________________
(2)二茂铁属于___________________晶体;测定表明二茂铁中所有氢原子的化学环境都相同,则二茂铁的结构应为下图中的________________(选填“a”或“b”)

(3)环戊二烯()中C的杂化方式 _______________。1mol环戊二烯中含有σ键的数目为___________。
(4)分子中的大π键可用符号πmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),在C5H5—中的每个碳原子上都有一个未参与σ键的电子,这些电子占据与环的平面垂直的p轨道上。C5H5—的大π键可以表示为______________。
(5)如图,铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法正确的是_______
A.γ﹣Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
B.α﹣Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
C.若δ﹣Fe晶胞边长为acm,α﹣Fe晶胞边长为bcm,则两种晶体密度比为2b3:a3
D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型相同

(6)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体性质会产生重大影响。由于晶体缺陷,晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm-3,晶胞边长为4.28×10-10 m,则FexO中x=_____(用代数式表示,不要求算出具体结果)。
高三化学综合题中等难度题查看答案及解析
用还原铁粉制备二茂铁开辟了金属有机化合物研究的新领域。二茂铁甲酰胺是其中一种重要的衍生物,结构如图所示。

(1)基态Fe原子价层电子排布式是_______。
(2)已知二茂铁甲酰胺熔点是176℃,沸点是249℃,难溶于水,易溶于氯仿、丙酮等有机溶剂。据此可推断二茂铁甲酰胺晶体为_______晶体。
(3)二茂铁甲酰胺中碳原子的杂化方式为_________,H、C、N、O四种元素的电负性由大到小的顺序是_________。
(4)碳、氮元素对应的最简单氢化物分别是CH4和NH3,相同条件下CH4的沸点比NH3的沸点_______(填“高”或“低”),主要原因是_______。
(5)氢、氮、氧三种元素按照4:2:3的原子个数比形成离子化合物。该离子化合物中,阳离子空间构型是_______,1 mol阴离子含有σ键的数目为_______。
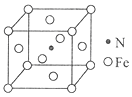
(6)氮和铁能形成一种磁性材料,其晶胞如图所示,该磁性材料的化学式为_______。已知晶胞参数为a nm,则该晶胞密度的计算式为ρ=_______g/cm3(用NA表示阿伏加德罗常数的值)。
高三化学填空题中等难度题查看答案及解析
用还原铁粉制备二茂铁开辟了金属有机化合物研究的新领域。二茂铁甲酰胺是其中一种重要的衍生物,结构如图所示。
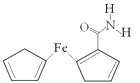
(1)基态Fe原子价层电子排布式是_______。
(2)已知二茂铁甲酰胺熔点是176℃,沸点是249℃,难溶于水,易溶于氯仿、丙酮等有机溶剂。据此可推断二茂铁甲酰胺晶体为_______晶体。
(3)二茂铁甲酰胺中碳原子的杂化方式为_________,H、C、N、O四种元素的电负性由大到小的顺序是_________。
(4)碳、氮元素对应的最简单氢化物分别是CH4和NH3,相同条件下CH4的沸点比NH3的沸点_______(填“高”或“低”),主要原因是_______。
(5)氢、氮、氧三种元素按照4:2:3的原子个数比形成离子化合物。该离子化合物中,阳离子空间构型是_______,1 mol阴离子含有σ键的数目为_______。
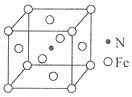
(6)氮和铁能形成一种磁性材料,其晶胞如图所示,该磁性材料的化学式为_______。已知晶胞参数为a nm,则该晶胞密度的计算式为ρ=_______g/cm3(用NA表示阿伏加德罗常数的值)。
高三化学填空题中等难度题查看答案及解析
二茂铁是一种具有芳香族性质的有机过渡金属化合物。二茂铁熔点是173℃,在100℃时开始升华,沸点是249℃,不溶于水,易溶于苯、乙醚、汽油、柴油等有机溶剂;化学性质稳定,400℃以内不分解。实验室制备二茂铁装置示意图如下图,实验步骤为:
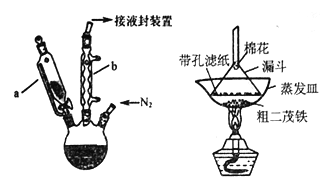
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a 中加入60mL 无水乙醚到三颈烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a 滴入5.5 mL 新蒸馏的环戊二烯(C5H6、密度0.95g/cm3),搅拌;
③将6.5g 无水FeCl2 与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25ml 装入仪器a中,慢慢滴入三颈烧瓶中,45min 滴完,继续搅拌45min;
④再从仪器a 加入25mL 无水乙醚搅拌;
⑤将三颈烧瓶中液体转入分液漏斗,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b 的名称是__________________,作用是_____________________。
(2)步骤①中通入氮气的目的是_____________________。
(3)三颈烧瓶的适宜容积应为__________ (填序号);①100ml、②250ml、③500ml;步骤⑤所得的橙黄色溶液的溶剂是_____________________。
(4)KOH、FeCl2、C5H 6反应生成二茂铁[Fe(C5H5)2]和KCl 的化学方程式为_____________________。
(5)二茂铁粗产品的提纯过程在上图中进行,其操作名称为________________。二茂铁及其衍生物可做抗震剂用于制无铅汽油,它们比曾经使用过的四乙基铅安全得多,其中一个重要的原因是_________________________________。
(6)最终得到纯净的二茂铁4.8g,则该实验的产率为___________________(保留两位有效数字)。
高三化学实验题中等难度题查看答案及解析
二茂铁是一种具有芳香族性质的有机过渡金属化合物。二茂铁熔点是173℃,在100℃时开始升华,沸点是249℃,不溶于水,易溶于苯、乙醚、汽油、柴油等有机溶剂;化学性质稳定,400℃以内不分解。实验室制备二茂铁装置示意图如下图,实验步骤为:
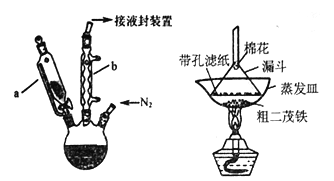
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a 中加入60mL 无水乙醚到三颈烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a 滴入5.5 mL 新蒸馏的环戊二烯(C5H6、密度0.95g/cm3),搅拌;
③将6.5g 无水FeCl2 与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25ml 装入仪器a中,慢慢滴入三颈烧瓶中,45min 滴完,继续搅拌45min;
④再从仪器a 加入25mL 无水乙醚搅拌;
⑤将三颈烧瓶中液体转入分液漏斗,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b 的名称是__________________,作用是_____________________。
(2)步骤①中通入氮气的目的是_____________________。
(3)三颈烧瓶的适宜容积应为__________ (填序号);①100ml、②250ml、③500ml;步骤⑤所得的橙黄色溶液的溶剂是_____________________。
(4)KOH、FeCl2、C5H 6反应生成二茂铁[Fe(C5H5)2]和KCl 的化学方程式为_____________________。
(5)二茂铁粗产品的提纯过程在上图中进行,其操作名称为________________。二茂铁及其衍生物可做抗震剂用于制无铅汽油,它们比曾经使用过的四乙基铅安全得多,其中一个重要的原因是_________________________________。
(6)最终得到纯净的二茂铁4.8g,则该实验的产率为___________________(保留两位有效数字)。
高三化学实验题中等难度题查看答案及解析
2001年诺贝尔化学奖被美国的诺尔斯、夏普雷斯和日本的野依良治获得,他们发现了某些手性分子可用作某些化学反应的催化剂,为合成对人类有用的重要化合物开辟了一个全新的研究领域。在有机物分子中,若某个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”,如。若同一个碳原子上连着2个碳碳双键(如C="=C==C" )时,极不稳定,因此这种结构不存在。某链烃C7H10的众多同分异构体中:
(1)处于同一平面上的碳原子数最多有_______。
A.6个 B.5个 C.7个 D.4个
(2)含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的有5种。它们的结构简式除以下3种外,还有_______、_______。
①
②
③
(3)含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”的结构简式是_________________。
高三化学填空题困难题查看答案及解析
二茂铁[(C5H5)2Fe] 分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。
它的结构如右图所示,下列说法正确的是( )
A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
B.1mol环戊二烯()中含有σ键的数目为5NA
C.分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d44s2
高三化学选择题中等难度题查看答案及解析