辉钼精矿主要成分是二氧化钼(MoS2),还含有石灰石、石英、黄铜矿(CuFeS2)等杂质。某学习小组设计提取MoS2的过程如下:下列说法错误的是
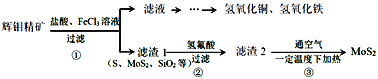
A.为加快辉钼精矿溶解,可将矿石粉粹并适当加热
B.加滤液中含Ca2+、Fe2+、Fe3+、Cu2+、H+等离子
C.以上①②③过程均涉及氧化还原反应
D.步骤③温度不宜过高,以免MoS2被氧化
高三化学单选题中等难度题
辉钼精矿主要成分是二氧化钼(MoS2),还含有石灰石、石英、黄铜矿(CuFeS2)等杂质。某学习小组设计提取MoS2的过程如下:下列说法错误的是

A.为加快辉钼精矿溶解,可将矿石粉粹并适当加热
B.加滤液中含Ca2+、Fe2+、Fe3+、Cu2+、H+等离子
C.以上①②③过程均涉及氧化还原反应
D.步骤③温度不宜过高,以免MoS2被氧化
高三化学单选题中等难度题
辉钼精矿主要成分是二氧化钼(MoS2),还含有石灰石、石英、黄铜矿(CuFeS2)等杂质。某学习小组设计提取MoS2的过程如下:下列说法错误的是

A.为加快辉钼精矿溶解,可将矿石粉粹并适当加热
B.加滤液中含Ca2+、Fe2+、Fe3+、Cu2+、H+等离子
C.以上①②③过程均涉及氧化还原反应
D.步骤③温度不宜过高,以免MoS2被氧化
高三化学单选题中等难度题查看答案及解析
某学习小组设计如图装置,验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质不参与反应)。
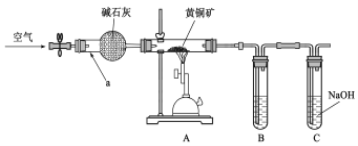
回答下列问题。
(1)仪器a的名称_________,碱石灰的作用______________________________________。
(2)为检验灼烧黄铜矿产生的气体,B中可选__________________
a.HNO3溶液 b.品红溶液 c.BaCl2溶液 d.溴水 e.KMnO4溶液
(3)C中NaOH的作用____________________________________________________
(4)样品经煅烧后的固体中铜元素以泡铜(Cu、Cu2O)形式存在,其中Cu2O能与稀H2SO4反应生成Cu和CuSO4。
①请设计实验验证泡铜中含有Cu2O____________________________________________。
②用泡铜与CO反应来制取粗铜装置如下图,实验时依次进行的操作:
组装仪器→检查装置气密性→加装药品→____________→____________→…→尾气处理;CO还原Cu2O的化学方程式_______________________________________________

(5)为测定CuFeS2的纯度,称取a g黄铜矿样品充分灼烧,从灼烧产物中分离出泡铜,完全溶于稀硝酸,并配成200 mL的溶液,取20.00 mL该溶液用c mol· L-1的标准液EDTA(用H2Y2-表示)滴定至终点(标准液不与杂质反应),消耗EDTA V mL,则CuFeS2的纯度为____________。(滴定时的反应为:Cu2++H2Y2-===CuY2-+2H+)
高三化学实验题中等难度题查看答案及解析
我国是世界上主要产钼国家之一,我国的钼资源十分丰富,以辉钼矿为主,是具有优势的战略资源。将辉钼矿精矿(主要成分为MoS2,杂质为CaCO3,SiO2,FeS2,CuFeS2,PbS等)除杂提纯可得到粗MoS2,通过精制转化最终可得到纯度更高的MoS2。
MoS2的相关信息:
①具有类似石墨的层状结构,有金属光泽,熔点1185℃,密度4.80g/cm-3,硬度很低,被广泛地应用在润滑领域。
②一般不溶于水、酸、碱和有机溶剂中,但溶于王水和煮沸的浓硫酸。Mo为+4价,在空气中加热至350℃以上开始被氧化,生成钼的氧化物。
有人提出了如下制取高纯MoS2的流程:
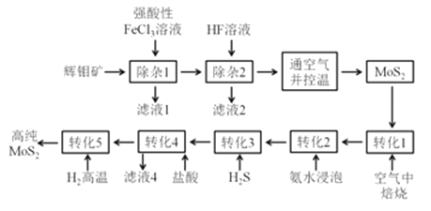
(1) MoS2可用作润滑添加剂的原因是:_____________。
(2)滤液1中存在的阳离子除H+、Ca2+、Pb2+外,还有:____________,写出“除杂1”过程发生的其中1个氧化还原反应的化学方程式:____________。
(3)“通空气并控温”这步操作的目的是:___________。必须控制好温度的原因:___________。
(4)“转化3”得到硫代钼酸铵(NH4)2MoS4。“转化4”中钼的化合价不变,产生气体和沉淀(二元化合物),写出该反应的离子方程式:____。
(5)上述流程中,哪些步骤发生了氧化还原反应:_____。
A.除杂1 B.除杂2 C.转化1 D.转化2 E.转化3 F.转化4 G.转化5
(6)上述流程中,可以循环使用的物质为(写化学式):_______。
高三化学实验题中等难度题查看答案及解析
磷酸二氢钾(KH2PO4)是一种高效复合肥。工业上以羟磷灰石精矿[主要成分是Ca5(PO4)3OH,还含有少量石英和氧化铁等杂质]为原料,生产磷酸二氢钾的流程如下:
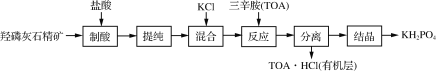
(1)“制酸”过程中生成磷酸的化学方程式为___________________________________________________。
该过程若用硫酸代替盐酸,磷酸的产率明显降低,其原因是___________________________________。
(2)“反应”中加入有机碱——三辛胺(TOA)的目的是____________________________________________。
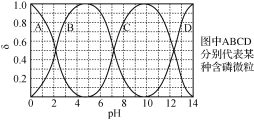
(3)“反应”中,三辛胺的用量会影响溶液的pH。水溶液中H3PO4、H2PO4-、HPO42-、PO43-的分布分数δ随pH的变化如右图所示。
①“反应”中,当pH=____时,停止加入三辛胺。
②使用pH试纸测定溶液pH的操作是_____________________________________________。
(4)查阅资料可知:①磷酸三丁酯、二(2乙基己基)磷酸都是难溶于水的液态有机物。
②磷酸三丁酯对H3PO4和Fe3+有较强的萃取作用。
③二(2乙基己基)磷酸仅对Fe3+有较强的萃取作用。
请根据题中信息,补充完整“提纯”步骤的实验方案:向“制酸”所得粗磷酸中加入活性炭,________________,向有机层中加入蒸馏水,振荡、静置,分液取水层,得到稀磷酸。[实验中须使用的试剂有:二(2乙基己基)磷酸、磷酸三丁酯]
高三化学工业流程中等难度题查看答案及解析
钼是一种稀有金属,为人体及动植物必须的微量元素。某化学兴趣小组在实验室模拟了从铜钼精矿(主要含有Cu2S、MoS2、SiO2、P、As等)中提取分离得到氧化钼的过程
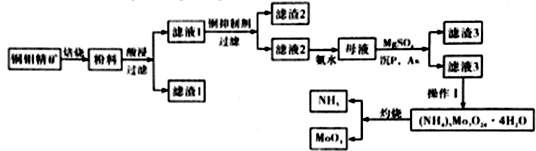
已知:MoO3在869.9K时开始升华
(1)滤渣I的主要成分为__________________。
(2)铜钼精矿中的钼元素在过量的空气中,于一定温度下,很容易被氧化成MoO3,其方程式为________________________,焙烧过程中应控制温度在800~870K左右,其原因为______________。
(3)当NH3∶MoO3等于或稍大于6∶7时,可从氨溶液中结晶出分子式为(NH4)6Mo7O24·4H2O的盐。则在控制好NH3与MoO3比例的前提下,操作I为_________________。
(4)①向滤液1中加入的铜抑制剂有多种,如氰化钠,向含重金属离子的溶液中添加氰化钠,会立即生成沉淀,但是若继续添加氰化钠,沉淀继续与CN-反应,生成[Me(CN)4]2-稳定的配离子,因此需要控制氰化钠的用量,试写出向滤液中加入过量氰化钠的离子方程式_______________________;
②由于氰化钠有剧毒,所以需要对剩余的氰化钠进行处理,通常选用漂白粉回漂白液在酸性条件下将其氧化为两种空气中常见无毒气体,试写出漂白液与氰化钠反应的离子方程式________________。
③除氰化钠外,常用的抑制剂还有亚铁氰化钠,Na4[Fe(CN)6]可与重金属阳离子反应,生成溶度积较小的沉淀,已知Cu2Fe(CN)6 的Ksp=1.00×10-16;滤液中Cu2+的浓度为0.5mol/L。当溶液中离子浓度小于1.00×10-3mol/L 时可认为沉淀完全,则欲处理1L滤液需要0.1 mol/L 的Na4[Fe(CN)6]体积为____________(溶液混合体积变化忽略不计,保留两位小数)。
高三化学简答题困难题查看答案及解析
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
Ⅰ.将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎。
Ⅱ.采用如下装置进行电化学浸出实验
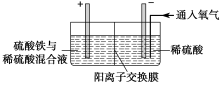
将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并加入少量催化剂。
Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相) R2Cu(有机相)+2H+(水相)
分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。
Ⅳ.电解硫酸铜溶液制得金属铜。
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS2+4H+=Cu2++Fe2++2H2S
2Fe3++H2S=2Fe2++S↓+2H+
①阳极区硫酸铁的主要作用是____________。
②电解过程中,阳极区Fe3+的浓度基本保持不变,原因是______________________。
(2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解。写出上述现象对应的反应式____________________。
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是__________;加入有机萃取剂的目的是__________。
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是____________。
(5)步骤Ⅳ,若电解200 mL 0.5 mol·L-1的CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是__________。
高三化学填空题中等难度题查看答案及解析
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
Ⅰ.将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎
Ⅱ.采用如下装置进行电化学浸出实验
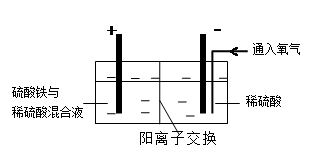
将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并加入少量催化剂。
Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:
2RH(有机相)+ Cu2+(水相)R2Cu(有机相)+ 2H+(水相)
分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。
Ⅳ.电解硫酸铜溶液制得金属铜。
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S↓+ 2H+
① 阳极区硫酸铁的主要作用是________。
② 电解过程中,阳极区Fe3+的浓度基本保持不变,原因是________。
(2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解。写出上述现象对应的反应式________。
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是;加入有机萃取剂的目的是________。
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是________。
(5)步骤Ⅳ,若电解200mL0.5 mol/L的CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是________。
高三化学填空题极难题查看答案及解析
某化学兴趣小组利用下图装置探究验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质为SiO2)。
实验步骤:①组装好仪器,检查装置的气密性良好。②加入药品,打开弹簧夹,从左口不断鼓入空气。③点燃B处的酒精喷灯,高温灼烧石英管中黄铜矿的样品。
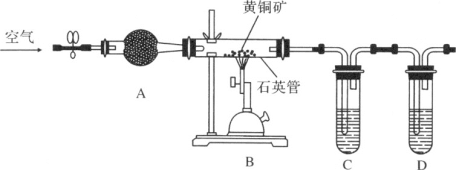
请回答下列问题。
(1)仪器A中的试剂是________,其作用为________。
(2)为检验灼烧氧化黄铜矿产生的气体,则C、D中的试剂可选择________(多选)。
a.Na2S溶液、NaOH溶液
b.BaCl2溶液、NaOH溶液
c.品红溶液、NaOH溶液
d.KMnO4溶液、NaOH溶液
(3)查阅资料:
①样品经煅烧后得到的固体可能为泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO)。
②Cu2O与稀H2SO4的反应为:Cu2O+H2SO4=Cu+CuSO4+H2O
探究Ⅰ:为验证熔渣的成分,取分离出的熔渣少许于试管中,加入适量的稀硫酸溶解,取两份所得液。完成下表中横线上的内容。
| 试样 | 加入试剂及操作 | 实验现象 | 得出结论 |
| 第一份 | 滴入几滴K3Fe(CN)6]溶液 | ________ | 含FeO |
| 第二份 | 滴入几滴________溶液 | 溶液变为血红色 | 含Fe2O3 |
探究Ⅱ:设计实验方案验证泡铜中是否含有Cu2O?________。
(4)为测定CuFeS2的纯度,称取a g的黄铜矿样品充分燃烧后,甲、乙两组同学设计如下两个不同的实验方案(以下纯度结果均用含相应字母的代数式表示)。
甲方案:若C试管中为足量的H2O2和NaOH的混合溶液,吸收完气体后向C中加入过量的BaCl2溶液振荡且静置,经过滤后处理得到固体为w g,则CuFeS2的纯度为________。写出C试管中吸收气体时的总反应的离子方程式________。
乙方案:从上述煅烧产物中分离出泡铜,使其完全溶于稀硝酸并配成250mL的溶液,取出25.00mL该溶液用c mol·L-1的标准液EDTA(用H2Y2-表示)滴定至终点(滴定荆不与杂质反应),消耗EDTA标准液V mL,则CuFeS2的纯度为________。(滴定时的反应为:Cu2++H2Y2-=CuY2-+2H+)
高三化学实验题中等难度题查看答案及解析
某化学兴趣小组利用下图装置探究验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质为SiO2)。
实验步骤:①组装好仪器,检查装置的气密性良好。②加入药品,打开弹簧夹,从左口不断鼓入空气。③点燃B处的酒精喷灯,高温灼烧石英管中黄铜矿的样品。
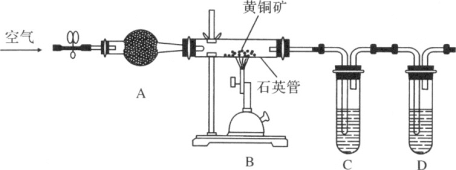
请回答下列问题。
(1)仪器A中的试剂是________,其作用为________。
(2)为检验灼烧氧化黄铜矿产生的气体,则C、D中的试剂可选择________(多选)。
a.Na2S溶液、NaOH溶液
b.BaCl2溶液、NaOH溶液
c.品红溶液、NaOH溶液
d.KMnO4溶液、NaOH溶液
(3)查阅资料:
①样品经煅烧后得到的固体可能为泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO)。
②Cu2O与稀H2SO4的反应为:Cu2O+H2SO4=Cu+CuSO4+H2O
探究Ⅰ:为验证熔渣的成分,取分离出的熔渣少许于试管中,加入适量的稀硫酸溶解,取两份所得液。完成下表中横线上的内容。
| 试样 | 加入试剂及操作 | 实验现象 | 得出结论 |
| 第一份 | 滴入几滴K3Fe(CN)6]溶液 | ________ | 含FeO |
| 第二份 | 滴入几滴________溶液 | 溶液变为血红色 | 含Fe2O3 |
探究Ⅱ:设计实验方案验证泡铜中是否含有Cu2O?________。
(4)为测定CuFeS2的纯度,称取a g的黄铜矿样品充分燃烧后,甲、乙两组同学设计如下两个不同的实验方案(以下纯度结果均用含相应字母的代数式表示)。
甲方案:若C试管中为足量的H2O2和NaOH的混合溶液,吸收完气体后向C中加入过量的BaCl2溶液振荡且静置,经过滤后处理得到固体为w g,则CuFeS2的纯度为________。写出C试管中吸收气体时的总反应的离子方程式________。
乙方案:从上述煅烧产物中分离出泡铜,使其完全溶于稀硝酸并配成250mL的溶液,取出25.00mL该溶液用c mol·L-1的标准液EDTA(用H2Y2-表示)滴定至终点(滴定荆不与杂质反应),消耗EDTA标准液V mL,则CuFeS2的纯度为________。(滴定时的反应为:Cu2++H2Y2-=CuY2-+2H+)
高三化学实验题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析