-
在一定条件下N2 + 3H2⇌ 2NH3 的反应中,起始N2浓度为2mol/L,H2浓度为5mol/L, 反应到2分钟时,测得 NH3 的反应速率为v(NH3 )=0.4mol/(L·min),填空:
(1) NH3 的转化浓度为c(NH3 )=___________ mol/(L·min)
(2)三段式填空:
(mol/L) N2 + 3H2 ⇌ 2NH3
起始浓度 2 5 0
转化浓度 _ _ _
2min后浓度 _ _ _
(3)用v(N2)表示的反应速率为:v(N2)=__________mol/(L·min)
(4)用v(H2)表示的反应速率为:v(H2)=__________mol/(L·min)
高一化学填空题简单题查看答案及解析
-
在一个0.5L密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下发生反应N2(g) + 3H2(g)
2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
A.0.1mol·L-1·min-1 B.0.6mol·L-1·min-1
C.0.3mol·L-1·min-1 D.0.2mol·L-1·min-1
高一化学选择题中等难度题查看答案及解析
-
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g) + 3H2(g)
2NH3(g) ΔH<0,相关数据如下表所示:
容器
甲
乙
丙
相关条件
恒温恒容
绝热恒容
恒温恒压
反应物投料
1mol N2、3mol H2
2mol NH3
2mol NH3
平衡时容器体积
V(甲)
V(乙)
V(丙)
反应的平衡常数K
K(甲)
K(乙)
K(丙)
平衡时NH3的浓度c/mol·L-1
c(甲)
c(乙)
c(丙)
平衡时NH3的反应速率
v/mol·L-1·min-1
v(甲)
v(乙)
v(丙)
下列说法正确的是( )
A.V(甲)>V(丙) B.K(乙)<K(丙) C.c(乙)>c(甲) D.v(甲)=v(丙)
高一化学多选题困难题查看答案及解析
-
一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2
2NH3(正反应是放热反应)。下列有关说法正确的是
A.达到化学反应限度时,可生成2mol NH3
B.向容器中再加入N2,可以加快反应速率
C.降低温度可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
高一化学选择题中等难度题查看答案及解析
-
(16分)(1)氨在国民经济中占有重要地位。
工业合成氨的反应原理为:N2(g)+ 3H2(g)
2NH3(g) △H=―92.4 kJ·mol-1。
①若起始时向容器内放入2mol N2和6mol H2,达平衡后放出的热量为Q,则Q 184.8 kJ(填“>”、“<”或“=”)。
②已知:

1mol N—H键断裂吸收的能量为 kJ。
③某温度下,把10 mol N2与28 mol H2置于容积为10 L的密闭容器内,10 min时反应达到平衡状态,测得氮气的平衡转化率为60%,则10 min内该反应的平均速率v(H2)= mol·L-1·min-1,该温度下反应的平衡常数K = 。欲增大氮气的平衡转化率,可采取的措施有 (写一种措施即可)。
(2)某课外小组用下图所示装置对电解原理进行实验探究。用下图所示装置进行实验。实验过程中,两极均有气体产生,Y极区产生氧气,同时Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
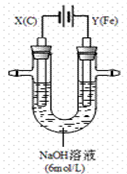
① 电解过程中,X极区溶液的pH (填“增大”、“减小”或“不变”)。
② 电解过程中,Y极发生的两个电极反应为Fe-6e-+8OH-== FeO42-+4H2O和 。
③ 若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少 g。
④在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4 + 3Zn == Fe2O3 +ZnO +2K2ZnO2,该电池正极发生的反应的电极反应式为 。
高一化学填空题困难题查看答案及解析
-
已知合成氨反应的浓度数据如下:
N2 + 3H2
2NH3
起始浓度mol/L
1.0
3.0
0
2秒末浓度mol/L
0.6
1.8
0.8
当用氨气浓度的增加来表示该化学反应速率时,其速率为 ( ).
A. 0.2 mol/(L·s) B. 0.4 mol/(L·s) C. 0.6 mol/(L·s) D. 0.8 mol/(L·s)
高一化学选择题中等难度题查看答案及解析
-
已知合成氨反应的物质的量数据如下:
N2 + 3H2
2NH3
起始物质的量mol
1.0
3.0
0
2秒末物质的量mol
0.6
1.8
0.8
反应在2L容器中进行,当用氢气浓度的减少来表示该化学反应速率时,其速率为( )
A、0.2 mol/(L·s) B、0.3 mol/(L·s) C、0.6 mol/(L·s) D、0.8 mol/(L·s)
高一化学选择题简单题查看答案及解析
-
在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g)
2NH3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是
A.N2、H2、NH3的浓度相等 B.N2、H2、NH3的浓度不再变化
C.N2、H2、NH3在密闭容器中共存 D.反应停止,正、逆反应速率都等于零
高一化学选择题简单题查看答案及解析
-
在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g)
2NH3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是
A.N2、H2、NH3的浓度相等 B.N2、H2、NH3的浓度不再变化
C.N2、H2、NH3在密闭容器中共存 D.反应停止,正、逆反应速率都等于零
高一化学选择题中等难度题查看答案及解析
-
在一定条件下,对于密闭容器中进行的反应:N2 (g) + 3H2 (g)
2NH3 (g),下列说法能充分说明该反应已经达到化学平衡状态的是
A.正、逆反应速率都等于零 B.N2、H2、NH3的浓度均不再变化
C.N2、H2、NH3在容器中共存 D.N2、H2、NH3的浓度相等
高一化学选择题简单题查看答案及解析