-
常温下,向浓度为0.1mol·L-1、体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图中信息回答下列问题:
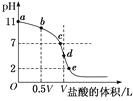
(1)该温度时NH3·H2O的电离常数K=__;
(2)比较b、c、d三点时的溶液中,由水电离出的OH-浓度大小顺序为__;
(3)滴定时,由b点到c点的过程中,下列各选项中数值保持不变的是__(填字母,下同);
A.c(H+)·c(OH-) B. C.
C. D.
D.
(4)根据以上滴定曲线,下列说法正确的是__;
A.点b所示溶液中:c(NH )+c(H+)=c(OH-)+c(NH3·H2O)
)+c(H+)=c(OH-)+c(NH3·H2O)
B.点c所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH )
)
C.点d所示溶液中:c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)
D.滴定过程中可能有:c(NH3·H2O)>c(NH )>c(OH-)>c(Cl-)>c(H+)
)>c(OH-)>c(Cl-)>c(H+)
(5)滴定过程中所用盐酸的pH=___,d点之后若继续加入盐酸至图像中的e点(此时不考虑NH4+水解的影响,忽略混合时溶液体积变化),则e点对应的横坐标为___。
-
常温下,向20 mL 0.1 mol•L-1氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。
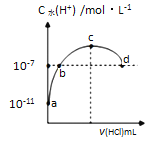
则下列说法正确的是
A. 常温下,0.1mol•L-1氨水的电离常数K约为1×10-5mol•L-1
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)=c(Cl-)
D. d点代表两溶液恰好完全反应
-
常温下,向20mL 0.1mol/L氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是( )
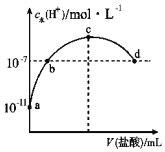
A.常温下,0.1 mol/L氨水中,c (OH﹣)=1×10﹣5 mol/L
B.b点代表溶液呈中性
C.c点溶液中c(NH4+)=c(Cl﹣)
D.d点溶液中:c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
-
常温下,向20 mL 0.1 mol·L-1氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法不正确的是( )
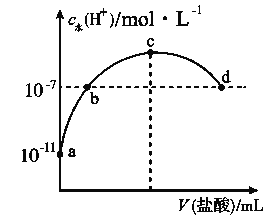
A. 常温下,0.1 mol·L-1氨水中 的电离常数
的电离常数 约为
约为
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)<c(Cl-)
D. b点代表溶液呈中性
-
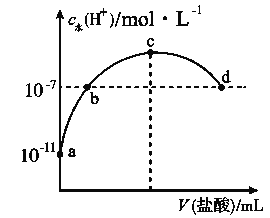
常温下,向20 mL 0.1 mol·L-1氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法不正确的是( )
A. 常温下,0.1 mol·L-1氨水中 的电离常数
的电离常数 约为
约为
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)<c(Cl-)
D. b点代表溶液呈中性
-
常温下,向20 mL 0.1 mol·L-1氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是( )
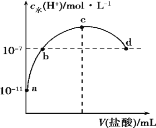
A. 常温下,0.1 mol·L-1氨水中NH3·H2O的电离常数K约为1×10-5
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)=c(Cl-)
D. d点代表两溶液恰好完全反应
-
常温下,向20mL0.1mol/L氨水中滴加一定浓度的稀盐酸,溶液中水电离的氢离子浓度随加入盐酸体积的变化如右图所示。下列说法错误的是
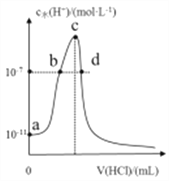
A. 常温下,0.1mol/L氨水的电离平衡常数Kb约为1.0×10-5
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)-)
D. c点溶质为NH4Cl
-
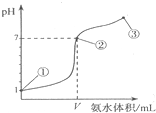
常温下,向20 mL某浓度的盐酸中逐滴加入0.1 mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示。
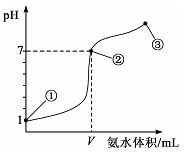
下列叙述正确的是
A.盐酸的物质的量浓度为l mol/L
B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-)
C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20
D.在点③所示溶液中:由水电离出的c(OH-)>l0-7mol/L
-
常温下,向20mL某盐酸溶液中逐滴加入0.1mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示,下列叙述正确的是( )
A.盐酸的物质的量浓度为1mol/L
B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-)
C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20
D.在点③所示溶液中:由水电离出的c(OH-)>10-7mol/L
-
常温下,向体积为10 mL、物质的量浓度均为0.1 mol/L的盐酸和醋酸的混合溶液中滴入0.1 mol/L NaOH溶液。下列说法错误的是( )
A.加入NaOH溶液后,溶液一定满足: c(H+)+c(Na+)=c(OH-)+c(C1-)+c(CH3COO-)
B.加入10 mLNaOH溶液时,溶液满足(溶液体积变化忽略不计):
c(CH3COO-)+c(CH3COOH)=0.05 mol/L
C.加入15 mLNaOH溶液时,呈酸性,溶液满足:
c(Na+)>c(C1-)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.加入足量NaOH溶液时,溶液中发生的中和反应的热化学方程式表示为:
H+(aq)+OH-(aq)=H2O(1) ΔH=-57.3 KJ/mol

C.
D.
)+c(H+)=c(OH-)+c(NH3·H2O)
)
)>c(OH-)
)>c(OH-)>c(Cl-)>c(H+)







