-
我国有世界储量第一的天然石膏(主要成分CaSO4),同时也有大量磷酸工业副产品石膏,可用于硫酸及水泥的联合生产。硫酸钙在高温下被CO还原,发生的反应有:
I.CaSO4(s)+4CO(g)⇌CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)⇌4CaO(s)+4SO2(g) K3
上述反应的平衡常数的对数值(lgK)与温度(T)的关系如图所示。下列说法错误的是( )
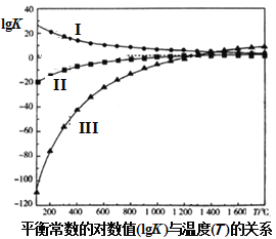
A.反应II的△H>0
B.lgK3=4lgK2−lgK1
C.使用适当的催化剂能够加快反应速率,提高原料的平衡转化率
D.调控适当的温度可以抑制反应I促进反应III而得到较纯净的CaO
-
最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。已知磷灰石的主要成分是Ca3(PO4)2,具体生产流程如图:
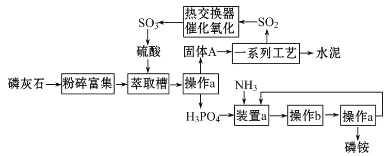
回答下列问题:
(1)装置a用磷酸吸收NH3。若该过程在实验室中进行,请画出装置a的示意图:_____。
(2)热交换器是实现冷热交换的装置。化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是_______________。
(3)依题意猜测固体A中一定含有的物质的化学式是___________(结晶水部分不写)。
(4)利用生产磷铵排放的废渣磷石膏制取硫酸,其中SO2生产硫酸的工艺流程图如图所示:

①在A处二氧化硫被氧化成三氧化硫,设备A的名称是___________,设备A中发生反应的化学方程式是______________。为提高三氧化硫的产率,该处应采用_____(填“等温过程”或“绝热过程”)为宜。
②在D处进行二次催化处理的原因是_______________________。
③B处气体混合物主要是氮气和三氧化硫.此时气体经过C后不立即进入D是因为:___________。
④20%的发烟硫酸(SO3的质量分数为20%)1吨需加水_______吨(保留2位有效数字)才能配制成98%的成品硫酸。
(5)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是___________________。
| A.NaOH溶液、酚酞试液 | B.KMnO4溶液、稀硫酸 |
| C.碘水、淀粉溶液 | D.氨水、酚酞试液 |
-
最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。已知磷灰石的主要成分是Ca3(PO4)2。具体生产流程如下:
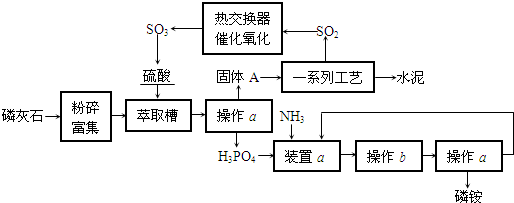
回答下列问题:
(1)装置a用磷酸吸收NH3.若该过程在实验室中进行,请画出装置a的示意图.___________;
(2)热交换器是实现冷热交换的装置.化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是___________;
(3)依题意猜测固体A中一定含有的物质的化学式是___________(结晶水部分不写).
(4)利用生产磷铵排放的废渣磷石膏制取硫酸,其中SO2生产硫酸的工艺流程图如图所示:
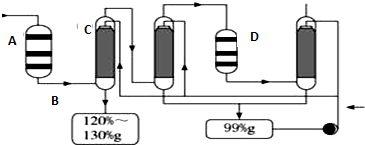
①在A处二氧化硫被氧化成三氧化硫,设备A的名称是___________,设备A中发生反应的化学方程式是___________,为提高三氧化硫的产率,该处应采用___________(填“等温过程”或“绝热过程”)为宜。
②在D处进行二次催化处理的原因是___________;
③B处气体混合物主要是氮气和三氧化硫。此时气体经过C后不立即进入D是因为:___________;
④20%的发烟硫酸(SO3的质量分数为20%)1吨需加水___________吨(保留2位有效数字)才能配制成98%的成品硫酸。
(5)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾.能用于测定硫酸尾气中SO2含量的是___________(选填字母)
A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液
-
最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。已知磷灰石的主要成 分是Ca3(PO4)2,具体生产流程如图:
分是Ca3(PO4)2,具体生产流程如图:
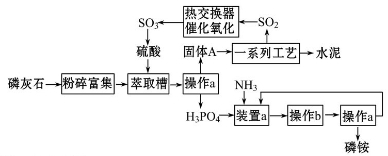
回答下列问题:
(1)装置a用磷酸吸收NH3。若该过程在实验室中进行,请画出装置a的示意图:_____。
(2)热交换器是实现冷热交换的装置。化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是_______________。
(3)依题意猜测固体A中一定含有的物质的化学式是___________(结晶水部分不写)。
(4)利用生产磷铵排放的废渣磷石膏制取硫酸,其中SO2生产硫酸的工艺流程图如图所示:
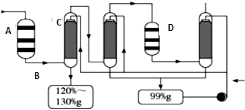
①在A处二氧化硫被氧化成三氧化硫,设备A的名称是___________,设备A中发生反应的化学方程式是______________。为提高三氧化硫的产率,该处应采用_____(填“等温过程”或“绝热过程”)为宜。
②在D处进行二次催化处理的原因是_______________________。
③B处气体混合物主要是氮气和三氧化硫.此时气体经过C后不立即进入D是因为:___________。
④20%的发烟硫酸(SO3的质量分数为20%)1吨需加水_______吨(保留2位有效数字)才能配制成98%的成品硫酸。
(5)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是___________________。
A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀硫酸
C.碘水、淀粉溶液 D.氨水、酚酞试液
-
工业上利用某地磷矿(主要成分是磷酸钙,质量分数为80%,另外还含有石英及少量碳酸镁、氧化铝等不含磷杂质)制取磷铵,并用制磷铵排放的废渣磷石膏制取硫酸、水泥。其生产流程如下:

请分析并回答下列问题:
(1)窑气(SO2)进入接触室前需要净化的目的是_________________;
(2)实验室完成操作b的方法是__________________过滤、洗涤和干燥等;
(3)下图表示接触室和吸收塔的内部构造。吸收塔内安装有许多瓷环作用是_________________;

(4)接触室中进行学反应是:2SO2(g) + O2(g) 2SO3(g) △H=-296.4kJ/mol。接触室内安装热交换器的目的是____________________。图1表示接触室中催化剂随温度变化图象,图2表示SO2的转化率a(SO2)随温度T及压强P的变化图象。你认为接触室中最合适的温度和压强是__________________。
2SO3(g) △H=-296.4kJ/mol。接触室内安装热交换器的目的是____________________。图1表示接触室中催化剂随温度变化图象,图2表示SO2的转化率a(SO2)随温度T及压强P的变化图象。你认为接触室中最合适的温度和压强是__________________。
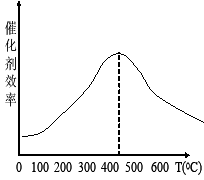
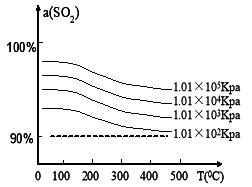
图1 图2
(5)硫酸厂的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸厂尾气中SO2含量的试剂是______________(填字母代号):
A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀H2SO4
C.氨水、酚酞试液 D.碘水、淀粉溶液
(6)在述生产过程中循环利用的物质有__________________(填化学式);
(7)磷铵是一种常用复合肥,经分析其中氮与磷原子数之比为3:2,在生产过程中平均有7%的磷元素损失,该厂日均生产74.1吨磷铵,要维持正常生产,每天需运入这种磷矿至少__________吨。
-
磷石膏是磷氨厂生产硫酸和磷酸所排放的废渣 主要成分为
主要成分为 ,大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
,大量堆积既占用土地,又易造成环境污染和硫资源的浪费,所以可从资源综合利用的角度将磷石膏转化成硫酸钾和氯化钙晶体,工艺流程如下:
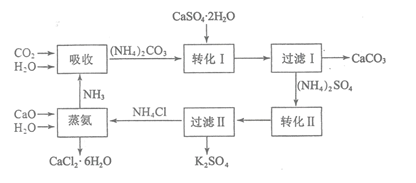
请回答以下问题:
 为了提高原料的利用率,吸收流程中通入
为了提高原料的利用率,吸收流程中通入 和
和 的先后顺序最好为______。
的先后顺序最好为______。
 碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为______。
碳酸铵溶液与磷石膏悬浊溶液混合后发生转化I的离子反应方程式为______。
 工艺流程中除了所给出的
工艺流程中除了所给出的 、
、 、
、 、
、 等原料外,在转化Ⅱ的过程中还需要加入______原料。
等原料外,在转化Ⅱ的过程中还需要加入______原料。
 过滤Ⅱ后所得滤液
过滤Ⅱ后所得滤液 溶液,确认其中含有
溶液,确认其中含有 的方法是:______;
的方法是:______;
 氯化钙结晶水合物
氯化钙结晶水合物 是目前常用的无机储热材料,选择的依据是因为______
是目前常用的无机储热材料,选择的依据是因为______ 选填序号
选填序号 ;
;
A.熔点较低 熔化
熔化
 能导电
能导电  能制冷
能制冷  无毒
无毒
 已知不同温度下
已知不同温度下 在100g水中达到饱和时溶解的量如下表:
在100g水中达到饱和时溶解的量如下表:
 时
时 的饱和溶液
的饱和溶液 冷却到
冷却到 ,可析出
,可析出 晶体______g。
晶体______g。
 上述工艺流程中循环利用的物质是______;还有一种物质,只要其纯净,也可以被循环利用,它是______
上述工艺流程中循环利用的物质是______;还有一种物质,只要其纯净,也可以被循环利用,它是______ 均填化学式
均填化学式 。
。
-
磷石膏是湿法生产磷酸排出的工业废渣,主要成分是CaSO4·2H2O。
⑴CaSO4·2H2O脱水反应相关的热化学方程式为:
CaSO4·2H2O(s)=CaSO4·1/2H2O(s)+3/2H2O(g) ΔH1=83.2 kJ·mol-1
CaSO4·2H2O(s)=CaSO4(s)+2H2O(l) ΔH2=26 kJ·mol-1
H2O(g)=H2O(l) ΔH3=-44 kJ·mol-1
则反应CaSO4·1/2H2O(s)=CaSO4(s)+1/2H2O(g)的ΔH4=____kJ·mol-1。
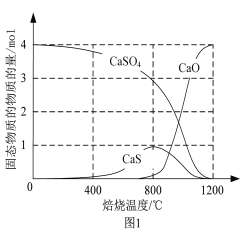
⑵用合适的还原剂可以将CaSO4还原,所得SO2可用于工业生产硫酸。
①以CO作还原剂,改变反应温度可得到不同的产物。不同温度下反应后所得固体成分的物质的量如右图1所示。在低于800℃时主要还原产物为______;高于800℃时主要发生的反应的化学方程式为______。
②以高硫煤为还原剂焙烧2.5 小时,不同条件对硫酸钙转化率的影响如下图2所示。CaCl2的作用是______;当温度高于1200 ℃时,无论有无CaCl2,CaSO4的转化率趋于相同,其原因是______。
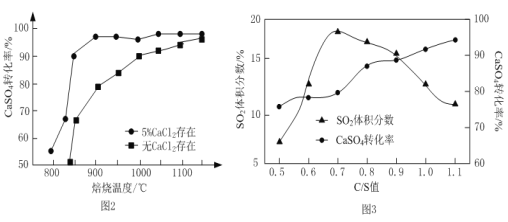
③以C作还原剂,向密闭容器中加入相同质量的几组不同C/S值(炭粉与CaSO4的物质的量之比)的混合物在1100℃加热,结果如上图3所示。当C/S值为0.5时,反应产物为CaO、SO2和CO2;当C/S值大于0.7时,反应所得气体中SO2的体积分数不升反降,其主要原因可能是______。
⑶利用反应CaSO4(s)+(NH4)2CO3(aq) CaCO3(s)+(NH4)2SO4(aq)可以将磷石膏转化为硫酸铵。若反应达到平衡后溶液中c(SO42-)=2.0 mol·L-1,此时溶液中c(CO32-)=__________。[已知:Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=3.2×10-7]
CaCO3(s)+(NH4)2SO4(aq)可以将磷石膏转化为硫酸铵。若反应达到平衡后溶液中c(SO42-)=2.0 mol·L-1,此时溶液中c(CO32-)=__________。[已知:Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=3.2×10-7]
-
磷石膏是湿法生产磷酸排出的工业废渣,主要成分是CaSO4·2H2O。
⑴CaSO4·2H2O脱水反应相关的热化学方程式为:
CaSO4·2H2O(s)=CaSO4· H2O(s)+
H2O(s)+ H2O(g) ΔH1=83.2 kJ·mol-1
H2O(g) ΔH1=83.2 kJ·mol-1
CaSO4·2H2O(s)=CaSO4(s)+2H2O(l) ΔH2=26 kJ·mol-1
H2O (g)=H2O(l) ΔH3=-44 kJ·mol-1
则反应CaSO4· H2O(s)=CaSO4(s)+
H2O(s)=CaSO4(s)+  H2O(g)的ΔH4=_________kJ·mol-1。
H2O(g)的ΔH4=_________kJ·mol-1。
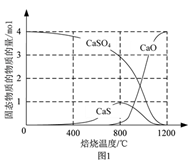
⑵用合适的还原剂可以将CaSO4还原,所得SO2可用于工业生产硫酸。
①以CO作还原剂,改变反应温度可得到不同的产物。不同温度下反应后所得固体成分的物质的量如图1所示。在低于800 ℃时主要还原产物为___________;高于800 ℃时主要发生的反应的化学方程式为___________。
②以高硫煤为还原剂焙烧2.5 小时,不同条件对硫酸钙转化率的影响如下图2所示。CaCl2的作用是___________;当温度高于1200 ℃时,无论有无CaCl2,CaSO4的转化率趋于相同,其原因是___________。
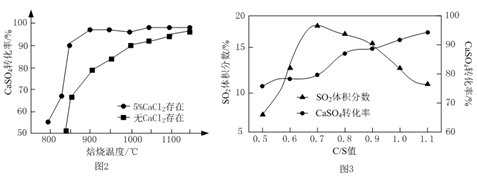
③以C作还原剂,向密闭容器中加入相同质量的几组不同C/S值(炭粉与CaSO4的物质的量之比)的混合物在1100 ℃加热,结果如上图3所示。当C/S值为0.5时,反应产物为CaO、SO2和CO2;当C/S值大于0.7时,反应所得气体中SO2的体积分数不升反降,其主要原因可能是___________。
⑶利用反应CaSO4(s)+(NH4)2CO3(aq) CaCO3(s)+(NH4)2SO4(aq)可以将磷石膏转化为硫酸铵。若反应达到平衡后溶液中c(SO42-)=2.0 mol·L-1,此时溶液中c(CO32-)=___________。(已知Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=3.2×10-6)
CaCO3(s)+(NH4)2SO4(aq)可以将磷石膏转化为硫酸铵。若反应达到平衡后溶液中c(SO42-)=2.0 mol·L-1,此时溶液中c(CO32-)=___________。(已知Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=3.2×10-6)
-
)【化学—选修化学与技术】
工业上以磷肥生产形成的副产物石膏(CaSO4·2H2O)与焦炭为原料可生产硫酸,同时
可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。
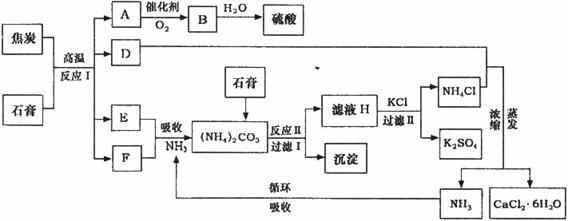
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
|  压 强 / M Pa 压 强 / M Pa
转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(4)检验滤液H中含有CO 的方法是___________________________________。
的方法是___________________________________。
(5)氯化钙结晶水合物( )是目前常用的无机储热材料,选择的依据是___________ (填序号)。
)是目前常用的无机储热材料,选择的依据是___________ (填序号)。
a.熔点较低(29℃熔化) b.能导电 c.易溶于水 d.无毒
-
(15分)
工业上以磷肥生产形成的副产物石膏(CaSO4·2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。
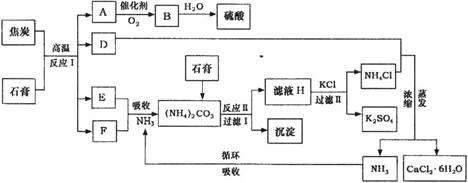
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
|  压 强 / M Pa 压 强 / M Pa
转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(4)检验滤液H中含有CO 的方法是___________________________________。
的方法是___________________________________。
(5)氯化钙结晶水合物( )是目前常用的无机储热材料,选择的依据是___________ (填序号)。
)是目前常用的无机储热材料,选择的依据是___________ (填序号)。
a.熔点较低(29℃熔化) b.能导电 c.易溶于水 d.无毒

















