已知硫酸钠晶体()的物质的量为1.5mol,请计算填空:
(1)所含钠离子的物质的量是________,钠离子的数目是________。
(2)所含硫酸根离子的物质的量是________,所含氧原子的数目是________。
(3) 硫酸钠晶体()是_______________________(填“纯净物”或“混合物”)
高一化学填空题简单题
已知硫酸钠晶体()的物质的量为1.5mol,请计算填空:
(1)所含钠离子的物质的量是________,钠离子的数目是________。
(2)所含硫酸根离子的物质的量是________,所含氧原子的数目是________。
(3) 硫酸钠晶体()是_______________________(填“纯净物”或“混合物”)
高一化学填空题简单题
已知硫酸钠晶体()的物质的量为1.5mol,请计算填空:
(1)所含钠离子的物质的量是________,钠离子的数目是________。
(2)所含硫酸根离子的物质的量是________,所含氧原子的数目是________。
(3) 硫酸钠晶体()是_______________________(填“纯净物”或“混合物”)
高一化学填空题简单题查看答案及解析
下列关于0.2 mol硫酸铜晶体(CuSO4·5H2O)的说法中,错误的是( )
A.含有铜离子的数目为0.2NA B.含有结晶水的数目为NA
C.含有氢原子的数目为2NA D.含有氧原子的数目为0.8NA
高一化学单选题简单题查看答案及解析
(10分)计算填空:
(1)(2分)1mol某金属单质与足量的H2SO4反应,放出1.5molH2(标况下)并转化为具有Ne原子的电子层结构的离子,则该金属在周期表的位置________。
(2)(6 分)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
_ aA (g)+ bB (g) 2C(g)
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则①a=________,b=________;
②2S内B的反应速率=。
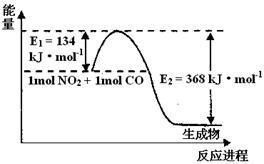
(3)(2分) 1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 ________。
高一化学填空题简单题查看答案及解析
下列叙述正确的是
A. CH4的摩尔质量为16 g,1.5mol CH4含6mol氢
B. 物质的量是表示物质粒子数目的物理量,摩尔是其单位
C. 利用气体摩尔体积计算时,气体可以是纯净物也可以是混合物
D. 将40gNaOH固体溶于1L水中配成溶液,溶液中氢氧化钠的浓度为1mol/L
高一化学单选题中等难度题查看答案及解析
(1)谋晶体的化学式为Na0.35CoO2 • 1.3H2O。试计算:该晶体的摩尔质量是________;
钴原子与氧原子的物质的量之比是________; 1mol该晶体中含有的氧原子数目
是。
(2)每组中都有一种物质与其他物质在分类上或性质上不同,试分析每组中物质的组成规律或性质特点,将这种物质找出来,并说明理由。
①O2 CO H2 Mg ________ , ________;
②CO2 SO3 CO CaO ________ , ________。
(3)10g碳酸钙溶于100ml盐酸溶液,恰好完全反应。写出该反应的离子方程式 ,标准状况下生成气体体积________L,盐酸的物质的量的浓度________mol/L.
高一化学填空题简单题查看答案及解析
在200mL某硫酸盐溶液中,含硫酸根离子1.5NA个,含金属离子NA个,则该硫酸盐溶液的物质的量浓度为
A.2.5mol/L B.5mol/L C.7.5mol/L D.2mol/L
高一化学选择题中等难度题查看答案及解析
用NA表示阿伏加德罗常数的值,下列有关物质结构中的说法正确的是
A.1 mol AlCl3 固体中,离子键的数目为3NA
B.1.5 g CH3+中含有的电子数为0.9NA
C.标准状况下,1 mol H2O2的体积小于22.4 L
D.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构
高一化学单选题中等难度题查看答案及解析
在200 ml某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子,则该硫酸盐的物质的量浓度为 ( )
A. 2 mol·L-1 B. 2.5 mol·L-1 C. 5 mol·L-1 D. 7.5 mol·L-1
高一化学单选题中等难度题查看答案及解析
在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
A. 2 mol·L-1 B. 2.5 mol·L-1 C. 5 mol·L-1 D. 7.5 mol·L-1
高一化学单选题中等难度题查看答案及解析
在200 mL某硫酸盐溶液中,含有1.5 NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
A.2 mol·L-1 B.2.5 mol·L-1 C.5 mol·L-1 D.7.5 mol·L-1
高一化学选择题简单题查看答案及解析