-
下列叙述中不正确的是( )
A. 元素在周期表中的位置,反映了元素的原子结构和元素的性质
B. 硫酸的酸性比次氯酸的酸性强,所以硫的非金属性比氯强
C. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
D. 人们在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
高一化学单选题简单题查看答案及解析
-
下列叙述中不正确的是
A.元素在周期表中的位置,反映了元素的原子结构和元素的性质
B.硫酸的酸性比次氯酸的酸性强,所以硫的非金属性比氯强
C.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
D.人们在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
高一化学单选题简单题查看答案及解析
-
周期表中元素的位置、原子结构与元素的性质之间关系密切。下列说法正确的是( )
A. Be(OH)2既可以和强酸反应,又可以和强碱反应
B. ①硫酸比次氯酸稳定;②S2-易被氯气氧化,均能说明氯元素的非金属性比硫元素强
C. 中学教材所附周期表中第15列元素的最高价氧化物对应水化物的化学式均为H3RO4
D. HF的沸点比HCl 高,是因为H-F键比H-Cl键强
高一化学单选题简单题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素性质,下列说法正确的是
A. 因为酸性HF<HCl<HBr<HI, 所以非金属性F<Cl<Br<I
B. 因为Cl2可以从NaBr溶液中置换出Br2,所以非金属性Cl>Br
C. 金属Na与O2在加热时有Na2O2生成,可以推断Li与O2在加热时有Li2O2生成
D. 同一主族的元素的原子,最外层电子数相同,化学性质完全相同
高一化学单选题中等难度题查看答案及解析
-
元素在周期表中的位置反映了元素的原子结构和元素的性质,下列说法正确的是( )
A. 同一主族的元素的原子,最外层电子数相同,化学性质完全相同
B. 短周期元素形成简单离子后,最外层都达到8电子稳定结构
C. 第三周期元素的最高正化合价等于它所处的主族序数
D. 同一元素的最高价氧化物的水化物不可能既表现酸性又表现碱性
高一化学单选题中等难度题查看答案及解析
-
元素在周期表中的位置反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
B.短周期元素形成简单离子后,最外层都达到8电子稳定结构
C.第三周期元素的最高正化合价等于它所处的主族序数
D.同一元素的最高价氧化物的水化物不可能既表现酸性又表现碱性
高一化学单选题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
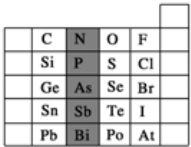
(1)阴影部分元素P在元素周期表中的位置为 。根据元素周期律预测:酸性强弱H3PO4 H3AsO4。(用“>”“<”或“=”表示)
(2)已知阴影部分As元素的原子核内质子数为33,则Sn2+ 的核外电子数为 。
(3)下列说法正确的是 。
A.C、N、O、F的原子半径随着原子序数的增大而增大
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.对于短周期元素,两种简单离子不可能相差3个电子层
D.HF、HCl、HBr、HI的还原性依次减弱
(4)在离子RO3n-中含有x个核外电子,R原子的质量数为A,则R原子中子数是 。
高一化学填空题中等难度题查看答案及解析
-
(14分)元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。
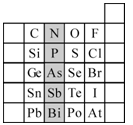
(1)阴影部分元素N在元素周期表中的位置为________。
根据元素周期律,预测:酸性强弱 H3AsO4 ________H3PO4。(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为______,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度________(选填“更大”、“更小”或“相同”) 。
(3)O原子与氢原子可形成10电子阴离子,写出该阴离子的电子式________
(4)Cl2、Br2、I2均可从中海洋提取,Br2的提取是采用向酸化的浓海水中通入Cl2置换出Br-的方法而获得,有关的离子方程式为________,利用Br2具有较强的氧化性,SO2具有较强的还原性,将吹出的Br2通入溶有SO2气体的溶液中,进行溴的富集,此时溶液中存在的主要离子是____________________________。
高一化学填空题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
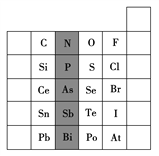
(1)阴影部分元素N在元素周期表中的位置为____周期第____族。根据元素周期律,预测酸性强弱:H3AsO4____H3PO4(填“>”或“<”)。
(2)S的最高化合价和最低化合价的代数和为____,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度____(填“更大”“更小”或“相同”)。
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是____。
(4)下列说法错误的是____(填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱
高一化学填空题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
(1)阴影部分元素N在元素周期表中的位置为第______周期第______族.
根据元素周期律,预测:酸性强弱 H3AsO4______H3PO4.(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为______,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度______.(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是______.
(4)下列说法正确的是______
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.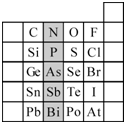
高一化学解答题中等难度题查看答案及解析