-
Fe、Ni均为Ⅷ族元素,与C、N、O、P等组成的化合物有广泛的用途。回答下列问题:
(1)基态Ni2+的价层电子轨道表达式为________,C、N、O的第一电离能从小到大的顺序为________。
(2)N、P可形成一些复杂离子,如(CH3)3NH+、NO2+、PCl6-等。
①(CH3)3NH+ 中N原子的杂化类型为___,NO2+的空间构型为______________。
②PCl5是一种白色固体,在加压下于148℃时液化,形成一种能导电的熔体。熔体能导电的原因是___________。
(3)Fe、Ni易与CO形成配合物,Fe(CO)5中σ键与π键个数比为______,Ni(CO)4熔点-25℃,沸点43℃,不溶于水,溶于乙醇、苯等有机溶剂,Ni(CO)4为______晶体。
(4)FeO、NiO的晶体类型与结构和NaCl相同。
① 熔点FeO_____NiO(填“>”、“<”或“=”)。
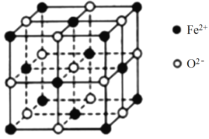
② FeO 晶胞如下图,Fe2+的配位数为_______。
③ FeO在氧气中加热,部分Fe2+被氧化为Fe3+,晶体结构产生铁离子缺位的缺陷,其组成变为FexO(x<1),测得晶胞边长为a cm,密度为⍴g·cm-3,则x=_______。
-
铜、锌及其化合物用途广泛。回答下列问题:
(1)Zn2+的价层电子轨道表达式为__。
(2)元素第二电离能(I2):Zn_Cu(填“>”“<”或“=”)。
(3)卤化锌的熔点如表所示:
| ZnF2 | ZnCl2 | ZnBr2 | ZnI2 |
| 溶点/℃ | 872 | 275 | 394 | 446 |
①ZnCl2、ZnBr2、ZnI2的熔点呈表中变化规律的原因___。
②ZnF2的熔点远高于其它三种卤化锌,其原因为___。
(4)邻氨基吡啶(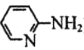 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。

①邻氨基吡啶的铜配合物中,C原子杂化类型为__。
②1mol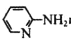 中σ键和π键的数目之比为__。
中σ键和π键的数目之比为__。
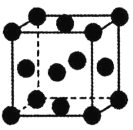
(5)铜的晶胞为面心立方(如图所示),已知晶胞参数为a,则该晶胞的空间利用率为__。(圆周率为π)。
-
氟及其化合物用途非常广泛。回答下列问题:
(1)基态F原子的价层电子的轨道表达式为____。
(2)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为_____,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_____和_____(各举一例)。
(3)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中中心原子的杂化类型是_____;氟化铵中存在的化学键是_____(填字母)。
中中心原子的杂化类型是_____;氟化铵中存在的化学键是_____(填字母)。
A.离子键 B.σ键 C.π键 D.氢键
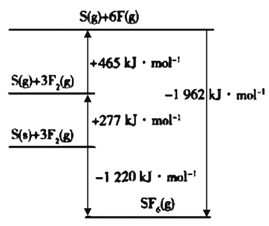
(4)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为____kJ·mol-1,S-F键的键能为____kJ·mol-1。
-
铁、钴(Co)属于第四周期第VIII族元素,含铁、钴化合物具有诸多用途。回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________。
(2)Co的配合物[Co(NH3)5Cl]SO4是一种重要的化合物。
①SO42-的空间立体构型为___________,其中S原子的杂化轨道类型是___________,写出一种与SO42-互为等电子体的分子的化学式:______________。
②[Co(NH3)5Cl]SO4中,N、O、S三种元素的第一电离能由大到小的顺序为_______________。
③[Co(NH3)5Cl]SO4中,存在___________(填字母)
a.离子键 b.金属键 c.配位键 d.非极性键 e.极性键
(3)铁氰化钾{K3 [Fe(CN)6]}溶液是检验Fe2+常用的试剂。
①1mol [Fe(CN)6]3-含 键的数目为__________。
键的数目为__________。
②CN-能与多种离子形成配合物,碳原子提供孤电子对,而不是氮原子,其原因是____________。
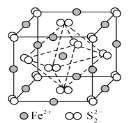
③FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______g•cm-3;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为_________nm。
-
由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态Cl原子核外电子排布式为____,P、S、Cl的第一电离能由大到小顺序为____。
(2)SCl2分子中的中心原子杂化轨道类型是____,该分子构型为_____。
(3)Ni与CO能形成配合物Ni(CO)4,该分子中配位键个数为____;以“—”表示σ键、“→”表示配位键,写出Ni(CO)4分子的结构式____。
(4)已知MgO与NiO的晶体结构(如图)相同,其中Mg2+和Ni2+的离子半径分别为66 pm和69pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是____。
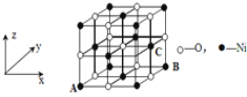
(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为____。
(6)金刚石晶胞含有___个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______a,列式表示碳原子在晶胞中的空间占有率____(请用r和a表示不要求计算结果)。

-
氮、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物用途广泛。回答下列问题:
(1)基态P原子的核外电子排布式为___________________
(2)自然固氮现象发生的一系列化学变化: ,解释了民谚“雷雨发庄稼”的原理。
,解释了民谚“雷雨发庄稼”的原理。
① 分子结构中σ键和π键数目之比为__________
分子结构中σ键和π键数目之比为__________
② 中N原子采取__________杂化方式,写出它的一种等电子体的化学式:__________。
中N原子采取__________杂化方式,写出它的一种等电子体的化学式:__________。
③已知酸性: ,下列相关见解合理的是__________。
,下列相关见解合理的是__________。
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C. 中氮元素的正电性更高,在水溶液中更易电离出
中氮元素的正电性更高,在水溶液中更易电离出 ,酸性强于
,酸性强于
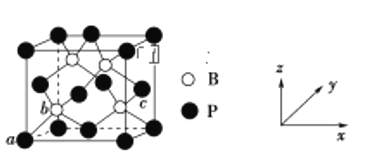
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图所示,图中a点和b点的原子坐标参数分别为(0,0,0)、 ,则c点的原子坐标参数为__________。已知该晶体密度为
,则c点的原子坐标参数为__________。已知该晶体密度为 ,则B—P键的键长为__________pm(阿伏加德罗常数用
,则B—P键的键长为__________pm(阿伏加德罗常数用 表示,列出计算式即可)。
表示,列出计算式即可)。
 。
。
-
铁及其化合物是日常生活生产中应用广泛的材料。请回答下列问题:
(1)基态铁原子的价电子轨道表达式为_____________________ 。
(2)铁元素常见的离子有Fe2+和Fe3+,稳定性Fe2+____Fe3+(填“大于”“”或“小于”),原因是______________________ 。
(3) 纳米氧化铁能催化火箭推进剂NH4ClO4的分解,NH4+的结构式为_________________(标出配位键),空间构型为_______________,其中氮原子的杂化方式为_______________;与ClO4-互为等电子体的分子或离子有______ (任写一种)。
(4)某种离子型铁的氧化物晶胞如图所示,它由A、B 方块组成。则该氧化物中Fe2+、Fe3+、O3-的个数比为___________(填最简整数比)。
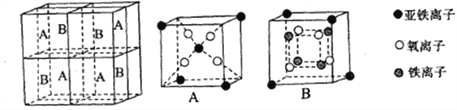
(5)铁有δ、γ、α三种同素异形体,如下图所示。
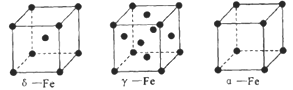
γ-Fe晶体的一个晶胞中所含有的铁原子数为________,δ-Fe、α-Fe两种晶胞中铁原子的配位数之比为_________。
已知δ-Fe晶体的密度为dg/cm3,NA表示阿伏伽德罗常数的数值,则Fe原子半径为_______Pm (列表达式)。
-
硅及其化合物有许多用途,回答下列问题:
(1)基态Si原子价层电子的排布图(轨道表达式)为_________,含有长硅链的化合物不是氢化物,而是氯化物。主要原因是F比H多了一种形状的原子轨道,该原子轨道的形状为___________。
(2)SiF4分子的立体构型为_______形,SiCl4的熔、沸点均高于SiF4,主要原因是________________。
(3)SiF4可KF反应得K2SiF6晶体,该晶体可用于制取高纯硅,K2SiF6晶体中微观粒子之间的作用力有______。
a.离子键 b.共价键 c.配位键 d.分子间作用力 e.氢键
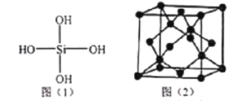
(4)H4SiO4的结构简式如图(1),中心原子Si的轨道杂化类型为_________,H4SiO4在常温下能稳定存在,但H4CO4不能,会迅速脱水生成H2CO3,最终生成CO2,主要原因是___________。
(5)硅的晶胞结构如图(2)所示,若该立方晶胞的边长为a nm,阿伏伽德罗常数的数值为NA,则距离最近的两个硅原子间的距离为_____nm,晶体硅密度的计算表达式为_____g/cm3。
-
镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
(1)Fe3+价层电子的轨道表达式(电子排布图)为__。
(2)晶体硅属于______晶体。硅能形成多种化合物(如SiH4、Si2H4等),SiH4的分子的立体构型为____;Si2H4分子中含有的σ键和π键的数目之比为____。
有机物种类繁多的原因其中之一就是因为碳原子之间既可以形成单键又可以形成双键和三键,Si和Ge与C是同主族价电子数相同,但是Si和Ge就难形成双键或三键,原因是________
(3)Mg、Al、Si的第一电离能由大到小顺序:______________
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是______。
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为______;设Ag原子半径为rcm,阿伏加德罗常数的值用NA表示,则Ag晶体的密度为______g·cm-3(写出表达式)。

-
(14分)铜是第四周期重要的过渡元素之一,其单质及化合物具有广泛用途。
请回答下列有关问题:
⑴ 铜原子的基态电子排布式是▲ 。比较第一电离能Cu▲ Zn(填 “>”、“=”、“<”),说明理由▲ 。
⑵氮和铜形成某种化合物的晶胞结构如图所示,则其化学式为▲ 。(每个球均表示1个原子)

⑶铜可以形成多种多样的配合物。
① NH3可以和很多过渡金属形成配合物。NH3分子中心原子的杂化类型为▲ 杂化,与NH3互为等电子体的粒子有▲ 。(只写其中一种)
②向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。试用离子方程式表示其原因 ▲ 、 ▲ 。
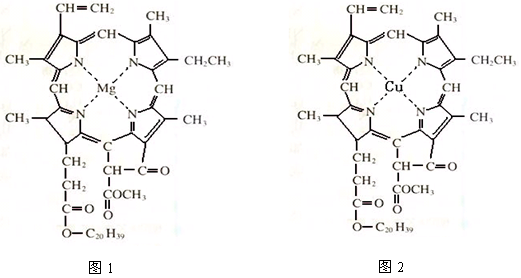
⑷在绿色植物标本的制作过程中,将植物材料洗净后浸入5%的硫酸铜溶液中,叶绿素(如图1)中心离子Mg2+被置换成Cu2+(如图2),叶片则永保绿色,请在图2中用箭头表示出配位键。

 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
 中σ键和π键的数目之比为__。
中σ键和π键的数目之比为__。




 。
。



