-
已知Na2CO3与稀盐酸反应分两步进行: +H+==
+H+== ,
, +H+= CO2↑+H2O。向10.00 mL 0.1000 mol·L-1Na2CO3溶液中滴加0.1000 mol·L-1盐酸,溶液pH随盐酸体积的变化如图。
+H+= CO2↑+H2O。向10.00 mL 0.1000 mol·L-1Na2CO3溶液中滴加0.1000 mol·L-1盐酸,溶液pH随盐酸体积的变化如图。
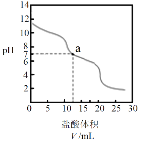
下列说法不正确的是
A.V = 5.00mL时,溶液中c( )>c(
)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.V =10.00mL时,溶液中c(Na+)=c( )+c(
)+c( )+c(H2CO3)+c(Cl-)
)+c(H2CO3)+c(Cl-)
C.a点的溶液中:n( )+n(
)+n( ) = 0.001 mol
) = 0.001 mol
D.V = 20.00mL时,溶液pH<7,是因为H2CO3 
 + H+
+ H+
-
某化学课外小组为测定空气中CO2的含量,进行了如下实验:
①配制0.1000 mol/L 和0.01000 mol/L的标准盐酸。
②将2~3滴酚酞加入未知浓度的Ba(OH)2溶液10.00 mL中,并用0.1000 mol/L的标准盐酸进行滴定,结果用去盐酸19.60 mL。
③用测定的Ba(OH)2溶液吸收定量空气中的CO2。取Ba(OH)2溶液10.00 mL,放入100 mL容量瓶里加水至刻度线,取出稀释后的溶液放入密闭容器内,并通入10 L标准状况下的空气,振荡,这时生成沉淀。
④过滤上述所得浊液。
⑤取滤液20.00 mL,用0.01000 mol/L的盐酸滴定,用去盐酸34.80 mL。
请回答下列问题:
(1)配制标准盐酸时,需用下列哪些仪器?_____________________。
A.托盘天平 B.容量瓶 C.酸式滴定管 D.量筒 E.烧杯 F.胶头滴管 G.玻璃棒
(2)②操作中到达滴定终点时的现象是___________________________________________。
(3)Ba(OH)2溶液的物质的量浓度是________。
(4)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即注入第二种标准盐酸,并进行第二次滴定,使测定结果________(填“偏大”“偏小”或“无影响”)。
(5)本实验中,若在第一次滴定的时候未润洗滴定管,会使测定结果_______(填“偏大”“偏小”或“无影响”)。
-
电解质溶液导电能力越强,电导率越大。常温下用0.1000 mol/L 盐酸分别滴定10.00 mL浓度均为0.1000 mol/L 的NaOH溶液和二甲胺[(CH3)2NH]溶液( 二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH·H2O]=1.6×10-4),利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是( )
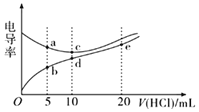
A.盐酸滴定二甲胺实验中选择酚酞做指示剂比选甲基橙误差更小
B.d点溶液中:c(H+)<c(OH-)+c[(CH3)2NH2+]
C.a 点溶液与d点的溶液混合后的溶液中:c[(CH3)2NH2+]<c[(CH3)2NH·H2O]
D.b、c、e三点的溶液中,水的电离程度最大的是e点
-
常温下,用0.1000mol·L-1HCl溶液滴定10.00mL浓度为0.1000 mol·L-1Na2CO3溶液,所得滴定曲线如图所示。已知H2CO3的Ka1=10-6.4,Ka2=10-10.2,下列说法不正确的是
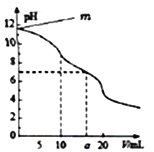
A. m=11.6
B. 当V=5 时,c(Na+)>c(CO32-) >c(HCO3-)>c(OH-)>c(H+)
C. 若用酚酞作指示剂,溶液由红色变为浅红色时,消耗盐酸体积约为10mL
D. 当V=a时c(Na+)>c(Cl-)>c(H+)=c(OH-)
-
25℃时,用0.10mol/L的氨水滴定10.00mL a mol/L的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。已知N点溶液中存在:c(H+)=c(0H-)+c(NH3•H2O),下列说法不正确的是
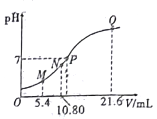
A. 图上四点离子种类相同
B. a=0.108
C. N、Q两点的 : N>Q
: N>Q
D. M点溶液中存在:c(H+)=c(OH-)+2(NH3•H2O) +c(NH4+)
-
常温下,用0.1000 mol/L盐酸滴定25 mL 0.1000 mol/L Na2CO3溶液,滴定曲线如图。关于滴定过程中所得溶液相关微粒的浓度关系,下列说法正确的是
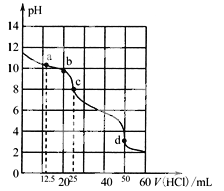
A.a点:c(CO32-)>c(HCO3-)>c(Cl-)
B.b点:5c(Cl-)>4c(HCO3-)+4c(CO32-)
C.c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.d点:c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
-
已知:25℃时,0.1mol·L-l CH3COOH的电离度(已电离的CH3COOH分子数/原CH3COOH分子总数)约为1%。该温度下,用0.1000mol·L-l 氨水滴定10.00 mL0.1000mol·L-l CH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法正确的是
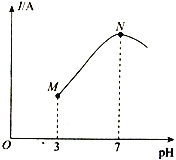
A. M点→N点,水的电离程度逐渐增大
B. 25℃时,CH3COOH 的电离常数约为1.0×10-2
C. N点溶液中,c(CH3COO-) =c(NH4+)=0.05 mol·L-l
D. 当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
-
已知:25℃时,0.1mol·L-l CH3COOH的电离度(已电离的CH3COOH分子数/原CH3COOH分子总数)约为1%。该温度下,用0.1000mol·L-l 氨水滴定10.00 mL0.1000mol·L-l CH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法正确的是
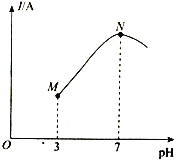
A. M点→N点,水的电离程度逐渐增大
B. 25℃时,CH3COOH 的电离常数约为1.0×10-2
C. N点溶液中,c(CH3COO-) =c(NH4+)=0.05 mol·L-l
D. 当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
-
已知:25℃时,0.1mol·L-l CH3COOH的电离度(已电离的CH3COOH分子数/原CH3COOH分子总数)约为1%。该温度下,用0.1000mol·L-l 氨水滴定10.00 mL0.1000mol·L-l CH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法正确的是
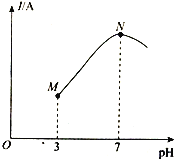
A. M点→N点,水的电离程度逐渐增大
B. 25℃时,CH3COOH 的电离常数约为1.0×10-2
C. N点溶液中,c(CH3COO-) =c(NH4+)=0.05 mol·L-l
D. 当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
-
在常温下,0.1000 mol/L Na2CO3溶液25 mL用0.1000 mol/L盐酸滴定,其滴定曲线如图。
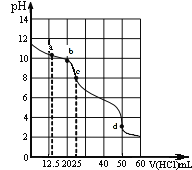
对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是
A.a点:c(CO32-)>c(HCO3-)>c(OH-)
B.b点:5c(Cl-)>4c(HCO3-)+4c(CO32-)
C.c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.d点:c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
+H+==
,
+H+= CO2↑+H2O。向10.00 mL 0.1000 mol·L-1Na2CO3溶液中滴加0.1000 mol·L-1盐酸,溶液pH随盐酸体积的变化如图。

)>c(
)>c(OH-)>c(H+)
)+c(
)+c(H2CO3)+c(Cl-)
)+n(
) = 0.001 mol
+ H+







