-
锌在电池制造方面有着重要的作用,也是人体必需的微量元素之一。它与常见的非金属都可以形成重要的化合物。
(1)Zn的核外电子排布式是[Ar]___。
(2)Zn的各级电离能数据如下表所示:

①请依据表中数据说明锌的常见化合价为+2的原因是___。
②氧、硫、氯三种常见非金属的电负性,由大到小的顺序是___。二氯化硫为鲜红色液体,熔点-78℃,则其晶体中微粒间的作用力应属于___,它的分子中中心原子具有的孤电子对数是___。
(3)氯化锌易溶于水,在水中形成配合物H[ZnCl2(OH)],H[ZnCl2(OH)]在水中电离时的离子方程式为___。
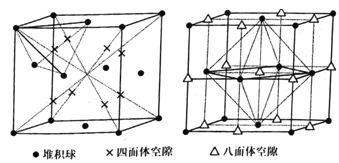
(4)晶胞的空隙问题是晶胞研究的重要内容。
①已知面心立方晶胞的四面体空隙和八面体空隙状况如图所示。面心立方晶胞的每个晶胞中,堆积球数:四面体空隙数:八面体空隙数=___。
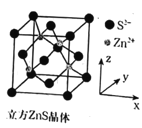
②根据立方ZnS晶胞示意图,描述在每个晶胞中,锌离子填充在硫离子的立方面心晶胞空隙中的方式为___。离坐标参数为(0,0,0)的硫离子最近的锌离子坐标参数为___ (参数数值限定为正值)。
-
钼(Mo)是人体及动植物必需的微量元素,且在芯片制作、药物和医学造影等方面也有重要作用。用辉钼矿冶炼金属钼的某反应:MoS2(s)+2Na2CO3(s)+4H2(g) Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),该反应中氢气的平衡转化率与温度、压强的关系如图所示:
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),该反应中氢气的平衡转化率与温度、压强的关系如图所示:

(1)Na2S的电子式为:____________。上述反应的气态反应物和生成物中属于极性分子的是____________(填写化学式)。举出一个事实,说明硫的非金属性比碳强(用化学方程式表示)____________。
(2)写出上述反应的平衡常数表达式K=____________。上述正反应是____________反应(填“吸热”或“放热”)。
(3)1100℃,2L恒容密闭容器中,加入0.1molMoS2、0.2molNa2CO3、0.4molH2,反应至20min时达到的平衡状态恰好处于上图中的A点。此过程中,用H2表示的平均速率为____________。其他条件一定时,B点的速率____________C点(填“大于”“等于”或“小于”),说明理由:____________。
(4)A、B、C三点代表的平衡状态的平衡常数的大小为:KA____________KB____________KC(填“大于”“等于”或“小于”),并说明理由:____________。
-
常见的非金属元素及化合物的特征性质有着重要的应用,请按要求回答:
(1)C、N、O、Si、S、Cl等元素形成的单质中
①属于空气主要成分它们相互反应的化学方程式_____________________;
②常用于自来水消毒的是实验室制备该气体的化学方程式_____________________。
(2)在CO、CO2、SO2、NO、NO2、SiO2等氧化物中:
①其中属于酸性氧化物的是______________,能形成酸雨的是_____________。
②光导纤维的主要成分与烧碱反应的化学方程式为___________________。
(3)在浓(稀)硝酸、浓(稀)硫酸中:
①常温下能使Fe、Al钝化的是_________。
②见光易分解的反应的化学方程式是:_____________________。
(4)在H2O2、NH3、HCl中:
①被称作绿色氧化剂,它与FeSO4酸性溶液反应的离子方程式为_______________________。
②可用于制氮肥、纯碱,加热条件下与氧气反应的化学方程式为_________________。
-
钼(Mo)是一种重要的过渡金属元素,常见化合价为+6、+5、+4,金属钼广泛用于冶金、机械制造、电子、照明及一些高科技领域。钼酸钠(Na2MoO4)是一种无公害型冷却水系统的金属缓蚀剂,也可用于制造生物碱、油墨、化肥、钼红颜料等。如图是化工生产中制备金属钼和钼酸钠的主要流程图,已知钼精矿的主要成分为MoS2,钼酸难溶于水。
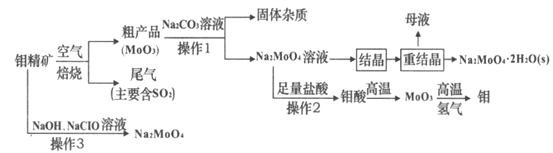
(1)MoS2焙烧时反应的化学方程式为________;产生的尾气对环境的主要危害是_______。
(2)操作1中,粗产品中的MoO3与Na2CO3溶液充分反应后,生成Na2MoO4和另外一种物质,该物质的电子式为_____。粗产品经过充分碱浸后所得的碱浸液中部分离子的浓度:c(MoO42-)=0.40mol·L-1,c(SO42-)=0.05mol·L-1。结晶前应先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4,开始沉淀时,SO42-的去除率为___。已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8
(3)该流程中操作2为过滤,如果在实验室模拟该操作时,发现滤液中有少量浑浊,从实验操作的角度分析,可能的原因是_______________________________。
(4)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因______________________________________。
(5)工业上由MoO3制备Mo粉也常用铝热反应,写出该反应的方程式_______________。
(6)操作3在碱性条件下,将钼精矿加入到足量的NaC1O溶液中,也可以制备钼酸钠。该反应的离子方程式为___________________________________。
-
微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也有着广泛的应用。
(1)基态B原子的价电子排布图为_____________________,其第一电离能比Be__________(填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。配离子[BH4]-的中心原子的杂化方式为________,写出与其互为等电子体的一种阳离子和一种分子的化学式:_________________。
(3)三氯化硼的沸点为12.5℃,而氯化镁的沸点高于1200℃,原因是____________________________________。
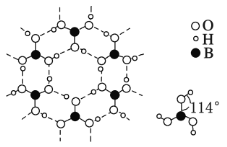
(4)硼酸晶体是片状结构,下图表示的是其中一层的结构。每一层内存在的作用力有______________;硼酸晶体在冷水中溶解度很小,但在热水中较大,原因是 _____________________________________________。
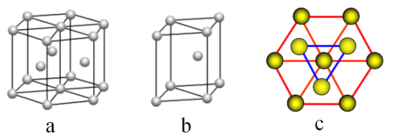
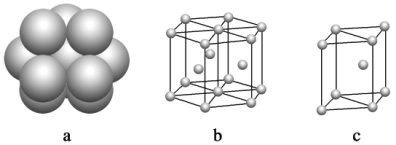
(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为__________________;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伽德罗常数为NA,则镁的摩尔质量计算式为________________。
-
锌是人体必需的微量元素,在体内有着重要的功能,然而过度的Zn2+会引起毒性,因此能够高效、灵敏检测Zn2+的方法非常重要。化合物L对Zn2+有高识别能力和良好的抗干扰性,其合成路线可设计如下:
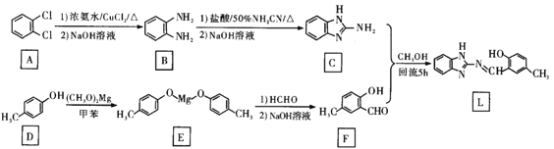
回答下列问题:
(1)A的化学名称为____________F的官能团名称为____________。
(2)D生成E的化学方程式为________________,该反应类型为____________。
(3)已知R-N=N-R分子中的N原子存在孤对电子(未共用电子对),且N = N双键不能旋转,因而存在顺反异构: (顺式),
(顺式), (反式)。判断化合物L是否存在顺反异构________(填“是”或“否”)。
(反式)。判断化合物L是否存在顺反异构________(填“是”或“否”)。
(4)研究人员利用某种仪器进行分析,发现化合物L中亚氨基(-NH-)及-OH上的氢原子的.吸收峰在结合Zn2+后的谱图中消失,该仪器的名称是___________仪;研究人员推测化合物L结合Zn2+的机理为: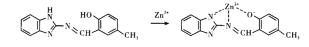 其中,Zn2+与-N=之间共价键的成键方式是________(填标号)。
其中,Zn2+与-N=之间共价键的成键方式是________(填标号)。
a. Zn2+和N原子各自提供单电子组成共用电子对
b. Zn2+单方面提供电子对与N原子共用
c. N原子单方面提供电子对与Zn2+共用
(5)X为F的芳香族同分异构体,写出满足如下条件的X的结构简式_____________。
①能发生水解反应和银镜反应,产物之一能与FeCl3溶液发生显色反应;
②有六种不同化学环境的氢,个数比为3:1:1:1:1:1。
(6)已知:通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。化合物Y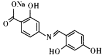 具有抑菌活性,以
具有抑菌活性,以 和
和 为原料制备Y,写出合成路线(有机溶剂和无机试剂任选)。____________。
为原料制备Y,写出合成路线(有机溶剂和无机试剂任选)。____________。
-
微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)基态B原子的电子排布图为________________________,其第一电离能比Be___________(填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为___________ (标出配位键),其中心原子的杂化方式为________,写出[BH4]-的一种阳离子等电子体_______。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________(以n表示硼原子的个数)。
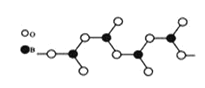
(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有_________。
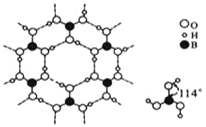
(5)三氯化硼的熔点比氯化镁的熔点低,原因是_______________________。
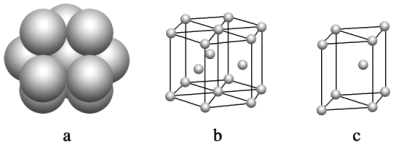
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为_______;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伽德罗常数为NA,则镁的摩尔质量的计算式是________________。
-
微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)基态B原子的电子排布图为________________________,其第一电离能比Be___________(填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为___________ (标出配位键),其中心原子的杂化方式为________,写出[BH4]-的一种阳离子等电子体_______。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________(以n表示硼原子的个数)。
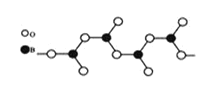
(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有_________。
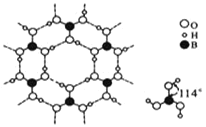
(5)三氯化硼的熔点比氯化镁的熔点低,原因是_______________________。
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为_______;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伽德罗常数为NA,则镁的摩尔质量的计算式是________________。
-
硼元素对植物生长及人体健康有着十分重要的作用,硼的化合物被广泛应用于新材料制备、生活生产等诸多领域。
(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为________、________(填标号)
A.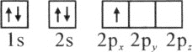
B.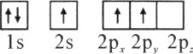
C.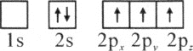
D.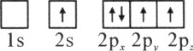
(2)晶体硼单质能自发呈现出正二十面体的多面体外形,这种性质称为晶体的________。
(3)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
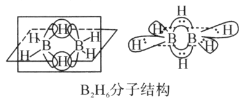
①B2H6分子结构如图,则B原子的杂化方式为________。
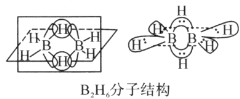
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
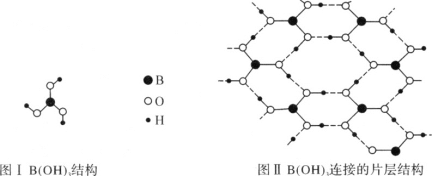
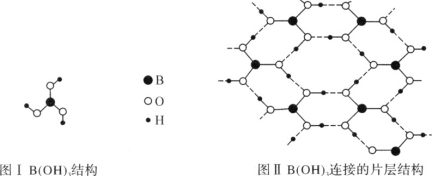
①H3BO3晶体中单元结构如图Ⅰ所示。各单元中的氧原子通过________氢键(用“A—B…C”表示,A、B、C表示原子)连结成层状结构,其片层结构如图Ⅱ所示,层与层之间以________(填作用力名称)相结合构成整个硼酸晶体。
②硼氢化钠中 的键角大小是________,立体构型为________。
的键角大小是________,立体构型为________。
③根据上述结构判断下列说法正确的是________
a.H3BO3分子的稳定性与氢键有关
b.硼酸晶体有滑腻感,可作润滑剂
c.H3BO3分子中硼原子最外层为8e-稳定结构
d.含1mol H3BO3的晶体中有3 mol氢键
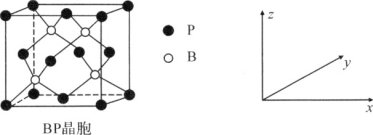
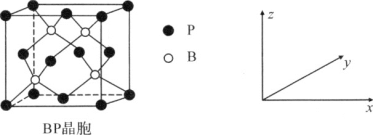
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是________;已知晶胞边长为a pm,则磷化硼晶体的密度是________g·cm-3(列出含a、NA的计算式即可)。
-
硼元素对植物生长及人体健康有着十分重要的作用,硼的化合物被广泛应用于新材料制备、生活生产等诸多领域。
(1)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为________、________(填标号)
A.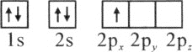
B.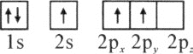
C.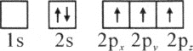
D.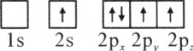
(2)晶体硼单质能自发呈现出正二十面体的多面体外形,这种性质称为晶体的________。
(3)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为________。
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。
①H3BO3晶体中单元结构如图Ⅰ所示。各单元中的氧原子通过________氢键(用“A—B…C”表示,A、B、C表示原子)连结成层状结构,其片层结构如图Ⅱ所示,层与层之间以________(填作用力名称)相结合构成整个硼酸晶体。
②硼氢化钠中 的键角大小是________,立体构型为________。
的键角大小是________,立体构型为________。
③根据上述结构判断下列说法正确的是________
a.H3BO3分子的稳定性与氢键有关
b.硼酸晶体有滑腻感,可作润滑剂
c.H3BO3分子中硼原子最外层为8e-稳定结构
d.含1mol H3BO3的晶体中有3 mol氢键
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是________;已知晶胞边长为a pm,则磷化硼晶体的密度是________g·cm-3(列出含a、NA的计算式即可)。








 其中,Zn2+与-N=之间共价键的成键方式是________(填标号)。
其中,Zn2+与-N=之间共价键的成键方式是________(填标号)。 具有抑菌活性,以
具有抑菌活性,以


















