-
根据要求写出下面的离子化学方程式:
(1)铜与稀硝酸反应的离子方程式为___________;
(2)实验室在保存含有Fe2+离子的溶液时,为了防止Fe2+离子变质,经常向其中加入铁粉,其原因是(用离子方程式表示)_____________
(3)铜与浓硫酸反应的离子方程式为______________;
(4)氢氧化钠不能用玻璃塞的原因用(用离子方程式表示)__________;
(5)二氧化硅与碳反应的化学方程式___________;
高一化学填空题简单题查看答案及解析
-
按要求填空:
(1)Fe2(SO4)3(写出电离方程式) .
(2)向稀硫酸溶液中滴加氢氧化钡溶液至中性(写出离子方程式) .
(3)写出实验室制取二氧化碳反应的离子方程式) .
(4)鉴别KCl溶液和K2CO3溶液的试剂是 (填名称),离子方程式为 .
(5)除去Na2CO3粉末中混入的NaHCO3杂质用 方法,化学方程式为 .
高一化学填空题简单题查看答案及解析
-
(6分)根据题目要求书写化学用语
(1)写出符合SO42—+ Ba2+= BaSO4↓的化学方程式
(2)写出实验室制二氧化碳的离子方程式
(3)氯水滴入硝酸银溶液的化学方程式
高一化学填空题简单题查看答案及解析
-
某待测液中可能含有Fe2+、Fe3+、Ag+、A13+、Ba2+、Ca2+、NH4+、Na+等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的)。

根据实验结果:
(1)写出沉淀D和E的化学式: D______,E__________;
(2)判断待测液中有无Ba2+、Ca2+?___________________;沉淀B为何物?____________;
(3)若溴水参加了反应,此反应的离子方程式是________________。
高一化学推断题困难题查看答案及解析
-
某待测液中可能含有Fe2+、Fe3+、Ag+、A13+、Ba2+、Ca2+、NH4+、Na+等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的)。
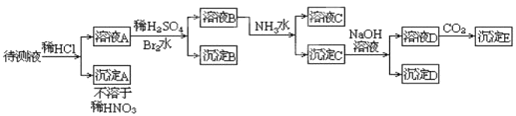
根据实验结果:
(1)写出沉淀D和E的化学式: D______,E__________;
(2)判断待测液中有无Ba2+、Ca2+?___________________;沉淀B为何物?____________;
(3)若溴水参加了反应,此反应的离子方程式是________________。
高一化学推断题困难题查看答案及解析
-
元素化合物知识是高中化学的重点内容,请你用学习到的元素化合物知识回答下列问题:
(1)浓硝酸见光易分解,实验室保存硝酸的方法是_____________。
(2)铜与稀HNO3反应产生NO的离子方程式为_______________,参与反应的硝酸中,表现酸性与氧化性的硝酸物质的量之比为_______。铜粉放入稀硫酸溶液中,无明显变化,但加入某盐一段时间后,发现铜粉质量减少,则该盐不可能是______。(填序号)
A.K2SO4 B.FeCl3 C.KNO3 D.Cu(NO3)2
(3)小苏打和Al(OH)3均可以治疗胃酸过多,小苏打治疗胃酸时发生的离子方程式为:_________________;Al(OH)3具有两性,也能溶解在NaOH溶液中,则反应的离子方程式为______________________________________;AlCl3溶液与过量氨水反应制备Al(OH)3的离子方程式为_____________________________________________。
高一化学填空题中等难度题查看答案及解析
-
【加试题】硝酸铝[Al(NO3)3]是一种常用媒染剂。工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3·9H2O]的流程如下:

(1)写出反应Ⅰ的离子方程式: (任写一个)。
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是 ,可采取的措施为 。
(3)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是 。
(4)若用右图所示实验装置制取Al(NO3)3,通入水蒸气的作用是 。
高一化学实验题中等难度题查看答案及解析
-
(11分)某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:
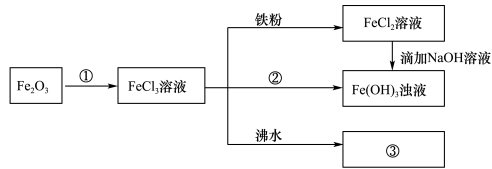
(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_________,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
高一化学填空题中等难度题查看答案及解析
-
写出下列反应的化学方程式或离子方程式:
(1)实验室制取Al(OH)3(离子方程式)______;
(2)保存碱性溶液不可用磨口玻璃瓶塞(离子方程式)______;
(3)盐酸除去铁锈的主要反应(离子方程式)______;
(4)氢氧化亚铁在空气中放置一段时间后会被氧化为氢氧化铁(化学方程式)______.
(5)Na2O2用于呼吸面具的主要原因(化学方程式)______.高一化学解答题中等难度题查看答案及解析
-
某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
高一化学填空题中等难度题查看答案及解析