-
某实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素。设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
(1)通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
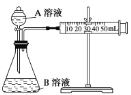
| 序号 | A溶液 | B溶液 |
| ① | 2mL0.1mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
| ② | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
| ③ | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液和少量MnSO4 |
该实验探究的是___对化学反应速率的影响。在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是___(用实验序号填空)。
(2)某组同学利用如图完成该实验。请分析导管a的两点作用:①___;②___。
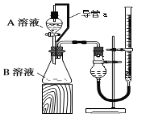
-
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素。
(1)该反应的离子方程式为__________________________。
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
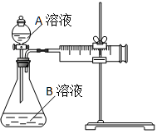
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
| 序号 | A溶液 | B溶液 |
| ① | 2 mL 0.1 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ② | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ③ | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液和少量MnSO4 |
该实验探究的是______对化学反应速率的影响。在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是____________(用实验序号填空)。
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小。取两支试管各加入2 mL 0.1 mol/L H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol/L KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验目的是研究_________对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是____________。
-
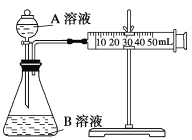
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
| ② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

① ;② 。
-
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
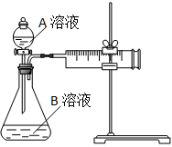
| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
| ② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
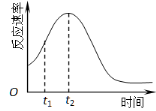 (5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
① ;② 。
-
Ⅰ.某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
| 实验 编号 | 0.01 mol·L-1酸性KMnO4溶液 | 0.1 mol·L-1 H2C2O4溶液 | 水 | 反应温度/℃ | 反应时间/s |
| ① | 5.0mL | 5.0mL | 0 | 20 | 125 |
| ② | V1 | V2 | 2.0mL | 20 | 320 |
| ③ | 5.0mL | 5.0mL | 0 | 50 | 30 |
反应方程式为:2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑+ 8H2O
(1)实验的记时方法是从溶液混合开始记时,至_________________时,记时结束。
(2)实验①和②研究浓度对反应速率的影响,则V1=______mL , V2=_______mL。
(3)下列有关该实验的叙述正确的是_________。
A.实验时必须用移液管或滴定管来量取液体的体积
B.实验时应将5.0 mLKMnO4溶液与5.0mL H2C2O4溶液混合后,立即按下秒表,再将盛有混合液的烧杯置于相应温度的水浴中至反应结束时,按下秒表,记录读数。
C.在同一温度下,最好采用平行多次实验,以确保实验数据的可靠性
D.实验①和③可研究温度对反应速率的影响
(4)某小组在进行每组实验时,均发现该反应是开始很慢,突然会加快,其可能的原因是__________;
Ⅱ. 某草酸晶体的化学式可表示为H2C2O4 • xH2O,为测定x的值,进行下列实验:
①称取7.56g某草酸晶体配成100.0mL的水溶液,
②用移液管移取25. 00mL所配溶液置于锥形瓶中,加入适量稀H2SO4,用浓度为0.600mol/L的KMnO4溶液滴定,滴定终点时消耗KMnO4 的体积为10.00mL。
(1)若滴定终点时仰视读数,则所测x的值将 _____(填“偏大”或“偏小”)。
(2)x=_________。
-
Ⅰ某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
| 实验 编号 | 0.01 mol·L-1酸性KMnO4溶液 | 0.1 mol·L-1 H2C2O4溶液 | 水 | 反应温度/℃ | 反应时间/s |
| ① | 5.0mL | 5.0mL | 0 | 20 | 125 |
| ② | V1 | V2 | 2.0mL | 20 | 320 |
| ③ | 5.0mL | 5.0mL | 0 | 50 | 30 |
反应方程式为:2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10CO2↑+ 8H2O
(1)实验的记时方法是从溶液混合开始记时,至 时,记时结束。
(2)实验①和②研究浓度对反应速率的影响,则V1= mL , V2= mL。
(3)下列有关该实验的叙述正确的是 。
A.实验时必须用移液管或滴定管来量取液体的体积
B.实验时应将5.0 mLKMnO4溶液与5.0mL H2C2O4溶液混合后,立即按下秒表,再将盛有混合液的烧杯置于相应温度的水浴中至反应结束时,按下秒表,记录读数。
C.在同一温度下,最好采用平行多次实验,以确保实验数据的可靠性
D.实验①和③可研究温度对反应速率的影响
(4)某小组在进行每组实验时,均发现该反应是开始很慢,突然会加快,其可能的原因是 ;
Ⅱ某草酸晶体的化学式可表示为H2C2O4 • xH2O,为测定x的值,进行下列实验:
①称取7.56g某草酸晶体配成100.0mL的水溶液,
②用移液管移取25. 00mL所配溶液置于锥形瓶中,加入适量稀H2SO4,用浓度为0.600mol/L的KMnO4溶液滴定,滴定终点时消耗KMnO4 的体积为10.00mL。
(1)移取所配溶液25.00 mL于锥形瓶中,操作如图所示(手持部分省略):正确的操作是图 。
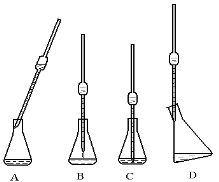
(2)x= 。
-
某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
| 实验 编号 | 0.01mol•L﹣1 酸性KMnO4溶液 | 0.1mol•L﹣1 H2C2O4溶液 | 水 | 1mol•L﹣1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
| Ⅰ | 2mL | 2mL | 0 | 0 | 20 | 125 |
| Ⅱ | V1 mL | V2 mL | 1mL | 0 | 20 | 320 |
| Ⅲ | V3 mL | V4 mL | V5 mL | 0 | 50 | 30 |
| Ⅳ | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
已知:反应的方程式(未配平):KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O
(1)实验记时方法是从溶液混合开始记时,至 时记时结束;
(2)实验I和Ⅱ研究浓度对反应速率的影响,实验Ⅰ和Ⅲ研究温度对反应速率的影响.则V1= V2= V3= V4= V5= ;
(3)从实验数据分析,实验I和IV研究 对反应的影响;
(4)请配平上面的化学方程式: KMnO4+ H2C2O4+ H2SO4= K2SO4+ MnSO4+ CO2↑+ H2O
-
(10分)某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
| 实验编号 | 0.01mol·L-1 酸性KMnO4溶液 | 0.1mol·L-1 H2C2O4溶液 | 水 | 1mol·L-1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
| I | 2mL | 2mL | 0 | 0 | 20 | 125 |
| II | ____mL | ____mL | 1mL | 0 | 20 | 320 |
| III | ____mL | __ _mL | ___mL | 0 | 50 | 30 |
| IV | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
已知:反应的方程式(未配平):KMnO4 + H2C2O4 + H2SO4 —— K2SO4 + MnSO4 + CO2↑+ H2O
(1)实验记时方法是从溶液混合开始记时,至___ ___ __时记时结束。
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响。请在上表空格中填入合理的实验数据。
(3)从实验数据分析,实验I和IV研究________对反应的影响。
(4)请配平上面的化学方程式:
KMnO4 + H2C2O4 + H2SO4= K2SO4 + MnSO4 + CO2↑+ H2O
-
(10分)某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
| 实验编号 | 0.01mol·L-1 酸性KMnO4溶液 | 0.1mol·L-1 H2C2O4溶液 | 水 | 1mol·L-1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
| I | 2mL | 2mL | 0 | 0 | 20 | 125 |
| II | ____mL | ____mL | 1mL | 0 | 20 | 320 |
| III | ____mL | __ _mL | ___mL | 0 | 50 | 30 |
| IV | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
已知:反应的方程式(未配平):KMnO4 + H2C2O4 + H2SO4 —— K2SO4 + MnSO4 + CO2↑+ H2O
(1)实验记时方法是从溶液混合开始记时,至___ ___ __时记时结束。
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响。请在上表空格中填入合理的实验数据。
(3)从实验数据分析,实验I和IV研究________对反应的影响。
(4)请配平上面的化学方程式:
KMnO4 + H2C2O4 + H2SO4= K2SO4 + MnSO4 + CO2↑+ H2O
-
某实验探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性KMnO4溶液的浓度可选择0.010mol·L1、0.001 mol·L1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性KMnO4溶液的用量均为4 mL,H2C2O4溶液(0.100mol·L1)、H2SO4溶液(0.100mol·L1)的用量均为2mL。
(1)写出该实验反应的离子方程式:______________________________________。
(2)请完成实验设计表,并在表中填出对应的实验设计内容:
| 实验编号 | T/K | 催化剂的用量/g | 酸性KMnO4溶液的浓度/(mol·L1) | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a. 实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b. 实验①和③探究___________对该反应速率的影响; c. 实验①和④探究催化剂对该反应速率的影响 |
| ② | 298 | 0.5 | 0.001 |
| ③ | 323 | 0.5 | 0.010 |
| ④ | _____ | ______ | ________ |
(3)该反应的催化剂应选择MnCl2还是MnSO4________________。简述选择的理由:____________________________________________________。
(4)某同学对实验①和②分别进行了三次重复实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验编号 | 溶液褪色所需时间t/min |
| 第1次 | 第2次 | 第3次 |
| ① | 12.8 | 13.0 | 11.0 |
| ② | 4.9 | 5.1 | 5.0 |
实验②中用KMnO4的浓度变化表示的平均反应速率为______________________(忽略混合前后溶液的体积变化,结果保留3位有效数字)。该同学分析上述数据后得出“当其他条件相同的情况下,酸性KMnO4溶液的浓度越小,所需要的时间就越短,即其反应速率越快”的结论,你认为是否正确____________(填“是”或“否”)。他认为不用经过计算,直接根据表中褪色所需时间的长短就可以判断浓度大小与反应速率的关系,你认为是否可行_____________(填“是”或“否”),若不可行(若认为可行则不填),请设计可以直接通过观察褪色所需时间的长短来判断的改进方案:_____________________________.




 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

 (5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是: