-
实验室以次氯酸盐和铁盐为原料制备少量K2FeO4的操作步骤如下:
Ⅰ.制备NaClO强碱性饱和溶液:
①将20 mL NaOH溶液加入仪器b中,冷水浴冷却,通入Cl2,搅拌,直至溶液变为黄绿色且有少量白色晶体析出为止(装置如下图所示)。

②将所得饱和NaClO倒入烧杯并置于冷水浴中,分几次加入20 g NaOH固体并不断搅拌,过滤,得NaClO强碱性饱和溶液。
(1)甲装置中a管的作用是_____________________________________________。
(2)写出甲装置中反应的化学方程式_____________________________________。
(3)石灰乳的作用是___________________________________________________。
(4)反应过程中用冷水浴冷却的原因是___________________________________。
Ⅱ.合成K2FeO4:
①称取5.05 g Fe(NO3)3·9H2O(相对分子质量为404)固体,在冷水浴中分批加入Ⅰ中所得滤液,并不断搅拌,反应1小时后溶液呈深紫红色(即Na2FeO4)。
②离心分离除去Na2FeO4水解得到的Fe(OH)3胶体,留上层清液(深紫红色)。
③向②的上层清液中缓慢加入KOH饱和溶液50.00mL,冰水浴保持5 min,过滤,得K2FeO4(相对分子质量为198)粗产品。
④将粗产品重结晶,并用异丙醇洗涤,低温烘干,得纯产品2.13 g。
(5)合成Na2FeO4的离子方程式为____________________________________。
(6)过程③加入饱和KOH溶液即可得到K2FeO4粗产品,原因是__________。
(7)用异丙醇洗涤的目的是__________________________________________。
(8)K2FeO4的产率为___________(保留至0.1%)。
-
高铁酸钾的确是一种新型、高效、多功能水处理剂,应用前景广阔.实验室以次氯酸盐和铁盐为原料制备少量高铁酸钾的操作步骤如下:
(1)制备次氯酸钾强碱性饱和溶液:①在100mL水中溶解56gKOH,冷至室温后倒入三口瓶中(装置见右图),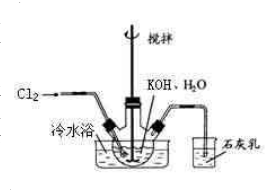 冷水浴冷却,通入Cl2,用电动搅拌器不断搅拌,直至溶液变为黄绿色且有少量白色晶体析出为止.②将饱和次氯酸钾倒入烧杯并置于冷水浴中.在不断搅拌下,分几次加入130gKOH固体.用玻璃砂芯漏斗过滤,弃去残渣(主要成分为KCl和少量KOH、KClO),得次氯酸钾强碱性饱和溶液.
冷水浴冷却,通入Cl2,用电动搅拌器不断搅拌,直至溶液变为黄绿色且有少量白色晶体析出为止.②将饱和次氯酸钾倒入烧杯并置于冷水浴中.在不断搅拌下,分几次加入130gKOH固体.用玻璃砂芯漏斗过滤,弃去残渣(主要成分为KCl和少量KOH、KClO),得次氯酸钾强碱性饱和溶液.
①石灰乳的作用是________.石灰乳参与反应的化学方程式________.
②反应过程中和保存饱和次氯酸钾中用冷水浴冷却的原因是________
________(以必要文字和方程式加以说明).
③在上述制备过程中不断搅拌原因是________(以必要文字加以说明).
(2)合成高铁酸钾:将次氯酸钾饱和溶液转入烧杯,冷水浴冷却,在剧烈搅拌下分次加入13.5g研细的FeCl3•6H2O,立即产生大量紫黑色K2FeO4.加少量稳定剂Na2SiO3•9H2O和CuCl2•2H2O,反应30min后,分次加入100gKOH固体,保持温度在20℃以下,陈化30min,用玻璃砂芯漏斗抽滤,得高铁酸钾粗品.
①写出合成高铁酸钾的离子方程式________.
②13.53gFeCl3•6H2O理论上可制得高铁酸钾________g.
(3)高铁酸钾的净水原理:①高铁酸钾在水中发生反应生成Fe(OH)3胶体.写出化学方程式________
________.②高铁酸钾作为水处理剂发挥的作用是________、________.
-
高纯 是制备高性能磁性材料的主要原料。实验室以
是制备高性能磁性材料的主要原料。实验室以 为原料制备少量高纯
为原料制备少量高纯 的操作步骤如下:
的操作步骤如下:
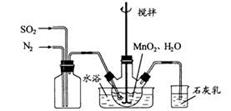 (1)制备
(1)制备 溶液:在烧瓶中(装置见右图)加入
溶液:在烧瓶中(装置见右图)加入
一定量 和水,搅拌,通入
和水,搅拌,通入 和
和 混合
混合
气体,反应3h。停止通入 ,继续反应片刻,
,继续反应片刻,
过滤(已知 )
)
①石灰乳参与反应的化学方程式为_____________。
②反应过程中,为使 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有__________________________、_________________。
比例一定、不改变固液投料的条件下,可采取的合理措施有__________________________、_________________。
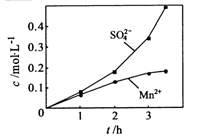 ③若实验中将
③若实验中将 换成空气,测得反应液中
换成空气,测得反应液中
 、
、 的浓度随反应时间t的浓度变化如右图。
的浓度随反应时间t的浓度变化如右图。
导致溶液中 、
、 浓度变化产生明显差异的
浓度变化产生明显差异的
原因是_____________。
(2)制备高纯 固体:已知
固体:已知 难溶于水、乙醇,潮湿时易被空气氧化,
难溶于水、乙醇,潮湿时易被空气氧化, 开始分解;
开始分解; 开始沉淀时
开始沉淀时 。请补充由(1)时制得的
。请补充由(1)时制得的 制备高纯
制备高纯 的操作步骤【实验中可选用的试剂:
的操作步骤【实验中可选用的试剂:  、
、 、
、  、
、 】。
】。
①________;②________;③________;④________;⑤低于 。
。
-
 (12分)高纯
(12分)高纯 是制备高性能磁性材料的主要原料。实验室以
是制备高性能磁性材料的主要原料。实验室以 为原料制备少量高纯
为原料制备少量高纯 的操作步骤如下:
的操作步骤如下:
(1)制备 溶液:
溶液:
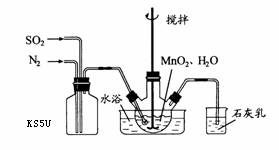
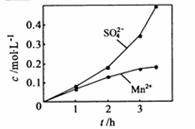 在烧瓶中(装置见右图)加入一定量
在烧瓶中(装置见右图)加入一定量 和水,搅拌,
和水,搅拌,
通入 和
和 混合气体,反应3h。停止通入
混合气体,反应3h。停止通入 ,
,
继续反应片刻,过滤(已知 )。
)。
①石灰乳参与反应的化学方程式为________。
②反应过程中,为使 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有________、________。
比例一定、不改变固液投料的条件下,可采取的合理措施有________、________。
③若实验中将 换成空气,测得反应液中
换成空气,测得反应液中 、
、 的浓度随反应时间t变化如右图。导致溶液中
的浓度随反应时间t变化如右图。导致溶液中 、
、 浓度变化产生明显差异的原因是________。
浓度变化产生明显差异的原因是________。
(2)制备高纯 固体:已知
固体:已知 难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;
难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解; 开始沉淀时
开始沉淀时 。请补充由(1)制得的
。请补充由(1)制得的 溶液制备高纯
溶液制备高纯 的操作步骤[实验中可选用的试剂:
的操作步骤[实验中可选用的试剂:  、
、 、
、  、
、 ]。
]。
①________;②________;③________;④________;⑤低于100℃干燥。
-
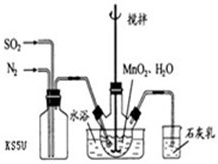
高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
在烧瓶中(装置见下图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+ H2SO3= MnSO4+H2O)。
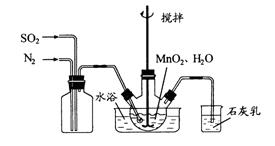
①石灰乳参与反应的化学方程式为 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 。
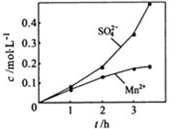
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如下图。
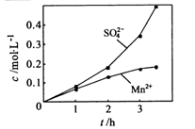
导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7。请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
①边搅拌边加入 ,并控制溶液pH ;
② ;
③检验SO42-是否被洗涤干净;(实验操作: )
④用少量C2H5OH洗涤;
⑤ 。
-
高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤.
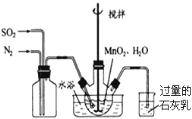
① 写出左边集气瓶的作用 。
② 石灰乳的作用是: (用化学方程式表示)
③ 写出MnO2和H2SO3反应的离子反应方程式 。
④反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 (选择选项填空)。
a.缓慢通入混合气体 b.快速通入混合气体c.控制适当的温度 d.高温加热
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化, 100℃开始分解;Mn(OH)2开始沉淀时pH=7.7。请补充由(1)制得的MnSO4制备高纯MnCO3的操作步骤【实验中可选用的试剂: Ca(OH)2、NaHCO3、Na2CO3、C2H5OH】。
100℃开始分解;Mn(OH)2开始沉淀时pH=7.7。请补充由(1)制得的MnSO4制备高纯MnCO3的操作步骤【实验中可选用的试剂: Ca(OH)2、NaHCO3、Na2CO3、C2H5OH】。
① 边搅拌边加入Na2CO3,并控制溶液pH<7.7;
② ;
③ 检验SO42-是否被洗涤干净。检验水洗是否合格的方法是 。
④ 用少量C2H5OH洗涤,其目的是 ;
⑤ 低于1 00℃干燥。
00℃干燥。
-
高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
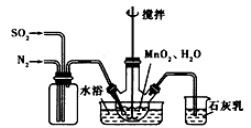
(1)制备MnSO4溶液:在烧瓶中(装置见上图)加入一定量MnO2和水,搅拌,通人SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤。
①写出反应方程式:MnO2+ H2SO3=_________________;
石灰乳参与反应的化学方程式为___________________。
②反应过程中,为使SO2尽可能转化完全,在通人SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有(填两种)________________、___________________。
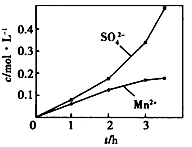
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如上图。导致溶液中Mn2+、SO42-的浓度变化产生明显差异,其中Mn2+对O2与H2SO3反应所起的作用是_________________。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH= 7.7。
请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2O 、Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
①边搅拌边加入_________________,并控制溶液pH_______7.7;
②_______________________;
③_______________________;
④_______________________;
⑤低于100℃干燥。
-
高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
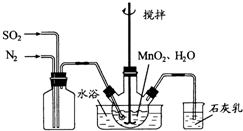
在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O).
①石灰乳参与反应的化学方程式为______.
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有______、______.
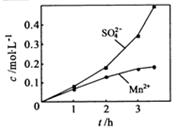
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是______.
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7.请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①______;②______;③______;④______;⑤低于100℃干燥.
-
Ⅰ高纯MnCO3是制备高性能磁性材料的主要原料.
实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:
在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O).
①石灰乳作用________.
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是________.
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH].
①________;②________;③检验SO42-是否被洗涤除去;④________;⑤低于100℃干燥.
Ⅱ锌铝合金的主要成分有Zn、Al、Cu、Si等元素.实验室测定其中Cu含量的步骤如下:
①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于
250mL容量瓶中.
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,
用0.01100mol⋅L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3溶液6.45mL.
(1)判断步骤②滴定终点的方法是________.
(2)计算合金中Cu的质量分数________.
-
高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下.

(1)制备MnSO4溶液:在烧瓶中(装置见图1)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入O2,继续反应片刻,过滤(已知MnO2+H2SO3═MnSO4+H2O).
①石灰乳参与反应的化学方程式为 .
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 .
③若实验中将N2换成空气,测得反应液中Mn2+、SO42﹣的浓度随反应时间t变化如图2导致溶液中Mn2+、SO42﹣浓度变化产生明显差异的原因是 .
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7.请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤
实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH.
①边搅拌边加入 ,并控制溶液pH ;
② ;
③检验SO42﹣是否被洗涤干净;(实验操作: )
④用少量C2H5OH洗涤;
⑤ .

 冷水浴冷却,通入Cl2,用电动搅拌器不断搅拌,直至溶液变为黄绿色且有少量白色晶体析出为止.②将饱和次氯酸钾倒入烧杯并置于冷水浴中.在不断搅拌下,分几次加入130gKOH固体.用玻璃砂芯漏斗过滤,弃去残渣(主要成分为KCl和少量KOH、KClO),得次氯酸钾强碱性饱和溶液.
冷水浴冷却,通入Cl2,用电动搅拌器不断搅拌,直至溶液变为黄绿色且有少量白色晶体析出为止.②将饱和次氯酸钾倒入烧杯并置于冷水浴中.在不断搅拌下,分几次加入130gKOH固体.用玻璃砂芯漏斗过滤,弃去残渣(主要成分为KCl和少量KOH、KClO),得次氯酸钾强碱性饱和溶液. (1)制备
(1)制备 ③若实验中将
③若实验中将 (12分)高纯
(12分)高纯 在烧瓶中(装置见右图)加入一定量
在烧瓶中(装置见右图)加入一定量








