-
LiFePO4电池具有能量密度大、绿色环保等优点,在可再生能源发电站发电安全并网等领域有着良好的应用前景。LiFePO4 电池结构如图所示,电池反应为:Li1-xFePO4+ LixC6  C6+ LiFePO4。
C6+ LiFePO4。
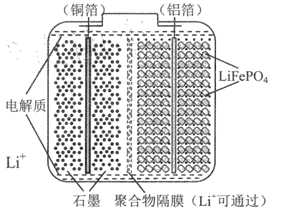
下列说法错误的是
A.充电时, Li+通过聚合物隔膜由左向右移动
B.充电时, 阳极反应为LiFePO4 -xe-=Li1-xFePO4+ xLi+
C.放电时, 负极反应为LixC6 -xe-= xLi++ C6
D.放电时,电子由左侧电极通过外电路移向右侧电极
-
锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
(1)高温固相法是磷酸铁锂生产的主要方法。通常以铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛的保护中先经过较低温预分解,再经高温焙烧,研磨粉碎制成。其反应原理如下:
Li2CO3+2FeC2O4•2H2O+2NH4H2PO4═2NH3↑+3CO2↑+______+_______+_______
①完成上述化学方程式.
②理论上,反应中每转移0.15mol电子,会生成LiFePO4______________g;
③反应需在惰性气氛的保护中进行,其原因是______________;
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
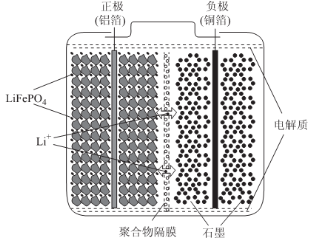
电池工作时的总反应为:LiFePO4+6C Li1-xFePO4+LixC6,则放电时,正极的电极反应式为______________。充电时,Li+迁移方向为______________(填“由左向右”或“由右向左”),图中聚合物隔膜应为______________(填“阳”或“阴”)离子交换膜。
Li1-xFePO4+LixC6,则放电时,正极的电极反应式为______________。充电时,Li+迁移方向为______________(填“由左向右”或“由右向左”),图中聚合物隔膜应为______________(填“阳”或“阴”)离子交换膜。
(3)用该电池电解精炼铜。若用放电的电流强度I=2.0A的电池工作10分钟,电解精炼铜得到铜0.32g,则电流利用效率为______________(保留小数点后一位)。(已知:法拉第常数F=96500C/mol,电流利用效率= 100%)
100%)
(4)废旧磷酸亚铁锂电池的正极材料中的LiFePO4难溶于水,可用H2SO4和H2O2的混合溶液浸取,发生反应的离子方程式为______________。
-
LiFePO4新型锂离子电池因其原材料丰富、对环境友好、循环性能和安全性能好的特点,具有广阔的应用前景。已知该电池放电时的电极反应式为:
正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+,下列说法中正确的是
A.充电时阳极反应为Li++e-=Li
B.充电时动力电池上标注“-”的电极应与外接电源的负极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
-
镁燃料电池作为一种高能化学电源,具有比能量高、使用安全方便、成本低、燃料易于贮运、污染小等特点,拥有良好的应用前景。如图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料。下列有关该镁燃料电池的叙述正确的是
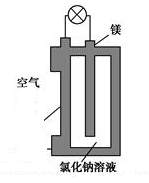
A. 该电池的总反应为2Mg+O2=2MgO
B. 反应生成O2-,该离子有正极移向负极
C. Cl-在阳极失去电子生成Cl2
D. 正极反应式为O2+2H2O+4e-=4OH-
-
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车备受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括( )
①原料来源广;②易燃烧、热值高;③储存方便;④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
-
新型锂-空气电池具有能量密度高的优点,可以用作新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过。下列说法不正确的是
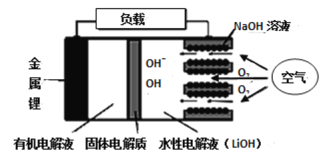
A. 放电时,负极反应式:Li-e- =Li+
B. 应用该电池电镀铜,阴极质量增加64 g,理论上将消耗标准状况下11.2 L O2
C. 放电时,随外电路中电子的转移,水性电解液中离子总数减少
D. Li+穿过固体电解质向正极移动而得到LiOH溶液
-
钼(Mo)及其合金在冶金、农业、电气、化工、环保和宇航等重要领域有着广泛的应用和良好的前景,成为国民经济中一种重要的原料和不可替代的战略物质。钼酸钠晶体(Na2MoO4 ·2H2O)是一种重要的金属缓蚀剂。某工厂利用钼精矿(主要成分 MoS2 )制备钼酸钠晶体和金属钼的流程如图所示:
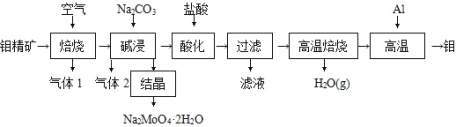
请回答下列问题:
(1)Na2 MoO 4·2H2O 中 Mo 的化合价是 ________。
(2)已知“焙烧”过程中 MoS2 变成 MoO3,则气体 1 中对大气有污染的是 ________。
(3)“碱浸”过程中生成 Na2MoO4 的化学方程式是 ________;“结晶”的钼酸钠晶体仍含其他杂质,要得到较纯的晶体,还应采取的方法是 ________。
(4)“滤液”的主要成分是 ________。
(5)将过滤操作得到的钼酸沉淀进行高温焙烧,实验室模拟高温焙烧时用于盛放钼酸的仪器是 ________。
(6)钼酸高温焙烧的产物与 Al 在高温下发生反应的化学方程式是 ________。
(7)测得碱浸液中部分离子浓度为:c(MoO42-) =0.4 mol·L-1,c(SO42-) =0.02 mol·L-1。结晶前加入氢氧化钡固体除去SO42-,不考虑加入氢氧化钡固体后溶液体积的变化,当BaMoO4开始沉淀时,SO42- 的去除率为 ________ (保留三位有效数字)。 [已知: Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8]
-
(14分) 二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等领域也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳。
Ⅰ.①氧化产物是 ________
②请写出化学反应方程式,并用双线桥法表示该反应的电子转移总数
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
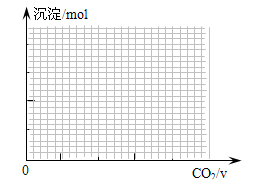
取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示
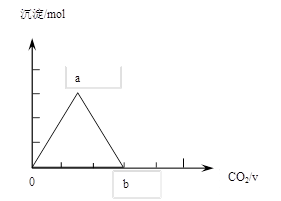
写出沉淀变化由a到b的离子方程式: ________
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;
并写出与上图中不同曲线处对应的离子反应方程式________;
________。
-
(14分) 二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等领域也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳。
Ⅰ.①氧化产物是 ________
②请写出化学反应方程式,并用双线桥法表示该反应的电子转移总数
________
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示
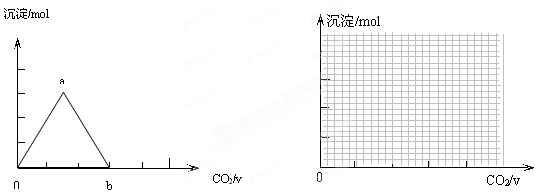
写出沉淀变化由a到b的离子方程式: ________
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;
并写出与上图中不同曲线处对应的离子反应方程式________;
________。
-
(18分) 二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳
Ⅰ.①氧化产物是 ________
②请写出化学反应方程式,并用单线桥法表示该反应的电子转移总数
________
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
①少量CO2通入过量的KOH溶液中,请写出离子反应方程式
________
②取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示


写出沉淀变化由a到b的离子方程式:________
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;并写出与图②中不同曲线处对应的离子反应方程式
________
C6+ LiFePO4。









