-
工业上常用还原沉淀法处理含铬废水( 和
和 ),其流程为:
),其流程为:
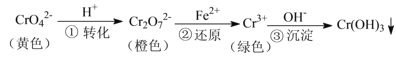
已知:步骤③生成的 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:
 ,
,
下列有关说法不正确的是
A.步骤①中当 时,说明反应:
时,说明反应: 达到平衡状态
达到平衡状态
B.若向 溶液中加NaOH浓溶液,溶液可由橙色变黄色
溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原 离子,需要
离子,需要
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽 当溶液中
当溶液中 时,可视作该离子沉淀完全
时,可视作该离子沉淀完全
-
工业上常用还原沉淀法处理含铬废水( 和
和 ),其流程为:
),其流程为:
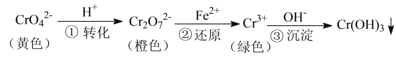
已知:步骤③生成的 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:
 ,
,
下列有关说法不正确的是
A.步骤①中当 时,说明反应:
时,说明反应: 达到平衡状态
达到平衡状态
B.若向 溶液中加NaOH浓溶液,溶液可由橙色变黄色
溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原 离子,需要
离子,需要
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽 当溶液中
当溶液中 时,可视作该离子沉淀完全
时,可视作该离子沉淀完全
-
工业上常用还原沉淀法处理含铬废水( 和
和 ),其流程为:
),其流程为:
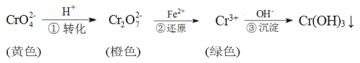
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)Ksp=c(Cr3+)·c3(OH-)=10-32
下列有关说法正确的是( )
A.步骤①中当2v正( )=v逆(
)=v逆( )时,说明反应:2
)时,说明反应:2 +2H+⇌
+2H+⇌ +H2O达到平衡状态
+H2O达到平衡状态
B. 在酸性溶液中不能大量存在
在酸性溶液中不能大量存在
C.步骤②中,若要还原1mol 离子,需要12mol(NH4)2Fe(SO4)2
离子,需要12mol(NH4)2Fe(SO4)2
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+)≤10-5 mol/L时,可视作该离子沉淀完全)
-
工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
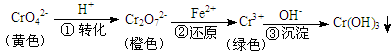
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
下列有关说法不正确的是
A.步骤①中当v正(CrO42—) = 2v逆(Cr2O72—)时,说明反应:2CrO42—+2H+ Cr2O72—+H2O 达到平衡状态
Cr2O72—+H2O 达到平衡状态
B.若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原1 mol Cr2O72—离子,需要12 mol (NH4)2Fe(SO4)2
D.步骤③中,当将溶液的pH 调节至5 时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+) ≤10-5 mol/L时,可视作该离子沉淀完全)
-
工业上常用还原沉淀法处理含铬废水(Cr2O72-和CrO42-),其流程为
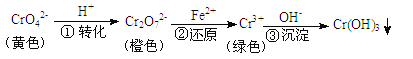
步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)∙c3(OH-)=10-32,下列有关说法正确的是
Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)∙c3(OH-)=10-32,下列有关说法正确的是
A.步骤①中当v(CrO42-)=2v(Cr2O72-)时,说明反应:2CrO42-+2H+  Cr2O72- +H2O达到平衡状态
Cr2O72- +H2O达到平衡状态
B.若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由黄色变橙色
C.步骤②中,若要还原1 mol Cr2O72- 离子,需要12 mol的Fe2+
D.步骤③中,当将溶液的pH 调节至5 时,可认为废水中的铬元素已基本除尽
-
工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
已知: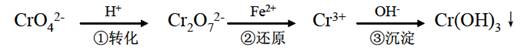
(1)步骤①中存在平衡:2Cr O42—(黄色)+2H+ Cr2O42—(橙色)+H2O
Cr2O42—(橙色)+H2O
(2)步骤③生成的Cr(OH)3 在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH 一(aq)
Cr3+(aq)+3OH 一(aq)
(3)常温下,Cr(OH)3 的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1 时可视作该离子不存在下列有关说法中,正确的是:( )
A.步骤①中加酸,将溶液的pH 调节至2,溶液显黄色,CrO42—离子浓度增大
B.步骤①中当2v(CrO42 一)=v(Cr2O72—)时,说明反应2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O 达到平衡状态
Cr2O72—(橙色)+H2O 达到平衡状态
C.步骤②中,若要还原1 mol Cr2O72一离子,需要12 mol(NH4)2Fe(SO4)2·6H2O。
D.步骤③中,当将溶液的pH 调节至6 时,则可认为废水中的铬已除尽
-
工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
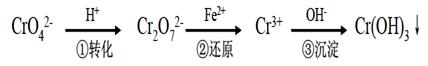
已知:(1)步骤①中存在平衡:2Cr O42—(黄色)+2H+ Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH 一(aq)
Cr3+(aq)+3OH 一(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在下列有关说法中,正确的是( )
A.步骤①中加酸,将溶液的pH 调节至2,溶液显黄色,CrO42—离子浓度增大
B.步骤①中当2v(CrO42 一)=v(Cr2O72—)时,说明反应2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O 达到平衡状态
Cr2O72—(橙色)+H2O 达到平衡状态
C.步骤②中,若要还原1 mol Cr2O72一离子,需要12 mol(NH4)2Fe(SO4)2·6H2O。
D.步骤③中,当将溶液的pH 调节至6 时,则可认为废水中的铬已除尽
-
工业上常用还原沉淀法处理含铬废水(Cr2 和Cr
和Cr ),其流程为:Cr
),其流程为:Cr
 Cr2
Cr2
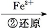 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr (黄色)+2H+
(黄色)+2H+ Cr2
Cr2 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是( )
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr 浓度增大
浓度增大
B.步骤①中当2v(Cr )=v(Cr2
)=v(Cr2 )时,说明反应2Cr
)时,说明反应2Cr (黄色)+2H+
(黄色)+2H+ Cr2
Cr2 (橙色)+H2O达到平衡状态
(橙色)+H2O达到平衡状态
C.步骤②中,若要还原1 mol Cr2 ,需要12 mol (NH4)2Fe(SO4)2·6H2O
,需要12 mol (NH4)2Fe(SO4)2·6H2O
D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽
-
铬及其化合物在工业上有着广泛的用途,但在生产和使用过程中易产生有毒害的含铬工业废水。
I.处理含铬工业废水的常用方法是还原沉淀法,该方法的工艺流程如下:
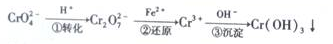
(l)上述流程的步骤①中存在如下平衡:2CrO42-(黄色)+2H+ Cr2072一(橙色)+H20。若平衡体系的pH =0时,溶液的颜色为_________色。
Cr2072一(橙色)+H20。若平衡体系的pH =0时,溶液的颜色为_________色。
(2)第②步反应的离子方程式为 ,步骤③可通过调节第二步反应后溶液的pH使Cr3+沉淀完全,请通过计算判断当pH >6时,溶液中Cr3+是否沉淀完全:。(简要写出计算过程。已知常温下,Cr( OH)3的溶度积Ksp=6.0 x10一31,且当溶液中离子浓度小于10 -5mol.L-l时可视作该离子不存在。)
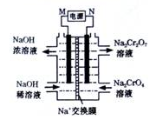
(3)以石墨为电极电解Na2CrO4溶液制取Na2Cr207,电解装置如下图所示。直流电源M极的电极名称是_________,和N相连的一极的电极反应式为_____________。
Ⅱ.Cr03俗称铬酸酐,常用于制备铬的化合物。Cr03具有强氧化性,热稳定性较差。
(4)Cr03具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火。在硫酸酸化时Cr03可将乙醇氧化成乙酸,而Cr03被还原成绿色的硫酸铬[Cr2(S04)3]。则该反应的化学方程式为 。
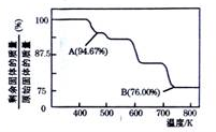
(5)Cr03的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如右图所示。请根据图示信息写出从开始加热到750K时总反应的化学方程式____ 。
-
工业上常用还原沉淀法处理含铬废水(Cr2 和Cr
和Cr ),其流为:
),其流为:
Cr
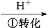 Cr2
Cr2
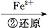 Cr3+
Cr3+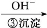 Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr (黄色)+2H+
(黄色)+2H+ Cr2
Cr2 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)  Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr 浓度增大
浓度增大
B.步骤①中当2v(Cr )=v(Cr2
)=v(Cr2 )时,说明反应2Cr
)时,说明反应2Cr (黄色)+2H+
(黄色)+2H+  Cr2
Cr2 (橙色)+H2O达到平衡状态
(橙色)+H2O达到平衡状态
C.步骤②中,若要还原1 mol Cr2 ,需要12 mol (NH4)2Fe(SO4)2·6H2O
,需要12 mol (NH4)2Fe(SO4)2·6H2O
D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽
和
),其流程为:

)=v逆(
)时,说明反应:2
+2H+⇌
+H2O达到平衡状态
在酸性溶液中不能大量存在
离子,需要12mol(NH4)2Fe(SO4)2
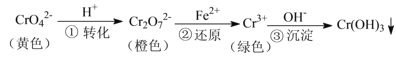
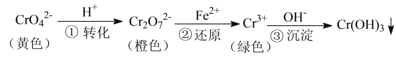
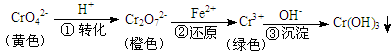

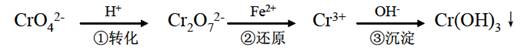

 Cr2
Cr2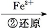 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓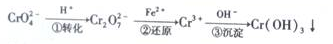


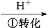 Cr2
Cr2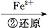 Cr3+
Cr3+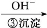 Cr(OH)3↓
Cr(OH)3↓