-
碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11,草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5,将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是
A. c(H+)>c(HC2O4-)>c(HCO3-)>c(C2O42-)
B. c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C. c(H+)>c(HC2O4-)>c(C2O42-)>c(HCO3-)
D. c(H2CO3)>c(HCO3-)>c(HC2O4-)>c(CO32-)
-
(1)已知碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11,草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
①0.1mol·L-1Na2CO3溶液的pH____0.1mol·L-1Na2C2O4溶液的pH。(填“大于”“小于”或“等于”)
②碳酸钠溶液显碱性的原因是_____________________________ 。(用主要的离子方程式表示)
③若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种粒子浓度大小的顺序正确的是______(填字母)。
a.c(H+)>c(HC2O4-)>c(HCO3-)>c(CO32-)
b.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
c.c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-)
d.c(H2CO3)>c(HCO3-)>c(HC2O4-)>c(CO32-)
(2)用氨水除去SO2。
已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol·L-1,溶液中的c(OH-)=________mol·L-1。将SO2通入该氨水中,当c(OH-)降至1.0×10-7mol·L-1时,溶液中的c(SO32-)/c(HSO3-)=__________。
-
(1)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11;草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1 mol/L Na2CO3 溶液的 pH________0.1 mol/L Na2C2O4 溶液的pH。(选填“大于”“小于”或“等于”)
等浓度草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
(2)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的 pH 变化不大,用平衡移动原理解释上述现象_________________________。
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的 pH 变化不大,用平衡移动原理解释上述现象_________________________。
(3)请写出Na2CO3溶液中的微粒之间的关系式:
电荷守恒______________________,
质子守恒_______________________。
(4)已知 Ag2 CrO4、AgCl 的 Ksp 分别为 2.0×10-12和 2.0×10-10。在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与 CrO42-生成砖红色沉淀,指示到达滴定终点。当溶液中 Cl-恰好完全沉淀(浓度等于1.0×10-5 mol·L-1)时,溶液中 c(Ag+)为____________mol·L-1,此时溶液中 c(CrO42-)等于__________mol·L-1。
-
碳酸:H2CO3,K1=4.3×10-7,K2=5.6×10-11、草酸:H2C2O4,K1=5.9×10-2,K2=6.4×10-5
0.1mol/L Na2CO3溶液的pH________0.1mol/L Na2C2O4溶液的pH;(选填“大于”“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是________;若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是________(选填编号);
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]
b.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]
d.[H2CO3]>[HCO3-]>[HC2O4-]>[CO32-]
-
碳酸:H2CO3,K1=4.3×10-7,K2=5.6×10-11
草酸:H2C2O4,K1=5.9×10-2,K2=6.4×10-5
0.1mol/L Na2CO3溶液的pH__________0.1mol/L Na2C2O4溶液的pH;(选填“大于”“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是________;若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是________(选填编号);
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]
b.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]
d.[H2CO3]>[HCO3-]>[HC2O4-]>[CO32-
-
(1)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
①0.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH。(选填“大于”“小于”或“等于”)
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填编号)
A.[H+]>[HC2O4-]>[HCO3-]>[CO32-] B.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
C.[H+]>[HC2O4-]>[C2O42-]>[CO32-] D.[H2CO3] >[HCO3-]>[HC2O4-]>[CO32-]
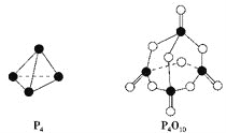
(2)白磷与氧气可发生如下反应:P4+5O2= P4O10。已知断裂下列化学键需要吸收的能量分别为: P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH=___________。
(3)25 ℃,某浓度的盐酸、氯化铵溶液中由水电离出的氢离子浓度分别为1.0×10-amol·L-1、1.0×10-b mol·L-1,这两种溶液的pH之和=___________。
(4)在t ℃时,某Ba(OH)2的稀溶液中c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 | 氢氧化钡溶液 的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则c=___________。
-
已知:
| 酸 | H2C2O4 | HF | H2CO3 | H2BO3 |
| 电离平衡常数Ka | Ka1=5.9×10-2 Ka2=6.4×10-5 | 未知 | Ka1=4.2×10-7 Ka2=5.6×10-11 | 5.8×10-10 |
(1)为了证明HF是弱酸,甲、乙、丙三位同学分别设计以下实验进行探究。
①甲同学取一定体积的HF溶液,滴入2滴紫色石蕊试液,显红色,再加入NaF固体观察到的现象是_______________,则证明HF为弱酸。
②乙同学取10ml未知浓度的HF溶液,测其pH为a,然后用蒸馏水稀释至1000ml。再测其pH为b,若要认为HF为弱酸,则a、b应满足的关系是b<_________(用含a的代数式表示)。
③丙同学用pH是指测得室温下0.10mol·L-1的HF溶液的pH为2,则测定HF为弱酸,由丙同学的实验数据可得室温下HF的电离平衡常数约为__________________。
(2)①已知H2BO3与NaOH溶液反应的离子方程式为H2BO3+OH-=B(OH)4,写出硼酸的电离方程式______________。
②向等浓度的H2C2O4与H2BO3混合溶液中逐滴加入NaOH溶液,则与OH-作用的粒子(包括分子和离子)依次为_____________,____________,____________。
③NaH C2O4溶液中加入少量的Na2CO3溶液,反应的离子方程式___________。
-
(1)碳酸:H2CO3,K1=4.3×10﹣7,K2=5.6×10﹣11
草酸:H2C2O4,K1=5.9×10﹣2,K2=6.4×10﹣5
0.1mol/L Na2CO3溶液的pH_____0.1mol/L Na2C2O4溶液的pH;(选填“大于”“小于”或“等于”)
(2)等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是_____;若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____(选填编号);
a.c(H+)>c(HC2O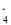 )>c(HCO
)>c(HCO )>c(CO
)>c(CO )
)
b.c(HCO )>c(HC2O
)>c(HC2O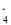 )>c(C2O
)>c(C2O )>c(CO
)>c(CO )
)
c.c(H+)>c(HC2O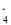 )>c(C2O
)>c(C2O )>c(CO
)>c(CO )
)
d.c(H2CO3)>c(HCO )>c(HC2O
)>c(HC2O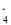 )>c(CO
)>c(CO )
)
-
25 ℃时,几种常见弱酸的Ka如下表所示[已知草酸(H2C2O4)是一种二元弱酸]:
| 弱酸 | H2C2O4 | CH3COOH | HCN | H2CO3 |
| Ka | K1=5.6×10-2 K2=5.4×10-5 | 1.8×10-5 | 6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
(1)25 ℃时,0.1 mol·L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3溶液的pH由大到小的顺序是________________________,中和等体积等pH的CH3COOH和HCN溶液消耗NaOH的物质的量________(填“前者大”或“后者大”)。
(2)KHC2O4溶液呈酸性。向10 mL 0.01 mol·L-1的H2C2O4溶液滴加0.01 mol·L-1KOH溶液V(mL),回答下列问题:
①当V<10 mL时,反应的离子方程式为________________________________。
②当V=10 mL时,溶液中HC2O 、C2O
、C2O 、H2C2O4、H+的浓度从大到小的顺序为_____________________。
、H2C2O4、H+的浓度从大到小的顺序为_____________________。
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O )+c(HC2O
)+c(HC2O );当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O
);当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O )+c(HC2O
)+c(HC2O )+c(H2C2O4);则a________(填“<”“=”或“>”)b。
)+c(H2C2O4);则a________(填“<”“=”或“>”)b。
④当V=20 mL时,再滴入NaOH溶液,则溶液中n(K+)/n(C2O )的值将________(填“变大”“变小”或“不变”)。
)的值将________(填“变大”“变小”或“不变”)。
-
已知: 乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4)。25℃时,草酸的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;碳酸(H2CO3) 的电离平衡常数为K1=4.5×10-7,K2=4.7×10-11。草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。
回答下列问题:
(1)写出水溶液中草酸的第一步电离方程式________________________。
(2)相同条件下物质的量浓度都为0.1mol/L的Na2C2O4溶液的pH 比Na2CO3溶液的pH_____(填“大”、“小”或“相等”)。
(3)常温下将0.4mol/L 的KOH 溶液20mL 与0.2mol/L 的草酸溶液20mL混合,则混合后溶液中阴离子浓度的大小顺序为___________________________。
(4) 往Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为_______________________。
(5)25℃时,向20mL碳酸钙的饱和溶液中逐滴加入cmolL的草酸钾溶液20mL后,有草酸钙沉淀生成,则c 的最小值为____________。
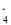 )>c(HCO
)>c(HCO )>c(CO
)>c(CO )
) )>c(HC2O
)>c(HC2O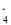 )>c(C2O
)>c(C2O )>c(CO
)>c(CO )
)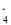 )>c(C2O
)>c(C2O )>c(CO
)>c(CO )
) )>c(HC2O
)>c(HC2O )>c(CO
)>c(CO )
)