-
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物酸锰(MnFe2O4)也可用于热化学循环分解水制氢,MnFe2O4的制备流程如下:
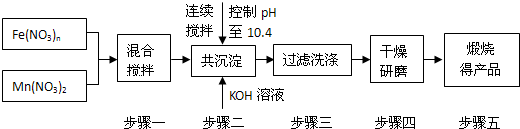
(1)原料Fe(NO3)n中n=______,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为______.
(2)步骤二中“连续搅拌”的目的是______;步骤三中洗涤干净的标准是______.
(3)利用MnFe2O4热化学循环制氢的反应可表示为:MnFe2O4 MnFe2O4-x+
MnFe2O4-x+ O2↑ MnFe2O4-x+xH2O→MnFe2O4+xH2↑
O2↑ MnFe2O4-x+xH2O→MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中X=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为______.
②该热化学循环制氢的优点有(答两点即可)______.
-
最新研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解制氢气:
①MnFe2O4(s)=MnFe2O(4-x)(s)+x/2 O2(g);△H1
②MnFe2O(4-x)(s)+xH2O(g)=MnFe2O4(s)+xH2(g);△H2 下列说法错误的是( )
A.反应①中O2是氧化产物,反应②中水是氧化剂
B.该热化学循环制氢过程简单、无污染,物料可循环使用,安全易分离
C.若MnFe2O(4-x)(s)中x=0.8,则MnFe2O(4-x)(s)中Fe2+占全部铁元素的百分率为60%
D.若xH2(g)+x/2O2 (g)=xH2O(g);△H3,则△H3=-(△H1+△H2)
-
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)热分解法制氢。某温度,H2O(g)  H2(g)+1/2O2(g)。该反应平衡常数表达式K=_____
H2(g)+1/2O2(g)。该反应平衡常数表达式K=_____
(2)热化学循环制氢。制备H2的反应步骤如下:
①Br2(g) + CaO(s) = CaBr2(s) + 1/2O2(g) ΔH=-73 kJ·mol-1
②3FeBr2(s) + 4H2O(g) = Fe3O4(s) + 6HBr(g) + H2(g) ΔH=+384 kJ·mol-1
③CaBr2(s) + H2O (g) = CaO(s) + 2HBr(g) ΔH=+212 kJ·mol-1
④Fe3O4(s)+8 HBr(g) = Br2(g) + 3FeBr2(s) + 4H2O(g) ΔH=-274 kJ·mol-1
则 H2O(g)  H2(g)+1/2O2(g) ΔH =_________kJ·mol-1。
H2(g)+1/2O2(g) ΔH =_________kJ·mol-1。
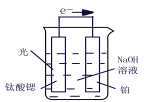
(3)光电化学分解制氢,钛酸锶光电极:4OH--4e-  O2+2H2O,则铂电极的电极反应为_______。
O2+2H2O,则铂电极的电极反应为_______。
(4)水煤气法制氢。CO(g) + H2O(g)  CO2(g)+ H2(g) ΔH <0,在850℃时,K=1。
CO2(g)+ H2(g) ΔH <0,在850℃时,K=1。
① 若升高温度到950℃时,达到平衡时K_________1(填“>”、“<”或 “=”)。
② 850℃时,若向一容积可变的密闭容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2 和x mol H2,若要使上述反应开始时向正反应方向进行,则x应满足的条件是_________。
(5)甲烷制氢。将1.0 mol CH4和2.0 mol H2O (g)通入容积为100 L的反应室,在一定条件下发生反应:CH4(g) + H2O (g)=CO (g) + 3H2(g)。测得达到平衡所需的时间为5 min,CH4的平衡转化率为50%,则用H2表示该反应的平均反应速率为_____。
(6)LiBH4具有非常高的储氢能力,分解时生成氢化锂和两种非金属单质。该反应的化学方程式为_____。
-
利用太阳能热化学硫碘循环分解水制氢反应过程如下图所示:
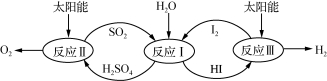
(1) 反应Ⅱ中涉及的热化学方程式为:
①H2SO4(l)=SO3(g)+H2O(g) ΔH=+177.3 kJ·mol-1
②2SO3(g) = 2SO2(g)+O2(g) ΔH=a kJ·mol-1
③2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) ΔH=+550.2 kJ·mol-1则 a= ;
(2)反应Ⅰ得到的产物可用I2进行分离。该产物的溶液在过量I2的存在下会分成两层 :含低浓度I2的H2SO4溶液层和高浓度的I2的HI溶液层。
①区分两层溶液可加入的试剂为 (填化学式)。
②下列说法正确的是 (填序号)。
A. SO2在反应Ⅰ中作氧化剂
B. 加过量I2前,H2SO4溶液和HI不互溶
C. 两层溶液的密度存在差异
D. I2在HI溶液中比在H2SO4溶液中易溶
(3)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如右图所示。
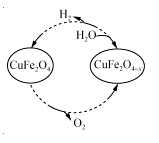
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为 。
②若x=0.15,则1 mol CuFe2O4参与该循环过程理论上一次能制得标准状况下的H2体积为 L。
③CuFe2O4可用电化学方法得到,其原理如图所示, 则阳极的电极反应式为 。
则阳极的电极反应式为 。

-
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

(1)反应Ⅰ的化学方程式是______________________________________
(2)已知反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
则SO3(g)分解的热化学方程式为____________________。
(3)L(L1、L2)、X可分别代表压强或温度其中之一。如图表示L一定时,ii中SO3(g)的质量分数随X的变化关系。
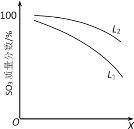
①X代表的物理量是__________。
②判断L1、L2的大小关系:L1_______L2,并简述理由:______________。
-
(6分)氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
L(L1、L2)、X可分别代表压强和温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
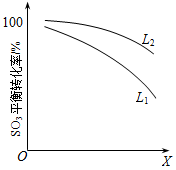
①X代表的物理量是 。
②判断L1、L2的大小关系,L1 L2
并简述理由: 。
-
人类研究氢能源从未间断过,而热化学循环分解水制 H2是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为H2和O2,这是一种节约能源、节省反应物料的技术,下图是热化学循环制氢气的流程:

(1)实验测得,1 g H2燃烧生成液态水放出142.9 kJ的热量,则表示氢气燃烧热的热化学方程式为_______。
(2)整个流程参与循环的物质是________和________(填化学式),最难进行的反应是____________(填序号)。
(3)汞虽然有毒,但用途广泛。用汞和溴化钙作催化剂,可以在较低温度下经过下列反应使水分解制氢气和氧气:①CaBr2+2H2O=Ca(OH)2+2HBr↑;②……③HgBr2+Ca(OH)2=CaBr2+HgO+H2O;④2HgO=2Hg+O2↑。反应②的化学方程式为________________________。
(4)合成氨用的H2可以甲烷为原料制得。有关化学反应的能量变化如图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________。


-
[2017新课标Ⅰ节选]下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为____________________________、____________________________,制得等量H2所需能量较少的是_____________。
-
下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。
通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为_____________________________、____________________________,制得等量H2所需能量较少的是________________________。

-
我国最近在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是
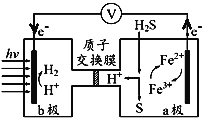
A.该装置工作时,H+由b极区流向a极区
B.该制氢工艺中光能最终转化为化学能
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液

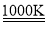 MnFe2O4﹣x+
MnFe2O4﹣x+ O2↑、MnFe2O4﹣x+xH2O→MnFe2O4+xH2↑。请认真分析上述两个反应并回答下列问题:
O2↑、MnFe2O4﹣x+xH2O→MnFe2O4+xH2↑。请认真分析上述两个反应并回答下列问题:













