-
(15分)合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) == 2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
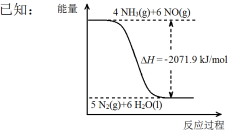
结合①中信息,尿素还原NO(g)的热化学方程式是 。
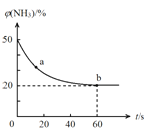
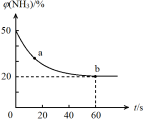
②密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) ==CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
==CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中离子浓度大小关系是c(Na+)>______。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) 2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a. 从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b. 在平衡体系中增加水的用量可使该反应的平衡常数增大
c. 降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
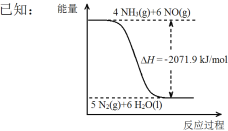
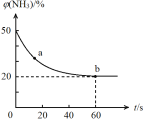
结合①中信息,尿素还原NO(g)的热化学方程式是 。
③密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>________。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) 2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a. 从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b. 在平衡体系中增加水的用量可使该反应的平衡常数增大
c. 降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
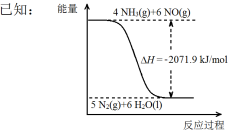

结合①中信息,尿素还原NO(g)的热化学方程式是 。
③密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>________。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) 2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a. 从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b. 在平衡体系中增加水的用量可使该反应的平衡常数增大
c. 降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
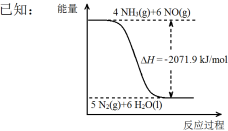
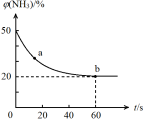
结合①中信息,尿素还原NO(g)的热化学方程式是 。
③密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>________。
-
合理应用和处理元素化合物,在生产生活中有重要意义。尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l) 2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
关于该反应的下列说法正确的是________(填字母序号)。
A.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.当容器中NH3的体积分数不再改变时,反应处于平衡状态
(2)尿素在一定条件下可将氮的氧化物还原为氮气。
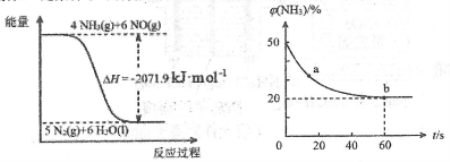
根据图像,结合(1)中信息,尿素还原NO(g)的热化学方程式是_____________________________________。
(3)密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+NH3(g) CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
-
合理应用和处理元素化合物,在生产生活中有重要意义。尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l) 2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
关于该反应的下列说法正确的是________(填字母序号)。
A.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.当容器中NH3的体积分数不再改变时,反应处于平衡状态
(2)尿素在一定条件下可将氮的氧化物还原为氮气。
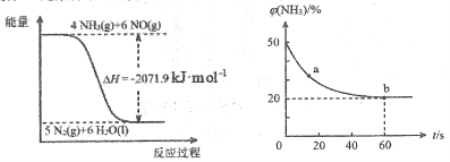
根据图像,结合(1)中信息,尿素还原NO(g)的热化学方程式是_____________________________________。
(3)密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+NH3(g) CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
-
合理应用和处理元素化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l) 2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
关于该反应的下列说法正确的是________(填序号)。
A.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.当容器中NH3的体积分数不再改变时,反应处于平衡状态
②尿素在一定条件下可将氮的氧化物还原为氮气。

根据图像,结合①中信息,尿素还原NO(g)的热化学方程式是_________。
③密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:
CO2(g)+2NH3(g) CO(NH2)2+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_____b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是_______。
CO(NH2)2+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_____b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是_______。
(2)在T℃下,分别在三个容积为10L的恒容绝热密闭容器中,发生反应: 2CO(g)+SO2(g)  S(g)+2CO2(g) △>0, 测得相关数据如下表所示。
S(g)+2CO2(g) △>0, 测得相关数据如下表所示。
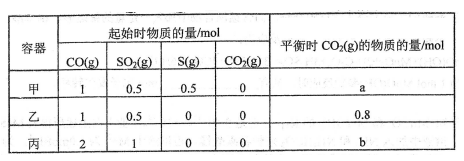
下列说法不正确的是________
A.反应开始时的速率:丙>乙 B. b=1.6 C.平衡常数:甲>乙
(3)ClO2是一种安全稳定的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备ClO2原理如下:
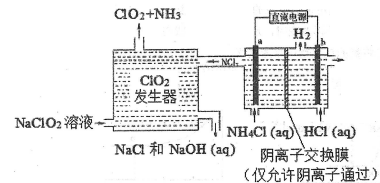
①a电极上产生的NCl3分子,常温下是一种黄色粘稠的油状液体,该分子的电子式为______。
②电解池中总反应的离子方程式为________。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。尿素[CO(NH2)2] 是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s)+H2O(l)  2NH3(g)+CO2(g) △H=+133.6kJ/mol。该反应的化学平衡常数的表达式 K=_____。关于该反应的下列说法不正确的是______(填序号)。
2NH3(g)+CO2(g) △H=+133.6kJ/mol。该反应的化学平衡常数的表达式 K=_____。关于该反应的下列说法不正确的是______(填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率减小
d.当2v正[NH3]=v逆[CO2],反应处于平衡状态
②尿素在一定条件下可将氮的氧化物还原为氮气。己知:如图1所示结合①中信息,尿素还原NO(g)的热化学方程式是____________。

③密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g) + 2NH3(g)  CO(NH2)2 (s)+ H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图2所示,则a点的正反应速率v正(CO2)___b点的逆反应速率V逆(CO 2)(填“〉”“=”或“<”);氨气的平衡转化率是________。
CO(NH2)2 (s)+ H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图2所示,则a点的正反应速率v正(CO2)___b点的逆反应速率V逆(CO 2)(填“〉”“=”或“<”);氨气的平衡转化率是________。
④NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。己知9.2gNa和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是________;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是 c(Na+)>_____。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:
CO(NH2)2(s)+H2O(l) 2NH3(g)+CO2(g) △H=+133.6 kJ/mol。关于该反应的下列说法正确的是____________________(填序号)。
2NH3(g)+CO2(g) △H=+133.6 kJ/mol。关于该反应的下列说法正确的是____________________(填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
d. 缩小容器的体积,平衡向逆反应方向移动,达新平衡时NH3的浓度大于原平衡
②尿素在一定条件下可将氮的氧化物还原为氮气。
已知: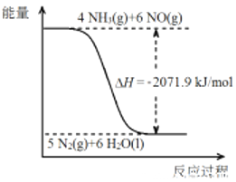
再结合①中的信息,则反应2CO(NH2)2(s)+6NO(g) 5N2(g)+2CO2(g)+4H2O(l)的△H =_______kJ/mol。
5N2(g)+2CO2(g)+4H2O(l)的△H =_______kJ/mol。
③密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g),混合气体中NH3的物质的量百分含量随时间变化关系如图所示。则a点的正反应速率v正(CO2)______b点的逆反应速率v逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率为________________。
CO(NH2)2(s)+H2O(g),混合气体中NH3的物质的量百分含量随时间变化关系如图所示。则a点的正反应速率v正(CO2)______b点的逆反应速率v逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率为________________。

(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式为_________;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中离子浓度大小关系是c(Na+)>______。
(3)用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度来制备纳米Cu2O,装置如图所示:
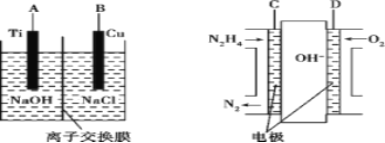
上述装置中B电极应连电极__(填“C”或“D”)。该电解池中的离子交换膜为__(填“阴”或“阳”)离子交换膜。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,其分子中各原子的原子半径大小关系为______,碳原子核外有___种运动状态不同的电子。
(2)氰化钠(NaCN)中,N元素显-3价,则非金属性N___________C(填“<”、“=”或“>”),写出氰化钠的电子式_______________。
(3)氰化钠属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(a)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑,则A的化学式为___。
(b)NaCN与Na2S2O3二者等物质的量反应可得到两种含硫元素的离子,其中一种遇到Fe3+显血红色。写出该反应的离子方程式____________。
(4)NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是______;恰好反应后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是__________。
 2NH3(g)+CO2(g) △H=+133.6kJ/mol。该反应的化学平衡常数的表达式K=_______________。关于该反应的下列说法正确的是______ (填序号)
2NH3(g)+CO2(g) △H=+133.6kJ/mol。该反应的化学平衡常数的表达式K=_______________。关于该反应的下列说法正确的是______ (填序号) 。
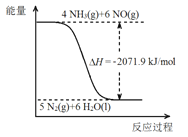
。
 CO(NH2)2(s)+H2O(g),混合气体中NH3的物质的量百分含量[ϕ(NH3)]随时间变化关系如图所示,则a点的正反应速率v正(CO2) ______b点的逆反应速率v逆(CO2) (填“>”、“=”或“<”);氨气的平衡转化率是______。
CO(NH2)2(s)+H2O(g),混合气体中NH3的物质的量百分含量[ϕ(NH3)]随时间变化关系如图所示,则a点的正反应速率v正(CO2) ______b点的逆反应速率v逆(CO2) (填“>”、“=”或“<”);氨气的平衡转化率是______。