-
(1)氯化铁水解的离子方程式为 ,加热该溶液,蒸干并灼烧得到____________(填化学式)
(2)实验室在配制Na2CO3溶液时,为了抑制水解应向溶液中加入少量的_________
(3)泡沫灭火器中装有NaHCO3溶液和AlCl3溶液,在灭火时能迅喷出气体并伴有白色胶状物,写出该反应的离子方程式
高二化学填空题中等难度题查看答案及解析
-
(1)氯化铁水解的离子方程式为_________________________________,加热氯化铁溶液,蒸干并灼烧得到_______(填化学式)。
(2)25℃时,NH4Cl溶液显_________性,原因是(用离子方程式表示)__________,若加入少量的氨水,使溶液中c(NH4+)=c(Cl﹣),则溶液的pH___7(填“>”、“<”或“=”)
高二化学填空题简单题查看答案及解析
-
(1)氯化铝水溶液呈______性,原因是______(用离子方程式表示).把AlCl3溶液蒸干灼烧,最后得到的主要固体产物是______(填化学式).
(2)硫化钠溶于水时发生水解,其水解的离子方程式为______,在配制硫化钠溶液时可以加入少量的______(填化学式)以抑制其水解.
(3)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
CO(g)+O2(g)═CO2(g)△H=-283kJ/mol
则1mol C(s)与O2(g)反应生成CO(g)的热化学方程式为______.高二化学解答题中等难度题查看答案及解析
-
(1)氯化铝水溶液呈 性,原因是: (用离子方程式表示);把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(2)硫化钠溶于水时发生水解,其水解的离子方程式为 (只写第一步),在配制硫化钠 溶液时可以加入少量的 以抑制其水解。
高二化学填空题中等难度题查看答案及解析
-
(1)硫酸铁净水原因(离子方程式):_____,SnCl2水解成碱式氯化亚锡(化学方程式)_____,要除去CuCl2溶液中FeCl3,可以向溶液中加入_______,将AlCl3溶液蒸干并灼烧所得固体的化学式为___。
(2)以石墨为电极,电解FeI2溶液,阳极电极反应式为________,利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,装置如图所示:
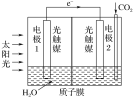
①电极2的电极反应式是_______;
②在标准状况下,当电极2室有11.2 L CO2反应。理论上电极1室液体质量___ (填“增加”或“减少”)___ g。
(3) 离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7—和AlCl4—组成的离子液体作电解液时,可在钢制品上电镀铝。钢制品应接电源的_____极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为__________。
(4)已知AsO43—+2I-+2H+
AsO33—+I2+H2O是可逆反应,设计如图装置(C1、C2均为石墨电极)开始时:C2棒电极反应式______,当电流表___时,反应达到化学平衡状态。
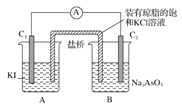
高二化学综合题中等难度题查看答案及解析
-
(1)根据氯化铁溶液回答下列问题:
①向FeCl3溶液中加入少量NaHCO3。产生的现象为___。用离子方程式表示其原因___。
②不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是___。
③在配制FeCl3溶液时,为防止溶液变浑浊,应加入___。
(2)利用反应Cu+H2O2+H2SO4=CuSO4+2H2O设计一个原电池,回答下列问题:
①负极材料为___;正极反应式为___。
②反应过程中SO
向____极移动。
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了___克。
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式
CH3COOH
H2CO3
HClO
电离平衡常数
Ka=1.8×10-5
Ka1=4.3×10-7
Ka2=5.6×10-11
Ka=3.0×10-8
①物质的量浓度均为0.1mol•L-1的四种溶液:pH由小到大排列的顺序是__(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②常温下,0.1mol•L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是___(填字母)
A.c(H+) B.
C.c(H+)•c(OH-) D.
E.
③写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____。
④25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=____(填准确数值)。
⑤标准状况下,将1.12LCO2通入100mL1mol•L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+____。
高二化学综合题中等难度题查看答案及解析
-
完成并分析下列化学原理
(1)在配制三氯化铁溶液时,为了防止发生水解,可以加入少量的________。
(2)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是____________;
(3)除去CuCl2溶液中少量的FeCl3,加入的试剂可以是_____________。
(4)在常温下,稀释等PH值的HCl、HF两种酸的稀溶液时,溶液pH随加水量的变化如图所示,能表示HF的稀释过程的曲线是:_____________
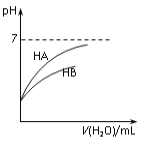
(5)amol·L-1(NH4 )2SO4溶液pH=5,其原因是_______(用相应的方程式说明)。
(6)有4种混合溶液,分别由等体积0.1 mol·L-1的两种溶液混合而成:①NH4Cl与 CH3COONa ②NH4Cl与HCl ③NH4Cl与NaCl ④NH4Cl与NH3·H2O(混合液呈碱性)。溶液中c(H+)由小到大的顺序为:(填混合溶液的编号)____________
(7)在做Zn与稀H2SO4反应制取H2的实验中,向溶液中滴加几滴CuSO4溶液,反应放出H2速度加快的原因是:__________________________
高二化学综合题中等难度题查看答案及解析
-
(1)氯化铝水溶液呈______(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示)______.把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是(化学式)______.
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量______(化学式)溶液.高二化学解答题中等难度题查看答案及解析
-
(1)氯化铝水溶液呈______性,原因是______(用离子方程式表示).把AlCl3溶液蒸干灼烧,最后得到的主要固体产物是______(填化学式).
(2)室温下,将pH=13的NaOH溶液与pH=2的HCl溶液按1:9的体积比混合,设混合溶液的总体积为二者相加,则所得混合液的pH值是______.
(3)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/molCO(g)+1/2O2(g)═CO2(g)△H=-283kJ/mol,则1mol C(s)与O2(g)反应生成CO(g)的热化学方程式为______.高二化学解答题中等难度题查看答案及解析
-
按要求完成下列填空:
(1)将AlCl3溶液加热蒸干并灼烧可得到 (填化学式)。
(2)盛放纯碱溶液的试剂瓶不能用玻璃塞,是因为 。
(3)泡沫灭火器灭火时发生反应的离子方程式是 。
(4)常温下将0.01molCH3COONa和0.02molHCl溶于水,配成0.5L混合溶液。溶液中共有 种粒子,各离子浓度从大到小的顺序为 。
高二化学填空题中等难度题查看答案及解析