硝酸发生氧化还原反应的时候,一般硝酸越稀,对应的还原产物中氮的化合价越低。现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示。下列说法中不正确的是

A.无法求出曲线C点数值
B.合金与硝酸反应时硝酸过量
C.合金中铝的物质的量为0.008 mol
D.合金中金属的物质的量共为0.032 mol
高二化学选择题中等难度题
硝酸发生氧化还原反应的时候,一般硝酸越稀,对应的还原产物中氮的化合价越低。现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示。下列说法中不正确的是

A.无法求出曲线C点数值
B.合金与硝酸反应时硝酸过量
C.合金中铝的物质的量为0.008 mol
D.合金中金属的物质的量共为0.032 mol
高二化学选择题中等难度题
硝酸发生氧化还原反应的时候,一般硝酸越稀,对应的还原产物中氮的化合价越低。现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示。下列说法中不正确的是

A.无法求出曲线C点数值
B.合金与硝酸反应时硝酸过量
C.合金中铝的物质的量为0.008 mol
D.合金中金属的物质的量共为0.032 mol
高二化学选择题中等难度题查看答案及解析
硝酸发生氧化还原反应的时候,一般硝酸越稀,对应的还原产物中氮的化合价越低。现有一定量的铝、铁合金与一定量稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4mol/L NaOH溶液,所加NaOH溶液的体积(V)与产生沉淀的物质的量(n)关系如图所示。下列说法中不正确的是
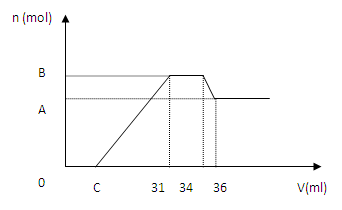
A.合金与硝酸反应时硝酸过量 B.合金中铝的物质的量为0.008mol
C.合金中金属的物质的量共为0.032mol D.无法求出C 点的值
高二化学选择题中等难度题查看答案及解析
(12分)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0)。试回答下列问题:
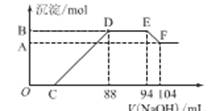
(1)写出反应过程中的离子反应方程式:
OC段________,
DE段,
EF段_____________________________________________________。
(2)硝酸溶液的物质的量浓度为________mol·L-1
(3)B的值为_________mol,C的值为________mL。
【解析】由题意知,金属与硝酸反应时,硝酸的还原产物为NH4NO3,由图又可看出金属与硝酸反应后,硝酸是过量的,故金属的氧化产物为Fe(NO3)3、Al(NO3)3。图中:①O→C:H++OH-===H2O;②C→88:R3++3OH-===R(OH)3↓(R代表Fe或Al);③88→94:NH+OH-===NH3·H2O;④94→104:Al(OH)3+OH-===AlO+2H2O。由④知n[Al(OH)3]=0.01 L×4 mol·L-1=0.04 mol=n(Al)。由③知,n(NH4NO3)=0.006 L×4 mol·L-1=0.024 mol,根据反应中得失电子相等的原则得:3n(R3+)=0.024×8=0.192 mol,则n(R3+)=0.064 mol=n(合金),故混合物中n(Fe)=0.024mol。0→88 mL中,用于沉淀金属离子的OH-有0.064 mol×3=0.192 mol,故C点:(0.088 L×4 mol·L-1-0.192 mol)÷4 mol·L-1=0.04 L,即40 mL。据原子守恒可知硝酸的物质的量是0.094L×4mol/L=0.376mol。其浓度是3.76mol/L。
高二化学填空题简单题查看答案及解析
高二化学解答题中等难度题查看答案及解析
现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为a mol,Cu的物质的量分数为x;研成粉末后,全部投入含b mol HNO的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为__________。(写出所有可能情况)
(2)当溶液中金属离子只有Fe、Cu
时,则b的取值范围是(用a、x表示)___________。
(3)当x=0.5,溶液中Fe与Fe
的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
高二化学填空题困难题查看答案及解析
在一定条件下,NO跟NH 3 可以发生反应生成N 2 和H 2 O。现有NO和NH 3 的混合物1 mol,充分反应后所得产物中,若经还原得到的N 2 比经氧化得到的N 2 多1.4 g。
(1)写出反应的化学方程式并标出电子转移的方向和数目。
(2)若以上反应进行完全,试计算原反应混合物中NO与NH 3 的物质的量可能各是多少。
高二化学计算题困难题查看答案及解析
一定条件下硝酸铵受热分解的化学方程式(未配平)为:NH4NO3 - HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为:
A.5∶3 B.5∶4 C.1∶1 D.3∶5
【解析】被氧化化合价升高,即N原子从-3价升高到0价,失去3个电子。被还原,化合价降低,即N原子从+5价降低到0价,得到5个电子。所以根据得失电子守恒可知被氧化与被还原的氮原子数之比为5∶3,即答案是A。
高二化学选择题简单题查看答案及解析
某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原HNO3的物质的量之比为2∶1时,还原产物可能是
A.N2O B.NO C.NO2 D.N2
高二化学选择题中等难度题查看答案及解析
氮及其化合物在工业生产中有广泛用。
(1)稀硝酸与二价活泼金属M反应制备硝酸盐,当反应物之比n(HNO3)∶n(M)=5∶2时,还原产物为___(填化学式)。
(2)连二次硝酸(HO-N=N-OH)是一种二元弱酸,向0.1 mol·L-1连二次硝酸钠(Na2N2O2)溶液中滴加酚酞,溶液变红色 ,用离子方程式表示其主要原因:__________________。
(3)已知以下热化学方程式: 2N2O5(g)4NO2(g)+O2(g) ΔH1
2NO(g)+O2(g)=2NO2(g) ΔH2
3NO2(g)N2O5(g)+NO(g) ΔH3
①ΔH3=______________________(用ΔH1、ΔH2表示)。
②一定温度下,在恒容密闭容器中进行反应:3NO2(g)N2O5(g)+NO(g),下列表明反应已达到平衡状态的是________。
A.容器内总压强保持不变 B.容器内气体密度保持不变
C.v正(NO2)∶v逆(N2O5)=3∶1 D.保持不变
(4)在密闭容器中充入NO,发生反应2NO(g)N2(g)+O2(g) ΔH,达到平衡之后,升高温度,平衡常数K减小。
①ΔH________0。(填“>”“<”或“=”)
②上述反应达到平衡之后,仅缩小容器体积,下列推断正确的是_________。
A.NO的浓度不再变化
B.NO的转化率不再变化
C.正、逆反应速率不再变化
D.容器内气体压强不再变化
(5)在2 L恒容密闭容器中投入一定量的N2O5(g),发生反应:2N2O5(g)4NO2(g)+O2(g),测得c(N2O5)与温度关系如图所示。T2 K时,该反应的平衡常数K为_________。若平衡时温度不变,再向容器中充入少量的N2O5气体,达到新平衡时N2O5的转化率会_________(填“增大”“减小”或“不变”)。

高二化学综合题困难题查看答案及解析
亚硝酸(HNO2)参加反应时,既可作氧化剂,也可作还原剂。当它作还原剂时,可能生成的产物是
A.NH3 B.N2 C.N2O3 D.HNO3
高二化学选择题中等难度题查看答案及解析