根据下图能量变化曲线判断,下列说法正确的是
A. H2(g)+1/2O2(g)=H2O(l) △H=-242kJ·mol-1
B. 若H—H、O==O的键能分别是436 kJ·mol-1和496 kJ·mol-1,则H—O的键能是463 kJ·mol-1
C. 据图可知,氢气的燃烧热为242 kJ·mol-1
D. 10克氢气在氧气中完全燃烧,放出热量为1210kJ
高三化学选择题中等难度题
根据下图能量变化曲线判断,下列说法正确的是

A. H2(g)+1/2O2(g)=H2O(l) △H=-242kJ·mol-1
B. 若H—H、O==O的键能分别是436 kJ·mol-1和496 kJ·mol-1,则H—O的键能是463 kJ·mol-1
C. 据图可知,氢气的燃烧热为242 kJ·mol-1
D. 10克氢气在氧气中完全燃烧,放出热量为1210kJ
高三化学选择题中等难度题
根据下图能量变化曲线判断,下列说法正确的是

A. H2(g)+1/2O2(g)=H2O(l) △H=-242kJ·mol-1
B. 若H—H、O==O的键能分别是436 kJ·mol-1和496 kJ·mol-1,则H—O的键能是463 kJ·mol-1
C. 据图可知,氢气的燃烧热为242 kJ·mol-1
D. 10克氢气在氧气中完全燃烧,放出热量为1210kJ
高三化学选择题中等难度题查看答案及解析
能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式
| ① | H2(g)+ | |||||||
| ② | 2H2(g)+ O2(g)= 2H2O(l) △H =﹣572kJ/mol; | |||||||
| ③ | C(s)+ | |||||||
| ④ | C(s)+ O2(g)= CO2(g) △H =﹣393.5kJ/moL; | |||||||
| ⑤ | CO2(g)+ 2H2O(g)= CH4(g)+ 2O2(g)△H = + 802kJ/moL | |||||||
| 化学键 | O=O | C-C | H-H | O-O | C-O | O-H | C-H | |
| 键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 | |
则下列说法正确的是
A.H2燃烧热的热化学方程式为H2(g)+ O2(g)= H2O(g) △H =﹣242kJ /mol
B.热化学方程式:C(s)+ H2O(g) H2(g)+ CO(g) △H = + 175.5 kJ/moL
C.CH4的燃烧热△H =— 802 kJ/moL
D.估算出C=O键能为800kJ/moL
高三化学选择题困难题查看答案及解析
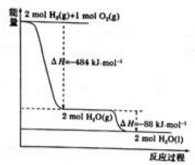
依据下图判断,下列说法正确的是

A.2 mol H2(g)与1 mol O2(g)所具有的总能量比2 mol H2O(g) 所具有的总能量低
B.氢气的燃烧热为△H = -241.8 kJ·mol-1
C.液态水分解的热化学方程式为:2H2O(l) == 2H2(g) + O2(g) △H = +571.6 kJ·mol-1
D.H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量
高三化学选择题中等难度题查看答案及解析
根据能量变化示意图,下列说法正确的是

A. 1molC和1molH2O反应生成1molCO和1molH2一定吸收131.3kJ的热量
B. 反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(a-b)KJ/mol
C. 该反应过程反应物断键吸收的能量要小于生成物成键放出的能量
D. 加入适当的催化剂,可以加快正、逆反应速率
高三化学单选题困难题查看答案及解析
根据能量变化示意图,下列说法正确的是

A. 1molC和1molH2O反应生成1molCO和1molH2一定吸收131.3kJ的热量
B. 反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(a-b)KJ/mol
C. 该反应过程反应物断键吸收的能量要小于生成物成键放出的能量
D. 加入适当的催化剂,可以加快正、逆反应速率
高三化学选择题困难题查看答案及解析
已知反应H2(g)+ O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )

A. H2(g)+ O2(g)=H2O(g) △H=c kJ·mol-1
B. 2H2O(g)=2H2 (g)+O2 (g) △H=—2(a-b) kJ·mol-1
C. 1 mol氢气与0.5 mol氧气总能量为akJ
D. 2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量小于2(b-a)kJ
高三化学选择题简单题查看答案及解析
已知反应H2(g)+
O2(g)===H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是( )

A. H2(g)+O2(g)===H2O(g) ΔH=c kJ·mol-1
B. 2H2O(g)===2H2(g)+O2(g) ΔH=-2(a-b)kJ·mol-1
C. 1 mol氢气与0.5 mol氧气总能量为a kJ
D. 2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量小于2(b-a) kJ
高三化学选择题中等难度题查看答案及解析
根据下图所示情况,判断下列说法中正确的是( )
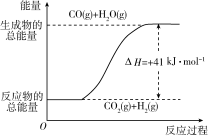
A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41 k
J·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值小于41 kJ·mol-1
高三化学选择题简单题查看答案及解析
己知断裂1molH2(g)中的H—H键需吸收436kJ 能量,断裂1molO2中的共价键需吸收496kJ能量,且氢气在氧气中燃烧的能量变化如图所示。下列说法正确的是
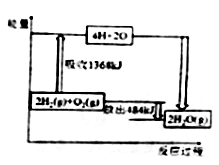
A. H2O(g)=H2(g)+1/2O2(l) △H=+242kJ/mol
B. H2(g)+1/2O2 (g)= H2O (l) △H<-242kJ/mol
C. 形成1molH2O(g)中的化学键需吸收926kJ
D. 2H2(g)+ O2 (g)= 2H2O (g) △H=-1852kJ/mol
高三化学选择题中等难度题查看答案及解析
已知:
①CO(g) +H2O(g)=CO2(g)+H2(g) △H = -41.2 kJ • mol-1
②CH4(g) +H2O(g)=CO(g) +3H2(g)的能量变化如下图所示
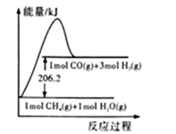
下列有关说法正确的是
A. ①和②均为放热反应
B. ①的反应物总能量低于生成物总能量
C. CO2(g) +CH4(g)=2CO(g) +2H2(g) △W = -247.4 kJ • mol-1
D. CH4(g) +H2O(g)=CO(g) +3H2(g)的活化能大于206.2 kJ • mol-1
高三化学选择题困难题查看答案及解析