-
已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200 mL混合溶液中含FeI2、FeBr2各0.10 mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其他反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是________,剩余Fe2+的物质的量为________。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为________,若最终所得溶液为400 mL,其中主要阳离子及其物质的量浓度为________。
(3)通过对上述反应的分析,试判断Cl2,I2,Fe3+,Br2四种氧化剂的氧化能力由强到弱的顺序是_________________________________________________。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:_________________;上述所有反应共消耗Cl2________mol。
高三化学填空题困难题查看答案及解析
-
(15分)已知几种离子的还原能力强弱顺序为I->Fe2+>Br-,现有200 mL混合溶液中含FeI2、FeBr2各0.10 mol,向其中逐滴滴入氯水(假定Cl2分子只与溶质离子反应,不考虑其他反应)
(1)若氯水中有0.15 mol Cl2被还原,则所得溶液中含有的阴离子主要是________,剩余Fe2+的物质的量为________。
(2)若原溶液中Br-有一半被氧化,共消耗Cl2的物质的量为________,若最终所得溶液为400 mL,其中主要阳离子及其物质的量浓度为________。
(3)通过对上述反应的分析,试判断Cl2、I2、Fe3+、Br2四种氧化剂的氧化能力由强到弱的顺序是________________________。
(4)上述反应若原溶液中溶质离子全部被氧化后,再滴入足量氯水,则I2全部被Cl2氧化成HIO3(强酸)。试写出此反应的离子方程式:_________________;上述所有反应共消耗Cl2________mol。
高三化学填空题困难题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中正确的是

A.离子的还原性顺序为:Fe2+>Br->I-
B.原混合溶液中FeBr2的物质的量为4mol
C.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
D.当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
高三化学选择题极难题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中正确的是

A.离子的还原性顺序为:Fe2+>I->Br-
B.原混合溶液中FeBr2的物质的量为4mol
C.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=1∶2∶3
D.当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
高三化学选择题中等难度题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:
==2Fe3++2Br-、2Fe3++2I-==2Fe2++I2,下列说法中错误的是
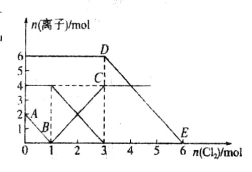
A.还原性:I->Fe2+>Br-
B.线段AB表示Fe2+被氯气氧化
C.线段BC表示生成4 mol Fe3+
D.原溶液中n (
)=6 mol
高三化学选择题中等难度题查看答案及解析
-
已知,还原性I->Fe2+ >Br-。向FeI2和FeBr2物质的量之比为1:1的混合溶液中逐滴滴入氯水,下列离子反应不可能发生的是
A.2Fe2+ + 4I-+ 3Cl2 → 2Fe3+ + 2I2 + 6Cl-
B.2Fe2+ + 2I-+ 2Cl2 → 2Fe3+ + I2 + 4Cl-
C.2Fe2+ + 2I-+ 2Br-+3Cl2 → 2Fe3+ + I2 + Br2 + 6Cl-
D.2Fe2+ + 4I-+ 4Br-+ 5Cl2 → 2Fe3+ + 2I2 + 2Br2 + 10Cl-
高三化学单选题简单题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。则下列有关说法中不正确的
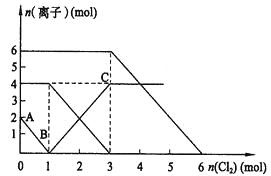
A. 还原性:I- >Fe2+ >Br-
B. 原混合溶液中FeBr2的物质的量为6mol
C. 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D. 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
高三化学选择题中等难度题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。则下列有关说法中不正确的
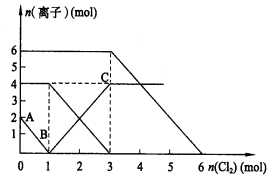
A.还原性:I- >Fe2+ > Br-
B.原混合溶液中FeBr2的物质的量为6mol
C.当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
高三化学选择题中等难度题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。
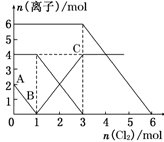
则下列有关说法中,不正确的是( )
A.还原性:I->Fe2+>Br-
B.原混合溶液中FeBr2的物质的量为6 mol
C.当通入2molCl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D.原溶液中:n(Fe2+)∶ n(I-)∶ n(Br-)=2∶ 1∶ 3
高三化学选择题困难题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.则下列说法中不正确的是

A.还原性:I->Fe2+>Br-
B.原混合溶液中FeBr2的物质的量为3mol
C.线段AB表示Fe2+被氯气氧化
D.原溶液中:n(Fe2+):n(I-):n(Br-)═2:1:3
高三化学选择题极难题查看答案及解析