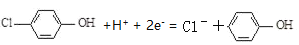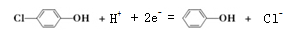-
近年华北地区频繁的雾霾天气已经引起人们的高度重视,化学反应原理可用于治理环境污染,请回答下列问题:
(1)一定条件下,可以用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:2CO(g)+O2(g) = 2CO2(g) ΔH= -566 kJ·mol-1
S(l) +O2(g) = SO2(g) ΔH=-296 kJ·mol-1
则用CO处理燃煤烟气的热化学方程式是_____________________。
②在一定温度下,在2 L密闭容器中投入2 mol CO、l mol SO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K的数值为____________。
(2)SNCR—SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:
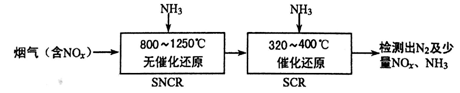
已知该方法中主要反应的热化学方程式:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1,在一定温度下,在密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1,在一定温度下,在密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
a. 4v逆(N2) = v正(O2)
b.混合气体的密度保持不变
c. c(N2)∶c(H2O)∶c(NH3)=4∶6∶4
d.单位时间内断裂4 mol N-H键的同时断裂4 mol 键
键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。

①SNCR技术脱硝的最佳温度选择925 ℃的理由是_____________。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是________________;但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是__________________。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
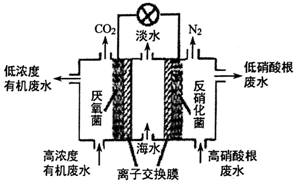
①中间室的Cl-移向_________(填“左室”或“右室”),处理后的含硝酸根废水的pH__________(填“降低”或“升高”)
②若图中有机废水中有机物用C6H12O6表示, 请写出左室发生反应的电极反应式:_________________。
-
前两年华北地区频繁出现的雾霾天气引起了人们的高度重视,化学反应原理可用于治理环境污染,请回答以下问题。
(1)一定条件下,可用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:2CO(g) + O2(g) = 2CO2(g) ΔH = −566 kJ·mol‾1
S(l) + O2(g) = SO2(g) ΔH = −296 kJ·mol‾1
则用CO处理燃煤烟气的热化学方程式是________________________。
②在一定温度下,向2 L 密闭容器中充入 2 mol CO、1 mol SO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K = _________________。
(2)SNCR─SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:

已知该方法中主要反应的热化学方程式:
4NH3(g) + 4NO(g) + O2(g) ⇌ 4N2(g) + 6H2O(g) ΔH = −1646 kJ·mol‾1,在一定温度下的密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
a.4υ逆(N2) = υ正(O2)
b.混合气体的密度保持不变
c.c(N2):c(H2O):c(NH3)=4:6:4
d.单位时间内断裂4 mol N─H键的同时断裂4 mol N≡N键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。
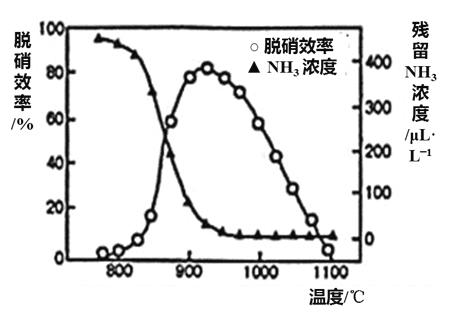
①SNCR技术脱硝的温度选择925 ℃的理由是___________________。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是____________________________________;但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是_____________________。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
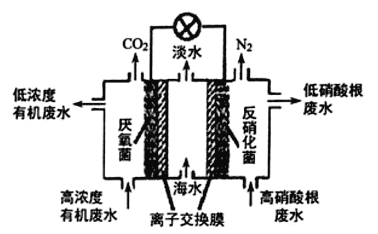
①中间室的Cl‾ 移向_________(填“左室”或“右室”),处理后的含硝酸根废水的pH__________(填“增大”或“减小”)
②若图中有机废水中的有机物用C6H12O6表示,请写出左室发生反应的电极反应式:______________________________________________。
-
近年来,新能源开发和环境保护问题日益引起人们的重视,新型电池是科学家们非常重视的研究方向。用吸附了 的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
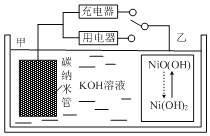
A.碳纳米管的作用只是吸附氢气
B.放电时,乙电极反应为
C.充电时,电池的甲电极与直流电源的正极相连放电
D.电池总反应为H2+2NiO(OH) 2Ni(OH)2
2Ni(OH)2
-
(14分)近几年来,我国中东部地区陷入严重的雾霾天气,面对全球近期的气候异常,环境问题再次成为焦点。非金属氧化物的合理控制和治理是优化我们生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
Ⅰ、目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-57kJ•mol-1
②4CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ•mol-1
③H2O(g)=H2O(l) △H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g),CO2(g)和H2O(l)的热化学方程式________________。
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+ 2NO(g) N2(g)+CO2(g)某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度(mol/L) 时间(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
①T℃时该反应的平衡常数为____________(结果保留两位有效数字)。
②30 min后改变某一条件,反应重新达到平衡,则改变的条件可能是___________________。
③若30min后升高温度重新达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应
△H_________0(填“<”“>”“=”)。
Ⅱ、某科研小组为治理SO2对大气的污染,利用烟气中的SO2为原料制取硫酸。
(1)利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式__________。
(2)利用Na2SO3溶液充分吸收SO2制得NaHSO3溶液。
①常温时吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
以下离子浓度关系的判断正确的是
A.NaHSO3溶液中c(H+)<c (OH-)
B.Na2SO3溶液中c(Na+)>c (SO32-)>c (HSO3-)>c (OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c (HSO3-)>c (SO32-)>c(OH-)=c(H+)
D.当n(SO32-):n(HSO3-)=1:1时,c(Na+)=c (HSO3-)+2c (SO32-)
②然后电解该NaHSO3溶液可制得硫酸。电解原理示意图如下图所示。请写出开始时阳极反应的电极反应式______________________________________。
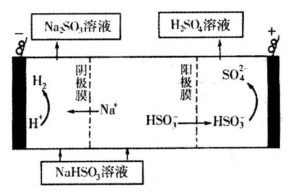
-
现在污水治理越来越引起人们的重视,通过膜电池可以除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法正确的是
),其原理如图所示,下列说法正确的是
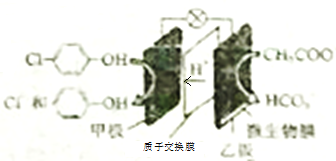
A. 甲极为电池的正极,发生氧化反应 B. 电流从乙极经导线、小灯泡流向甲极
C. 甲极的电极反应式为: 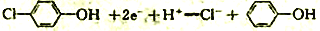 D. 当外电路中有0.2mole-转移时,甲板区增加H+0.2mol
D. 当外电路中有0.2mole-转移时,甲板区增加H+0.2mol
-
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )

A.b为电池的正极,发生还原反应
B.电流从b极经导线、小灯泡流向a极
C.当外电路中有0.2mole-转移时,a极区增加的H+的个数为0.2NA
D.a极的电极反应式为: +2e-+H+=Cl-+
+2e-+H+=Cl-+
-
污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚 ,其原理如图所示,下列说法不正确的是
,其原理如图所示,下列说法不正确的是
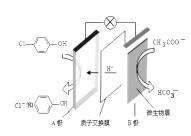
A.电流方向从B极沿导线经小灯泡流向A极
B.A为电池的正极,发生还原反应
C.A极的电极反应式为: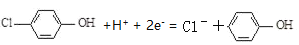
D.当外电路中有0.2mole-转移时,进入A极区的H+的个数为0.2NA
-
(7分)环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=== 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) === 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:_______________________;
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g)
N2 (g)+CO2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为 。
②下列各项能判断该反应达到平衡状态的是 。
A.容器内压强保持不变
B.速率关系:2v(NO)(正) = v (N2)(逆)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
③在相同条件下,若在容器中放人生石灰,则NO的平衡转化率 (填“增大”、“不变”或“减小”)。
-
(7分)环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=== 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) === 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g)  N2 (g)+CO2 (g)
N2 (g)+CO2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为 。
②下列各项能判断该反应达到平衡状态的是 。
A.容器内压强保持不变
B.速率关系:2v(NO)(正) = v (N2)(逆)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
③在相同条件下,若在容器中放入生石灰,则NO的平衡转化率 (填“增大”、“不变”或“减小”)。
-
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚( ),其原理如图所示,下列说法正确的是
),其原理如图所示,下列说法正确的是
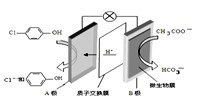
A.A为电池的正极,发生还原反应
B.电流方向从B极沿导线经小灯泡流向A极
C.A极的电极反应式为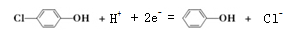
D.当外电路中有0.2mole-转移时,进入A极区的H+的个数为0.2NA

4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1,在一定温度下,在密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
键








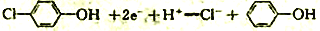 D. 当外电路中有0.2mole-转移时,甲板区增加H+0.2mol
D. 当外电路中有0.2mole-转移时,甲板区增加H+0.2mol