-
(1)以下两个反应在理论上能设计成原电池的反应是_____(填字母)。
A. NaOH+HCl=NaCl+H2O;B.2FeCl3+Fe=3FeCl2
(2)选择适宜的材料和试剂将(1)中你选择的反应设计为原电池装置。
①该电池的负极材料是______,离子导体是 ________。
②该电池的正极反应是________反应(填“氧化”或“还原”),电池的正极电极反应式为______。
③该电池放电时溶液中阳离子移向______(填“正”或“负”)极。
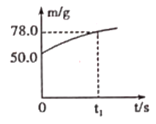
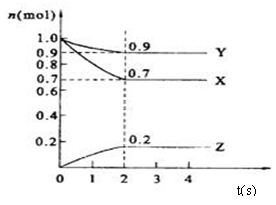
④该电池放电过程中,若测得电解质溶液的质量与时间的关系如图所示,则反应从开始至t1时,电路中转移电子的物质的量为________。
-
(1)现有如下两个反应:(A)NaOH+HCl=NaCl+H2O;(B)2FeCl3+Cu=2FeCl2+CuCl2,根据两反应本质,判断能设计成原电池的反应是___(填字母)。
(2)选择适宜的材料和试剂将(1)中你的选择设计为一个原电池。写出电池的正极电极反应式___。
(3)氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内部的新型发电装置,是一种具有应用前景的绿色电源。如图为氢氧燃料电池原理示意图,按照此图的提示回答下列问题:
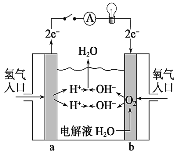
①该燃料电池的负极是___(填“a”或“b”)。
②___(填化学式)发生还原反应。
③总反应式是___。
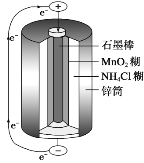
(4)锌锰干电池是最早使用的化学电池,其基本构造如图所示:锌锰干电池的负极是锌(Zn),电路中每通过0.4mole-,负极质量减少___g;工作时NH 在正极放电产生两种气体,其中一种气体分子是10e-的微粒,正极的电极反应式是___。
在正极放电产生两种气体,其中一种气体分子是10e-的微粒,正极的电极反应式是___。
-
在理论上不能用于设计原电池的化学反应是 ( )
A.HCl ( aq ) + NaOH ( aq ) = NaCl ( aq ) + H2O ( l ) △H < 0
B.2CH3OH ( l ) +3O2 ( g ) = 2CO2 ( g ) + 4H2O ( l ) △H < 0
C.4Fe (OH)2 ( s ) + 2H2O ( l ) + O2 ( g ) = 4Fe (OH)3( s ) △H < 0
D.2H2 ( g ) + O2 ( g ) = 2H2O ( l ) △H < 0
-
在理论上不能用于设计原电池的化学反应是 ( )
A.HCl ( aq ) + NaOH ( aq ) = NaCl ( aq ) + H2O ( l ) △H < 0
B.2CH3OH ( l ) +3O2 ( g ) = 2CO2 ( g ) + 4H2O ( l ) △H < 0
C.4Fe (OH)2 ( s ) + 2H2O ( l ) + O2 ( g ) = 4Fe (OH)3( s ) △H < 0
D.2H2 ( g ) + O2 ( g ) = 2H2O ( l ) △H < 0
-
现有如下两个反应:a.NaOH+HCl=NaCl+H2O b.Cu+2Ag+ =Cu2+ +2Ag
(1)反应____(填字母)不能设计成原电池。原因是__________________________。
(2)a反应为______反应(填“放热”或“吸热”),NaOH和HCl的总能量________(填“大于”“小于”或“等于”)NaCl和H2O的总能量。
(3)已知HCl中H-Cl键的键能为431 kJ·mol-1,则断开1molH-Cl键_____431 kJ的能量,形成1molH-Cl键_____431 kJ的能量。(填“吸收”或“放出”)
(4)反应____(填字母)能设计成原电池,请画出实验装置图,注明电极材料和电解质溶液。__________

写出电极反应式及反应类型
正极反应式:_____________________,
反应类型:_______________________,
负极反应式:_____________________。
(5)上题所设计原电池中,向正极移动的离子为_______,电池工作一段时间后,电解质溶液质量减轻7.6g,正极增重的质量为_______。
-
在理论上不能用于设计成原电池的化学反应是( )
A.HCl + NaOH = NaCl + H2O B.2CH3OH + 3O2= 2CO2 + 4H2O
C.4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 D.2H2 + O2 = 2H2O
-
现有如下两个反应:
A. NaOH+HCl=NaCl+H2O B. 2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池:
A._________,B.__________(选择“能”或“不能”);
(2)如果可以,则写出正、负极材料及其电极反应式:
负极材料________,电极反应式_______________,
正极材料________,电极反应式_______________。
-
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑上述反应中能设计成原电池的是______。
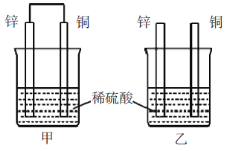
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
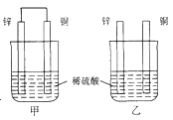
①下列说法正确的是____________。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______乙(填“>”、“<“或“=” )
③请写出图中构成原电池的负极电极反应式_________________________。
④当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为____________________。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入_____________极(填a或b),电子从 __________(填a或b)极流出。
-
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Zn+H2SO4=ZnSO4+H2↑;B.NaOH+HCl=NaCl+H2O。能设计成原电池的反应是__________(填“A”或“B”)。
(2)将锌片和铜片按如图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是__________。
A.甲、乙均为化学能转变为电能的装置
B.甲中铜片质量减少、乙中锌片质量减少
C.两烧杯中溶液的c(H+)均减小
②在相同时间内,两烧杯中产生气泡的速度:甲__________乙(填“>”、“<”或“=”)。
③请写出图中构成原电池的正极电极反应式:__________。
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为__________。
-
(15分)现有如下两个反应:(A)NaOH + HCl = NaCl + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)________(B)________。
(2)如果(A或B)不能,说明其原因________。
(3)如果(A或B)可以,则写出正、负极材料及其电极反应式,电解质溶液
负极:________;________。
正极:________;________。
电解质溶液:________。





