-
常温下,已知:1molCH4完全燃烧时放出890kJ的热量,1molH2完全燃烧时放出280kJ的热量。现有CH4和H2组成的混合气体共0.4mol,使其在O2中完全燃烧,恢复至常温共放出234kJ的热量,则CH4与H2的物质的量之比是( )
A.1:2 B.1:1 C.3:2 D.2:3
高二化学单选题中等难度题查看答案及解析
-
已知:101 kPa时,1molH2完全燃烧生成液态水,放出285.8 kJ的热量;1molCH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列能表示燃烧热的热化学方程式是
A.CH4(g)+2O2(g)
CO2(g)+2H2O(l) ΔH=−890.3 kJ
B.CH4(g)+2O2(g)
CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol−1
C.CH4(g)+2O2(g)
CO2(g)+2H2O(g) ΔH=−890.3 kJ·mol−1
D.H2(g)+
O2(g)
H2O(l) ΔH=−285.8 kJ·mol−1
高二化学单选题简单题查看答案及解析
-
(16分)(1)在298K时,1molCH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.0 kJ。写出该反应的热化学方程式 。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,并放出515kJ热量,则CH4的物质的量为 。
(2)利用该反应设计一个燃料电池:用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入甲烷和氧气。通入甲烷气体的电极应为 极(填写“正”或“负”),该电极上发生的电极反应式为 。
(3)在下图所示实验装置中总反应的方程式为 ;
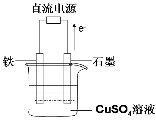
如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 ;
若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 。
高二化学填空题中等难度题查看答案及解析
-
(10分)已知1mol CO气体完全燃烧生成CO2气体,放出283kJ热量,1mol氢气完全燃烧生成液态水放出286kJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890kJ热量,
(1)写出H2完全燃烧生成液态水的热化学方程式________________________________;
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量_______890kJ(填“ =”、“>”、“<”)
(3)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)
的取值范围是______________________________________;
(4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物
质的量相等,则放出热量(Q)的取值范围是________________________________。
高二化学填空题简单题查看答案及解析
-
已知1mol CO气体完全燃烧生成CO2气体放出283KJ热量;1mol H2完全燃烧生成液态水放出286KJ热量;1mol CH4气体完全燃烧生成CO2气体和液态水放出890KJ热量.
(1)若1mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量______890KJ.
(填“>”、“<”或“=”)
(2)若将n mol CH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)的取值范围是______.
(3)若将a mol CH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,且CO2气体和水的物质的量相等时,则放出热量(Q)的取值范围是______.高二化学解答题中等难度题查看答案及解析
-
(8分)已知1mol CO气体完全燃烧生成CO2气体,放出283KJ热量,1mol氢气完全燃烧生成液态水放出286KJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890KJ热
(1)写出H2燃烧热的热化学方程式________。
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量________890KJ(填“=”、“>”“<”)
(3)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)的取值范围是________。
(4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物质的量相等,则放出热量(Q)的取值范围是________。
高二化学填空题简单题查看答案及解析
-
已知:101 Ka时,1mol H2完全燃烧生成液态水,放出285.8kJ的热量;1mol CH4完全燃烧生成液态水和CO2,放出890.3kJ的热量。下列热化学方程式的书写正确的是( )
①CH4(g)+ 2O2(g) = CO2(g) +2H2O(l) ΔH = + 890.3 kJ/mol
②CH4(g)+ 2O2(g) = CO2(g) +2H2O(l) ΔH = - 890.3 kJ/mol
③CH4(g)+ 2O2(g) = CO2(g) +2H2O(g) ΔH = - 890.3 kJ/mol
④2H2(g)+ O2(g) = 2H2O(l) ΔH = - 571.6 kJ/mol
A.仅有② B.仅有②④ C.仅有②③④ D.全部
高二化学单选题简单题查看答案及解析
-
已知1 mol CH4气体完全燃烧生成气态CO2和液态H2O,放出890.3 kJ热量,则表示该反应的热化学方程式正确的是
A. CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=+890.3 kJ·molˉ1
B. CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·molˉ1
C. CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890.3 kJ·molˉ1
D. CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·molˉ1
高二化学单选题简单题查看答案及解析
-
已知CH4(g)+2O2(g)= CO2(g)+2H2O(l); △H=-890kJ/mol。当一定量的CH4 (g) 完全燃烧生成CO2(g)和H2O(l) 所放出的热量为74kJ时,所需要空气在标况下的体积约为(空气中N2:O2体积比为4:1计) ( )
A.37.24L B.18.62L C.9.3L D.20.50L
高二化学单选题中等难度题查看答案及解析
-
1 mol CH4气体完全燃烧放出的热量为890 kJ,但当不完全燃烧生成CO和H2O(l)时,放出的热量为607 kJ,如果1 mol CH4与一定量O2燃烧生成CO、CO2、H2O,并放出819.25 kJ的热量,则一定量O2的质量为 ( )
A.40 g B.56 g
C.60 g D.无法计算
高二化学选择题简单题查看答案及解析