-
下列关于粒子结构的描述不正确的是( )
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含一个极性键的18电子粒子
C.CH2C12和CCl4均是四面体构型的非极性分子
D.1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值)高二化学选择题中等难度题查看答案及解析
-
下列关于粒子结构的描述不正确的是
A.H2S和NH3均是价电子总数为8的极性分子,且H2S分子的键角较大
B.HS﹣和HCl均是含一个极性键的18电子微粒
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值)
高二化学多选题中等难度题查看答案及解析
-
下列关于粒子结构的描述不正确的是
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含一个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.1 mol DO中含中子、质子、电子各10 NA(NA为阿伏加德罗常数)
高二化学选择题中等难度题查看答案及解析
-
下列关于粒子结构的描述不正确的是
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含一个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.SO2和SO3杂化轨道类型均为sp2杂化,立体构型分别为V形、平面三角形
高二化学单选题中等难度题查看答案及解析
-
下列关于粒子结构的描述不正确的是
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含1个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.SO2和SO3的杂化轨道类型均为sp2,空间构型分别为V形、平面三角形
答
高二化学单选题中等难度题查看答案及解析
-
下列关于粒子结构的描述不正确的是
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含1个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.SO2和SO3的杂化轨道类型均为sp2,空间构型分别为V形、平面三角形
答
高二化学选择题中等难度题查看答案及解析
-
关于下列粒子的描述不正确的是( )
A. PH3的电子式为
,其热稳定性不如NH3
B. HS-的电子式为
,是含有极性键的18电子的粒子
C. CH2Cl2的电子式为
,是结构呈正四面体的分子
D. KF的电子式为
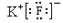 ,它是易溶于水的离子化合物
,它是易溶于水的离子化合物高二化学单选题中等难度题查看答案及解析
-
下列说法中正确的是
A.分子中键能越大,键长越长,则分子越稳定
B.HS- 和HCl均是含有一个极性键的18电子粒子
C.离子化合物的熔点一定比共价化合物的高
D.根据等电子原理,CH4和NH3具有相似的化学键特征,物理性质相近。
高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是 ( )
A.原子和其它原子形成共价键时,其共价键数一定等于该原子的价电子数
B.HS- 和HCl均是含有一个极性键的18电子粒子
C.铵根离子呈正四面体结构
D.离子化合物中只有离子键,共价化合物中只有共价键
高二化学选择题简单题查看答案及解析
-
下面关于氢化物的叙述正确的是
A.一个D216O分子所含的中子数为8 B.NH3的结构式为
C.HCl的电子式为
D.热稳定性:H2S>HF
高二化学选择题中等难度题查看答案及解析