-
(1)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得),若1 mol水蒸气转化为液态水放出的热量为45kJ,则反应H2(g) + O2(g) = H2O( l )的ΔH =________________kJ/mol。
O2(g) = H2O( l )的ΔH =________________kJ/mol。
(2)下图为氢氧燃料电池的结构示意图,当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
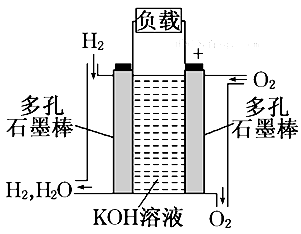
①图中通过负载的电子流动方向_______ (填“向左”或“向右”). 负极发生_____________反应;
②写出氢氧燃料电池工作时电极反应式负极:________________________________,正极:___________________________。
-
已知在101 kPa下,1 g氢气在氧气中完全燃烧生成气态水时,放出热量120.9 kJ.则下列说法中正确的是( )
A.氢气的燃烧热为241.8 kJ/mol
B.1 mol H2O(l)具有的能量大于1 mol H2O(g)具有的能量
C.反应的热化学方程式为:2H2(g)+O2(g)===2H2O(g);ΔH=+483.6 kJ/mol
D.2 mol H2(g)和1 mol O2(g)具有的能量总和大于2 mol H2O(g)具有的能量
-
用编号填空:
(1)下列关于燃烧热的说法正确的是
A.101kPa时1mol氢气完全燃烧生成水蒸气所放出的热量即氢气的燃烧热;
B.101kPa时1mol碳在氧气中燃烧生成CO所放出的热量即碳的燃烧热;
C.某物质的燃烧热不随热化学方程式计量数的改变而改变。
(2)下列关于用稀盐酸和氢氧化钠稀溶液测中和热的说法错误的是
A.实验结果随反应物用量改变而改变;
B.实验中氢氧化钠溶液稍过量是为了使盐酸完全被氢氧化钠中和;
C.实验中不可用环形铜质搅拌棒代替环形玻璃搅拌棒。
(3)下列关于化学平衡的说法错误的是
A.若改变影响化学平衡的条件之一,平衡向能够使这种改变减弱的方向移动;
B.达到化学平衡时,各组分的浓度不再改变,反应停止;
C.化学平衡移动,化学平衡常数不一定改变。
(4)改变下列条件,化学平衡一定向正反应方向移动的是
A.增大反应物浓度 B.升高温度 C.增大压强
(5)下列关于电解质的说法错误的是
A.酸、碱、盐及氧化物都是电解质;
B.电解质溶液能导电是因为发生了电离,产生了自由移动的离子;
C.电解质不一定能导电,能导电的物质不一定是电解质。
(6)下列反应的△H<0的是
A.铝和稀硫酸反应 B.碳酸氢铵受热分解 C.氢氧化钡晶体与氯化铵晶体反应
(7)下列情况,均为日常生活中为了改变反应速率而采取的措施,其中不属于浓度影响反应速率的是
A.汽车加大油门 B.食物放冰箱 C.糕点包装袋里放小包除氧剂
(8)下列实验现象与实际不符的是
A.向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色;
B.浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊;
C.将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅。
(9)一定温度下,有三种酸:A.盐酸,B.硫酸,C.醋酸,回答下列问题:
①三种酸溶液等物质的量浓度时,c(H+)最大的是 ;
②三种酸的c(H+)相同时,溶液浓度最大的是 ;
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,再加入同样的锌粒,反应最快的是 。
-
已知氢气和氧气反应生成1mol水蒸气时可以放出241.8kJ的热量,1g水蒸气转化为液态水放热2.444kJ。写出表示H2燃烧热的热化学方程式 。
-
由氢气和氧气反应生成1 mol水蒸气放出241.8 kJ的热量,1 g水蒸气转化为液态水放出2.45 kJ的热量,则下列热化学方程式书写正确的是( )
A. H2(g)+1/2O2(g)===H2O(l) ΔH=-285.9 kJ·mol-1
B. H2(g)+1/2O2(g)===H2O(l) ΔH=-241.8 kJ·mol-1
C. H2(g)+1/2O2(g)===H2O(l) ΔH=+285.9 kJ·mol-1
D. H2(g)+1/2O2(g)===H2O(g) ΔH=+241.8 kJ·mol-1
-
由氢气和氧气反应生成1 mol水蒸气放出241.8 kJ的热量,1 g水蒸气转化为液态水放出2.45 kJ的热量,则下列热化学方程式书写正确的是( )
A.H2(g)+1/2O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1
B.H2(g)+1/2O2(g)=H2O(l) ΔH=-241.8 kJ·mol-1
C.H2(g)+1/2O2(g)=H2O(l) ΔH=+285.9 kJ·mol-1
D.H2(g)+1/2O2(g)=H2O(g) ΔH=+241.8 kJ·mol-1
-
已知由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量。
(1)写出该反应的热化学方程式_______________________________________。
(2)若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+1/2O2(g)=H2O(l)的ΔH=______kJ·mol-1。
-
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。反应时释放大量热并快速产生大量气体。已知在101kPa,298K时,1mol液态N2H4在氧气中完全燃烧生成N2和水蒸气,放出热量624kJ,该反应的热化学方程式是___________ 。又知:H2O(g )=H2O (l)△H=-44 kJ·mol-1,若1mol液态N2H4在氧气中完全燃烧生成N2和液态水,则放出热量为__________________kJ。
(2)已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要能量是436KJ、391KJ、946KJ,则N2与H2反应生成NH3的热化学方程式是__________________。
-
已知在101KPa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
A. H2O(g)=H2(g)+1/2O2;△H(298K)=-242kJ·mol-1
B. H2(g)+1/2O2(g)=H2O(1);△H(298K)=+484kJ·mol-1
C. H2(g)+1/2O2(g)=H2O(g);△H(298K)=-242kJ·mol-1
D. H2(g)+1/2O2(g)=H2O(g);△H(298K)=-484kJ·mol-1
-
已知在101kPa,25℃条件下,1mol氢气燃烧生成水蒸气放出242kJ热量,下列热化学方程式正确的是
A.H2(g)+  O2(g)=H2O(g) ΔH=+242kJ•mol-1
O2(g)=H2O(g) ΔH=+242kJ•mol-1
B.2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ•mol-1
C.H2(g)+  O2(g)=H2O(l) ΔH=-242kJ•mol-1
O2(g)=H2O(l) ΔH=-242kJ•mol-1
D.2H2(g)+O2(g)=2H2O(g) ΔH=-242kJ•mol-1
O2(g) = H2O( l )的ΔH =________________kJ/mol。
