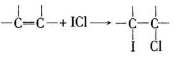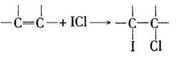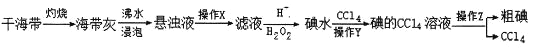-
已知:ICl的熔点为13.9℃,沸点为97.4℃,易水解,且能发生反应:ICl(l) + Cl2(g) == ICl3(l)。(图中夹持装置略去)

(1)装置A中发生反应的化学方程式是 。
(2)装置B的作用是 。不能用装置F代替装置E,理由 。
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是 (填标号)。
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。进行如下两个实验,实验过程中有关反应为:
①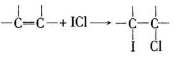
②ICl+KI=I2+KCl ③I2+2Na2S2O3=2NaI+Na2S4O6
实验1:将5.00g该油脂样品溶于四氯化碳后形成100mL溶液,从中取出十分之一,加入20mL某ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用a mol/L的Na2S2O3 标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
①滴定过程中可用 作指示剂。
②滴定过程中需要不断振荡,否则会导致V1 (填“偏大”或“偏小)。
③5.00g该油脂样品所消耗的ICl的物质的量为 mol。由此数据经换算即可求得该油脂的不饱和度。
-
已知:ICl的熔点为13.9℃,沸点为97.4℃,易水解,且能发生反应:ICl(l) + Cl2(g) == ICl3(l)。(图中夹持装置略去)

(1)装置A中发生反应的化学方程式是 。
(2)装置B的作用是 。不能用装置F代替装置E,理由 。
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是 (填标号)。
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。进行如下两个实验,实验过程中有关反应为:
①
②ICl+KI=I2+KCl ③I2+2Na2S2O3=2NaI+Na2S4O6
实验1:将5.00g该油脂样品溶于四氯化碳后形成100mL溶液,从中取出十分之一,加入20mL某ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用a mol/L的Na2S2O3 标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
①滴定过程中可用 作指示剂。
②滴定过程中需要不断振荡,否则会导致V1 (填“偏大”或“偏小)。
③5.00g该油脂样品所消耗的ICl的物质的量为 mol。由此数据经换算即可求得该油脂的不饱和度。
-
已知:ICl的熔点为13.9℃,沸点为97.4℃,易水解,且能发生反应:ICl(l)+Cl2(g)=ICl3(l)

(1)装置A中发生反应的化学方程式是________________________________;
(2)装置B的作用是___________________,不能用装置F代替装置E,理由_______________________;
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是___________(填标号);
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度.进行如下两个实验,实验过程中有关反应为:
①
②ICl+KI═I2+KCl
③I2+2Na2S2O3═2NaI+Na2S4O6
实验1:将5.00g该油脂样品溶于四氯化碳后形成100mL溶液,从中取出十分之一,加人20mL某ICl的冰醋酸溶液(过量),充分反应后,加人足量KI溶液,生成的碘单质用a mol•L-1的Na2S2O3标准溶液滴定.经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL.
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL.
①滴定过程中可用___________作指示剂.
②滴定过程中需要不断振荡,否则会导致V1_________(填“偏大”或“偏小).
③5.00g该油脂样品所消耗的ICl的物质的量为___________mol,由此数据经换算即可求得该油脂的不饱和度。
-
利用反应I2(s)+Cl2(g)=2ICl(l),实验室可用如下图所示装置(加热、夹持仪器已略去)制取少量IC1。
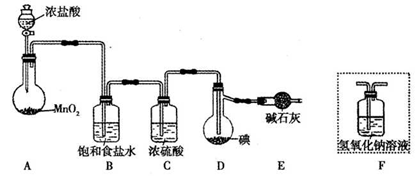
已知:ICl的熔点为13.9℃,沸点为97.4℃,易水解,且能发生反应:
ICl(l)+Cl2(g)=2ICl3(l)
(1)装置A中发生反应的化学方程式是____________。
(2)装置B的作用是______。不能用装置F代替装置E,理由是____________。
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是______ (填标号)。
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。进行如下两个实验,实验过程中有关反应为:
i.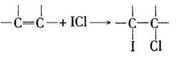
ii.ICl+KI=I2+KCl
iii.I2+2Na2S2O3=2NaI+Na2S4O6
实验1:将0.500g该油脂样品溶于10mL四氯化碳后,加人20mL某ICl的冰醋酸溶液(过量),充分反应后,加人足量KI溶液,生成的碘单质用a mol•L—1的Na2S2O3,标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
①滴定过程中可用______作指示剂。
②滴定过程中需要不断振荡,否则会导致V1______(填“偏大”或“偏小”)。
③0.500g该油脂样品所消耗的ICl的物质的量为______mol。由此数据经换算即可求得该油脂的不饱和度。
-
已知:ICl的熔点为13.90C,沸点为97.40C,易水解,且能发生反应:ICl(l)+ Cl2(g)=ICl3(l)

(1)装置A中发生反应的化学方程式是____________ 。
(2)装置B的作用是______。不能用装置F代替装置E,理由____________ 。
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是______ (填标号)。
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。进行如下两个实验,实验过程中有关反应为:
①
②ICl+KI=I2+KCl
③I2+2Na2S2O3=2NaI+Na2S4O6
实验1:将5.00g该油脂样品溶于四氯化碳后形成100mL溶液,从中取出十分之一,加人20mL某ICl的冰醋酸溶液(过量),充分反应后,加人足量KI溶液,生成的碘单质用a mol.L-1的Na2S2O3 标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
①滴定过程中可用______ 作指示剂。
②滴定过程中需要不断振荡,否则会导致V1______ (填“偏大”或“偏小)。
③5.00g该油脂样品所消耗的ICl的物质的量为__ mol。由此数据经换算即可求得该油脂的不饱和度。
-
ICl的冰醋酸溶液可用于测定油脂的不饱和溶液,其原理为 +ICl
+ICl
 。ICl制备装置图如下,(夹持装置及加热仪器已省略);
。ICl制备装置图如下,(夹持装置及加热仪器已省略);
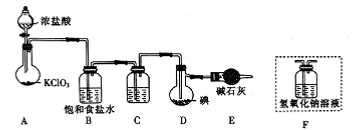
已知:ICl的熔点为27℃,沸点为97.4℃,易水解,且能发生反应ICl(1)+Cl2(g)=ICl3(1)。
(1)盛装浓盐酸的仪器名称是________;装置C中的试剂名称是________。
(2)装置B的作用是_________;不能用装置F代替装置E,理由是________。
(3)用ICl的冰醋酸溶液测定某油脂(M=880)的不饱和度。进行如下两个实验。
实验1:将4.40g该油渍样品溶于四氯化碳后形成l00mL溶液,从中取出十分之一,加入20mL某浓度的ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用1.00mol/L的Na2S2O3标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其他操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
① 滴定过程中可用_________作指示剂。
② 滴定过程中需要不断振荡,否则会导致V1_______(填“偏大”或“偏小”)。
③ 若V1=15.00mL,V2=20.00mL,则该油脂的不饱和度为___________。
-
卤素互化物如ICl、ICl3等具有与卤素单质相似的性质。利用反应I2+Cl2=2ICl,实验室可用如图所示装置(夹持仪器已略去)制取少量ICl3。已知:ICl的熔点为27.2℃,沸点为97.40C,容易水解,能发生反应:ICI+C12=IC13。下列叙述错误的是( )
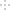
A.圆底烧瓶中的固体可以为KMnO4或KClO3
B.装置B、C中的试剂分别为饱和食盐水和浓硫酸
C.装置E的作用为吸收尾气,可用装置F替代
D.盐酸的滴加速度过快,ICl的产率会明显降低
-
三氯化碘(IC13)在药物合成中用途非常广泛。已知ICl3熔点33℃,沸点73℃,有吸湿性,遇水易水解。某小组同学用下列装置制取ICl3(部分夹持和加热装置省略)。

(1)按照气流方向连接接口顺序为a→__________________________________________。装置A中导管m的作用是____________________________________________。
(2)装置C用于除杂,同时作为安全瓶,能监测实验进行时后续装置是否发生堵塞,若发生堵塞C中的现象为____________________________________________________。
(3)氯气与单质碘需在温度稍低于70℃下反应,则装置E适宜的加热方式为____________。装置E中发生反应的化学方程式为_________________________________________。
(4)该装置存在的明显缺陷是_____________________________________。
(5)粗碘的制备流程为:

操作Y用到的玻璃仪器有烧杯、____________,操作Z的名称为__________。
-
三氯化碘(IC13)在药物合成中用途非常广泛。已知ICl3熔点33℃,沸点73℃,有吸湿性,遇水易水解。某小组同学用下列装置制取ICl3(部分夹持和加热装置省略)。
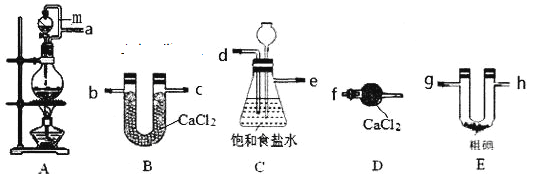
(1)按照气流方向连接接口顺序为a→__________________________________________。装置A中导管m的作用是____________________________________________。
(2)装置C用于除杂,同时作为安全瓶,能监测实验进行时后续装置是否发生堵塞,若发生堵塞C中的现象为____________________________________________________。
(3)氯气与单质碘需在温度稍低于70℃下反应,则装置E适宜的加热方式为____________。装置E中发生反应的化学方程式为_________________________________________。
(4)该装置存在的明显缺陷是_____________________________________。
(5)粗碘的制备流程为:
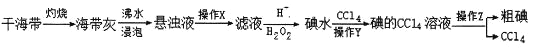
操作Y用到的玻璃仪器有烧杯、____________,操作Z的名称为__________。
-
三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点为33℃,沸点为73℃,氯气与单质碘需在温度稍低于70℃下反应制备ICl3。实验室可用如图装置制取ICl3。下列说法正确的是( )
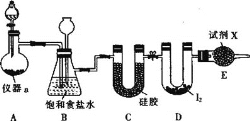
A.装置A可选用的药品为二氧化锰与浓盐酸
B.装置B的作用是除杂,也作安全瓶,能监测实验进行时装置C中是否发生堵塞
C.装置C中的硅胶可用碱石灰代替
D.装置D最恰当的加热方式为酒精灯直接加热