-
卤族元素单质具有相似的化学性质,这主要是由于卤素( )
A.单质均为双原子分子 B.均为非金属元素
C.原子最外层电子数相同,均为7个 D.原子核外电子层数依次增大
高二化学选择题简单题查看答案及解析
-
在1981年才第一次制得卤族元素的第五个成员砹,根据卤素性质的变化规律,我们可以预料砹的下列性质不正确的是( )
A.砹单质在室温下的状态是固体,颜色比碘深,单质能溶于四氯化碳
B.砹原子得电子能力比碘强
C.AgAt的颜色比AgI 深,HAt的稳定性比HI弱
D.单质砹是卤素中弱氧化剂,而砹离子是卤族中的强还原剂
高二化学单选题中等难度题查看答案及解析
-
卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX’型卤素互化物与卤素单质结构相似、性质相近。右图是部分卤素单质和XX’型卤素互化物的沸点与其相对分子质量的关系图。试推测ICl的沸点所处的范围
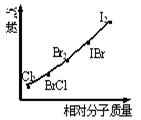
A.Cl2和BrCl之间 B.Br2和IBr之间 C.IBr和I2之间 D.BrCl和Br2之间
高二化学选择题中等难度题查看答案及解析
-
阅读下列短文:不同的卤素之间可以相互结合形成一系列的化合物。这类化合物称为卤素互化物。卤素互化物具有很高的化学活性,它们有许多化学性质跟卤素单质相似,例如:能跟大多数金属起反应生成相应的卤化物,也能跟某些非金属单质起反应生成相应的卤化物。溴化碘(IBr)是卤素互化物的一种。这种化合物在常温下是深红色的固体,熔点为41℃,沸点为116℃。下列对IBr的各种描述中,不正确的是
A.在很多化学反应中,溴化碘是一种氧化剂
B.固体溴化碘是一种原子晶体
C.与水能反应:IBr + H2O=HBr+HIO
D.在Fe3+的催化下可与苯反应生成
和HBr
高二化学选择题困难题查看答案及解析
-
卤族元素是典型的非金属元素,其单质及其化合物具有广泛的用途。已知:KMnO4与浓盐酸常温下反应可生成氯气。根据所学化学知识及所给信息,回答下列有关问题:
(1)下列可以用来判断氯、溴、碘元素非金属性强弱的是 (填序号)。
①HCl、HBr、HI的热稳定性逐渐减弱;
②AgCl、AgBr、AgI的颜色逐渐加深;
③ HCl、HBr、HI的酸性依次减弱;
④ Cl2、Br2、I2的颜色逐渐加深;
⑤ Cl2、Br2、I2和H2反应条件由光照(或点燃)→ 一定温度→ 持续加热;条件由易到难;
⑥Cl2、Br2、I2的氧化性逐渐减弱。
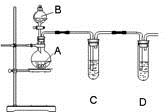
(2)某化学探究小组选用右图所示的装置和下列所给的试剂来证明非金属性:Cl>I,请你按照他们的设计思路完成该实验。
可供选择的试剂有:①浓盐酸,②硝酸银溶液,③KMnO4,④稀盐酸,⑤淀粉碘化钾溶液, ⑥MnO2, ⑦NaOH溶液;⑧浓硫酸
烧瓶A中应盛放的药品是 (填序号),试管C中应盛放的药品是 (填序号),则装置D的作用是 。观察到 现象,即可证明非金属性Cl>I。
(3)一定条件,在水溶液中1 mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示。
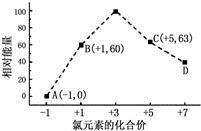
①D是 (填离子符号)。
②B→A+C反应的离子方程式为 ;生成1molC时, KJ的热(填吸收或放出以及具体数值)
高二化学简答题困难题查看答案及解析
-
(15分)卤族元素的单质和化合物很多,请用物质结构与性质的相关知识回答:
(1)在一定浓度的氢氟酸溶液中,存在(HF)n缔合分子,使HF分子缔合的作用力是___。
(2)ClO4-中心氯原子的杂化方式为_____,离子的立体构型为__________。
(3)已知碘酸(HIO3)和高碘酸(H5IO6)的分子结构分别如图I、II所示:请比较酸性强弱:HIO3_____H5IO6(填“>”、“<”或“=”)。H5IO6分子中σ键与π键的个数比为 。
(4)下图为碘晶体晶胞结构。有关说法中正确的是___。
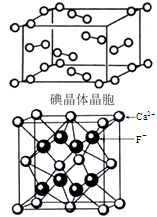
A.用均摊法可知平均每个晶胞中有4个碘原子
B.碘晶体中分子的配位数为12,具有分子密堆积特征
C.碘晶体中存在的相互作用有非极性键和范德华力
D.碘晶体中碘分子有3种排列方向
(5)观察CaF2晶胞结构,判断F-占据Ca2+ 形成的 面体空隙中,Ca2+ 占据F-形成的 面体空隙中。若相邻两个Ca2+ 的核间距为a cm,晶胞密度为ρ g/cm3,NA为阿伏加德罗常数,则CaF2的摩尔质量可以表示为________ g/mol。
高二化学填空题极难题查看答案及解析
-
砹是原子序数最大的卤族元素,推测砹或砹的化合物最不可能具有的性质是( )
①砹化氢很稳定
②砹单质与水反应,使砹全部转化成氢砹酸和次砹酸
③砹是黑色固体
④砹化银难溶于水
⑤砹易溶于某些有机溶剂.
A. 只有①② B. 只有①②⑤ C. 只有③⑤ D. 只有②⑤
高二化学选择题中等难度题查看答案及解析
-
下列说法不正确的是( )
A. 根据对角线规则,镁元素和锂元素的性质具有相似性
B. 一般来说,共价键键长越短,键能越大
C. 气体单质分子中,一定有σ键,可能有π键
D. 金属焰色反应原理是激发态的电子从能量较高的轨道跃迁到能量较低的轨道时, 以一定波长(可见光区域)光的形式释放能量
高二化学选择题中等难度题查看答案及解析
-
溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的产物与氯气与水反应的产物相似。下列有关IBr的叙述中,不正确的是( )
A.IBr是双原子分子
B.在很多反应中,IBr是强氧化剂
C.和NaOH溶液反应生成NaBr和NaIO
D.和水反应时,既是氧化剂又是还原剂
高二化学单选题简单题查看答案及解析
-
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为 。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为 。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于 。
(4)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为 ,中心原子杂化类型为 。
(5)①HClO4、②HIO4、③H5IO6〔可写成(HO)5IO〕的酸性由强到弱的顺序为 (填序号)。
(6)IBr和水能发生反应,生成物中有一种为三原子分子,写出该化合物的结构式 。
高二化学填空题中等难度题查看答案及解析