-
(10分)某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
编号
电极材料
电解质溶液
电流计指针偏转方向
1
Mg、Al
稀盐酸
偏向Al
2
Al、Cu
稀盐酸
偏向Cu
3
Al、C(石墨)
稀盐酸
偏向石墨
4
Mg、Al
氢氧化钠溶液
偏向Mg
5
Al、Zn
浓硝酸
偏向Al
试根据表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)是否相同(填“相同”或“不相同”)________。
(2)对实验3完成下列填空:
①铝为________极,电极反应式:______________________________。
②石墨为________极,电极反应式:___________________________。
③电池总反应式:______________________________________。
(3)实验4中铝作负极还是正极________,理由是__________________________
写出铝电极的电极反应式_________________________________。
(4)解释实验5中电流计指针偏向铝的原因:_____________________________。
高三化学填空题简单题查看答案及解析
-
某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据表中的实验现象回答下列问题:编号 电极材料 电解质溶液 电流计指针偏转方向 1 Mg、Al 稀盐酸 偏向Al 2 Al、Cu 稀盐酸 偏向Cu 3 Al、C(石墨) 稀盐酸 偏向石墨 4 Mg、Al 氢氧化钠溶液 偏向Mg 5 Al、Zn 浓硝酸 偏向Al
(1)实验1、2中Al所作的电极(正极或负极)是否相同(填“相同”或“不相同”)______.
(2)对实验3完成下列填空:
①铝为______极,电极反应式:______.
②石墨为______极,电极反应式:______.
③电池总反应式:______.
(3)实验4中铝作负极还是正极______,理由是______.写出铝电极的电极反应式______.
(4)解释实验5中电流计指针偏向铝的原因:______.高三化学解答题中等难度题查看答案及解析
-
某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
编号
电极材料
电解质溶液
电流计指针偏转方向
①
Mg 、Al
稀盐酸
偏向Al
②
Al、Cu
稀盐酸
偏向Cu
③
Al、石墨
稀盐酸
偏向石墨
④
Mg、Al
NaOH溶液
偏向Mg
⑤
Al、Zn
浓硝酸
偏向Al
根据上表中的实验现象完成下列问题:
(1)实验①、②中Al所作的电极是否相同?
答:____________________________________________
(2)写出实验③中的电极名称、电极反应式和电池总反应方程式。铝为( )______________________________
石墨为( )__________________________
电池总反应:__________________________
(3)实验④中的铝作________极。
(4)实验⑤中铝作________极。
高三化学填空题中等难度题查看答案及解析
-
某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
编号
电极材料
电解质溶液
电流计指针偏转方向
1
Mg Al
稀盐酸
偏向Al
2
Al Cu
稀盐酸
偏向Cu
3
Al 石墨
稀盐酸
偏向石墨
4
Mg Al
NaOH溶液
偏向Mg
5
Al Zn
浓硝酸
偏向Al
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同?
________________________________________________________________________。
(2)指出铝和石墨的电极并写出实验3中的电极反应式和电池总反应方程式。
铝为( ):
________________________________________________________________________。
石墨为( ):
________________________________________________________________________。
电池总反应:
________________________________________________________________________。
(3)实验4中的铝作正极还是负极?________,为什么?
________________________________________________________________________
________________________________________________________________________。
(4)解释实验5中电流计指针偏向铝的原因:
________________________________________________________________________
________________________________________________________________________。
(5)根据实验结果总结:在原电池中金属铝作正极还是负极受到哪些因素的影响?________________________________________________________________________
________________________________________________________________________。
高三化学填空题简单题查看答案及解析
-
某化学兴趣小组能探究发现水果汁中存在电解质,可以设计成如图所示的水果原电池。随后又进一步思考原电池工作效率和其构成要素之间的一些关系如下表所示。
实验次数
电极材料
水果品种
电极间距/cm
电压/mV
1
锌
铜
菠萝
3
900
2
锌
铜
苹果
3
650
3
锌
铜
西红柿
3
750
4
锌
铝
菠萝
3
650
5
锌
铝
苹果
3
450
6
锌
铝
苹果
2
550
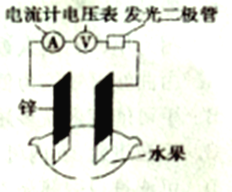
由表中数据可知,下列说法不正确的是
A. 实验1、4电流方向应该相反
B. 电极及其间距相同时,电压大小只与水果种类有关,与其他因素无关
C. 如果用锌、碳棒作电极,实验1中电压可能大于900mV
D. 实验中发光二极管不太亮,可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来
高三化学单选题中等难度题查看答案及解析
-
Ⅰ、某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图1为某实验小组设计的原电池
装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。
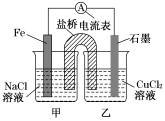
(2)如图,其他条件不变,若将乙烧杯中的CuCl2溶液换为NH4Cl溶液,则石墨电极的电极反应方程式为_____________________

(3)如图,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如下图所示乙装置中与铜丝相连的石墨电极上发生的反应方程式为_____________________
Ⅱ、氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油等燃料相比,氢气作为燃料的两个明显的优点是________________(写两点)
(2)化工生产的副产品也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气。总反应方程式为:Fe+2H2O+2OH−
FeO42−+3H2↑,工作原理如下图1所示。装置通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。

①电解一段时间后,c(OH−)降低的区域在________________(填“阴极室”或“阳极室”)
②电解过程中,须将阴极产生的气体及时排出,其原因是______________________
③c( Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_____________。
高三化学填空题简单题查看答案及解析
-
某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据的氧化还原反应:(用离子方程式表示)___________。
设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。
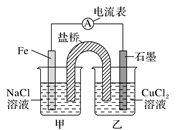
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为_________________________________________________,这是由于NH4Cl溶液显______(填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的原因_____________________________________,用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式_____________________________________________,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO
,试写出该反应的离子方程式_______________________________________________。
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,
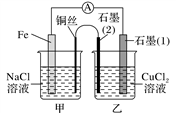
一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是________________,电极反应为________;乙装置中石墨(1)为________极(填“正”“负”“阴”或“阳”),乙装置中与铜丝相连石墨(2)电极上发生的反应式为________________________,产物常用________检验,反应的离子方程式为__________________________________________________________________。
高三化学简答题困难题查看答案及解析
-
某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应_______________(用离子方程式表示)设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差 12 g,导线中通过__________mol 电子。
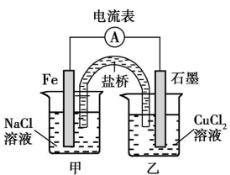
(2)其他条件不变,若将 CuCl2溶液换为 NH4Cl 溶液,石墨电极发生的电极反应为___________,这是由于 NH4Cl 溶液显_______________(填“酸性”、“碱性” 或“中性”)。用吸管吸出铁片附近的溶液少许置于试管中,向其中滴加少量新制饱和氯水,然后滴加几滴 KSCN 溶液,溶液变红,继续滴加过量新制饱和氯水,溶液颜色褪去,同学们对此做了多种假设,某同学的假设:“溶液中的+3 价铁被氧化为更高价态。” 如果+3 价铁被氧化为 FeO42-,写出发生反应的离子方程式___________________。
(3)其他条件不变,若将盐桥换成弯铜导线与石墨连成的形装置如图所示,一段时间后,在甲装置铜丝附近滴加酚酞溶液,现象是____________,电极反应为__________;乙装置中石墨(Ⅰ)为__________(填“正”、 “ 负” 、 “ 阴”或“阳”)极。
高三化学填空题困难题查看答案及解析
-
关于电解池应用的规律提炼题组
某化学兴趣小组用下图所示装置进行电化学原理的实验探究,回答下列问题:
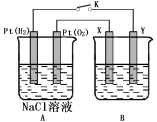
(1)通O2的Pt电极为电池 极(填电极名称),其电极反应式为 。
(2)若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为 ,电解质溶液为 。
(3)若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,在 电极(填“X”或“Y”)周围有固体沉积,该电极的电极反应式为 。
(4)若X、Y均为Pt,B电池的电解质溶液为500 mL 1.0mol/L的NaCl溶液,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变)。恢复到常温下,B电池溶液的pH= ,要使该溶液恢复到原来的状态,需加入 (填物质并注明物质的量)。
(5)若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为 。
(6)若X、Y均是Pt,电解质溶液为Na2SO4溶液,通电一段时间后,在阴极上逸出c mol气体,同时有N g Na2SO4•10H2O 晶体析出,若温度不变,此时剩余溶液的溶质的质量分数为 。
(学法题)通过以上题目,请总结书写电极反应式的关键 。
高三化学实验题困难题查看答案及解析
-
(12分)镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
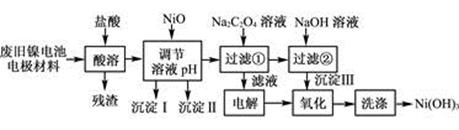
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O
③某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:
M(OH)n
Ksp
开始沉淀pH
沉淀完全pH
Al(OH)3
1.9×10-23
3.4
4.2
Fe(OH)3
3.8×10-38
2.5
2.9
Ni(OH)2
1.6×10-14
7.6
9.8
回答下列问题:
(1) 用NiO调节溶液的pH,依次析出沉淀Ⅰ________和沉淀Ⅱ__________(填化学式)。
(2) 写出加入Na2C2O4溶液的反应的化学方程式:
________。
(3) 检验电解滤液时阳极产生的气体的方法:
________
________。
(4) 写出“氧化”反应的离子方程式:
________。
(5) 如何检验Ni(OH)3已洗涤干净?
________
________。
高三化学填空题极难题查看答案及解析