在烧杯中加入一定量的枯草浸出液,烧杯中的枯草杆菌以其中的有机物为食。过几天后放入大草履虫,再过一段时间后,放入双小核草履虫,它们均以枯草杆菌为食。三种生物在浸出液中数量的增减情况如右图所示,据图分析错误的是 ( )
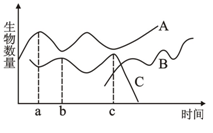
A.枯草杆菌和草履虫之间构成捕食关系,两种草履虫之间构成竞争关系
B.A、B两条曲线分别表示枯草杆菌和双小核草履虫的数量变化情况
C.烧杯内混合培养的每一种生物,均存在种内斗争
D.经过足够长的时间后,A、B两条曲线最终趋向动态平衡
高三化学选择题中等难度题
在烧杯中加入一定量的枯草浸出液,烧杯中的枯草杆菌以其中的有机物为食。过几天后放入大草履虫,再过一段时间后,放入双小核草履虫,它们均以枯草杆菌为食。三种生物在浸出液中数量的增减情况如右图所示,据图分析错误的是 ( )

A.枯草杆菌和草履虫之间构成捕食关系,两种草履虫之间构成竞争关系
B.A、B两条曲线分别表示枯草杆菌和双小核草履虫的数量变化情况
C.烧杯内混合培养的每一种生物,均存在种内斗争
D.经过足够长的时间后,A、B两条曲线最终趋向动态平衡
高三化学选择题中等难度题
在烧杯中加入一定量的枯草浸出液,烧杯中的枯草杆菌以其中的有机物为食。过几天后放入大草履虫,再过一段时间后,放入双小核草履虫,它们均以枯草杆菌为食。三种生物在浸出液中数量的增减情况如右图所示,据图分析错误的是 ( )

A.枯草杆菌和草履虫之间构成捕食关系,两种草履虫之间构成竞争关系
B.A、B两条曲线分别表示枯草杆菌和双小核草履虫的数量变化情况
C.烧杯内混合培养的每一种生物,均存在种内斗争
D.经过足够长的时间后,A、B两条曲线最终趋向动态平衡
高三化学选择题中等难度题查看答案及解析
高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为,含少量
等杂质元素)制备高纯碳酸锰的实验过程如下:其中除杂过程包括:①向浸出液中加入一定量的X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是( )已知室温下:
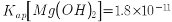 ,
,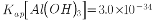 ,
,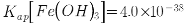 。)
。)
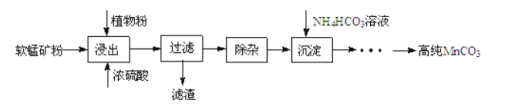
A.试剂X可以是等物质
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去等杂质
C.浸出时加入植物粉的作用是作为还原剂
D.为提高沉淀步骤的速率可以持续升高温度
高三化学单选题中等难度题查看答案及解析
| 实验方案 | 可能的现象和相应的结论 |
| ______ | ______ |
| ______ |
高三化学解答题中等难度题查看答案及解析
高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Kap[Mg(OH)2]=1.8×10-11,Kap[Al(OH)3]=3.0×10-34,Kap[Fe(OH)3]=4.0×10-38。)
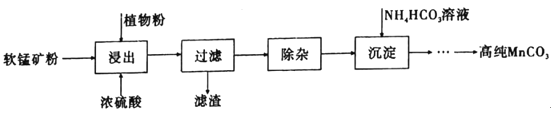
A.浸出时加入植物粉的作用是作为还原剂
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.试剂X可以是MnO、MnO2、MnCO3等物质
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
高三化学单选题中等难度题查看答案及解析
高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Kap[Mg(OH)2]=1.8×10-11,Kap[Al(OH)3]=3.0×10-34,Kap[Fe(OH)3]=4.0×10-38。)
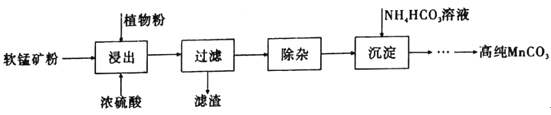
A.浸出时加入植物粉的作用是作为还原剂
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.试剂X可以是MnO、MnO2、MnCO3等物质
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
高三化学单选题中等难度题查看答案及解析
高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为MnO2,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下:其中除杂过程包括:①向浸出液中加入一定量的X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3.0×10-34,Ksp[Fe(OH)3]=4.0×10-38)
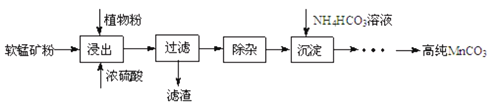
A.试剂X可以是MnO、MnO2、MnCO3等物质
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.浸出时加入植物粉的作用是作为还原剂
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
高三化学单选题中等难度题查看答案及解析
高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为MnO2,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下:其中除杂过程包括:①向浸出液中加入一定量的X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是( )
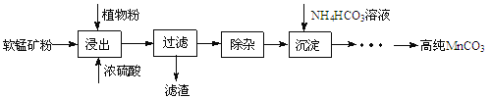
A.试剂X可以是MnO、MnO2、MnCO3等物质
B.浸出时加入植物粉的作用是作为还原剂
C.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
高三化学单选题困难题查看答案及解析
工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰。已知:菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。焙烧后的产物用浓盐酸酸浸,再对浸出液净化除杂,得到的净化液加入碳酸氢铵溶液生成沉淀,洗涤干燥后即可得到产品。回答:
(1)焙烧过程中产生两种气体,一种可使湿润的蓝色石蕊试纸变红,另一种可使湿润的红色石蕊试纸变蓝。请写出焙烧过程中主要反应的方程式______________。
(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,写出该反应的离子方程式______________________。检验Fe3+所用试剂的名称是__________。
(3)净化液加入碳酸氢铵溶液时反应的离子方程式为_____________________。
(4)上述生产过程中可循环使用的物质是________。
A.MnCO3 B. HCl C. NH4Cl D. 碳酸氢铵
(5)用滴定法测定浸出液中Mn2+的含量时,需向其中加入稍过量的磷酸和硝酸,加热会生成NO2-。加入稍过量的硫酸铵可以将其转化成无污染的物质而除去,该反应的离子方程式为________。
高三化学综合题中等难度题查看答案及解析
植物油厂想要提取大豆中丰富的油脂,下列方案设计合理的是( )
A.将大豆用水浸泡,使其中的油脂溶于水,然后再分馏
B.先将大豆压成颗粒状,再用无毒的有机溶剂浸泡,然后对浸出液进行蒸馏分离
C.将大豆用碱溶液处理,使其中的油脂溶解,然后再蒸发出来
D.将大豆粉碎,然后隔绝空气加热,使其中的油脂挥发出来
高三化学选择题简单题查看答案及解析
在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是 (填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是 (填化学式),反应的化学方程式为 。
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有 (填序号)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液 ,说明这种气体具有 性;将(2)中产生的有刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式: 。
(5)能否用澄清石灰水鉴别这两种气体? (填“能”或“不能”),若不能,请填写两种能鉴别的试剂 。
高三化学填空题中等难度题查看答案及解析