利用电导法测定某浓度醋酸电离的ΔH、Ka随温度变化曲线关系如图。已知整个电离过程包括氢键断裂、醋酸分子解离、离子水合。下列有关说法不正确的是
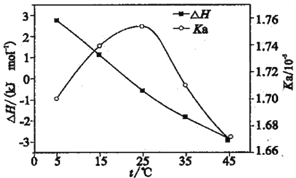
A. 理论上ΔH=0时,Ka最大
B. 25℃时,[CH3COOH]最大
C. 电离的热效应较小是因为分子解离吸收的能量与离子水合放出的能量相当
D. CH3COOH溶液中存在氢键是ΔH随温度升高而减小的主要原因
高三化学单选题困难题
利用电导法测定某浓度醋酸电离的ΔH、Ka随温度变化曲线关系如图。已知整个电离过程包括氢键断裂、醋酸分子解离、离子水合。下列有关说法不正确的是

A. 理论上ΔH=0时,Ka最大
B. 25℃时,[CH3COOH]最大
C. 电离的热效应较小是因为分子解离吸收的能量与离子水合放出的能量相当
D. CH3COOH溶液中存在氢键是ΔH随温度升高而减小的主要原因
高三化学单选题困难题
利用电导法测定某浓度醋酸电离的ΔH、Ka随温度变化曲线关系如图。已知整个电离过程包括氢键断裂、醋酸分子解离、离子水合。下列有关说法不正确的是

A. 理论上ΔH=0时,Ka最大
B. 25℃时,[CH3COOH]最大
C. 电离的热效应较小是因为分子解离吸收的能量与离子水合放出的能量相当
D. CH3COOH溶液中存在氢键是ΔH随温度升高而减小的主要原因
高三化学单选题困难题查看答案及解析
利用手持技术可测定酸碱滴定过程中溶液的电导率导电能力
和pH的变化,
时向
浓度均为
的盐酸和醋酸的混合溶液中逐滴加入
氨水,滴定过程中电导率和pH变化曲线如图所示,
已知
和
的电离平衡常数均为
。下列说法正确的是
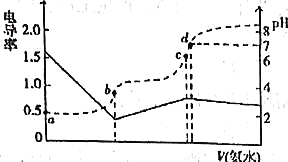
A.a点溶液中,
B.b点溶液中,主要溶质为和HCl
C.c点对应的氨水
D.d点溶液中,
高三化学单选题中等难度题查看答案及解析
室温下,将醋酸慢慢滴入到盛
蒸馏水的烧杯中,烧杯溶液中的
和温度随着加入醋酸体积的变化曲线如图所示,则下列有关说法正确的是
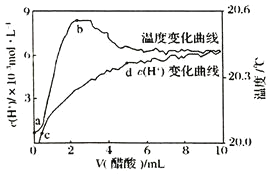
A.段,温度升高,可知醋酸电离过程中
键断裂为放热过程
B.段,
增加,醋酸电离程度增大
C.c点时,加入等体积等浓度的NaOH溶液,则:
D.d点时,
高三化学单选题困难题查看答案及解析
室温下,将醋酸慢慢滴入到盛
蒸馏水的烧杯中,烧杯溶液中的
和温度随着加入醋酸体积的变化曲线如图所示,则下列有关说法正确的是
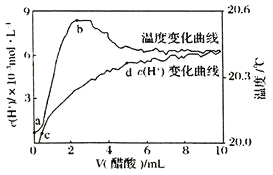
A.段,温度升高,可知醋酸电离过程中
键断裂为放热过程
B.段,
增加,醋酸电离程度增大
C.c点时,加入等体积等浓度的NaOH溶液,则:
D.d点时,
高三化学单选题困难题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
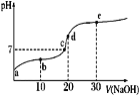
A. a点溶液的c(H+)=4×10-4mol·L-1
B. 水电离程度:e>d>c>b>a
C. b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D. d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
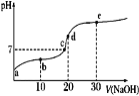
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
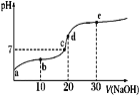
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
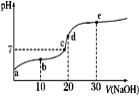
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定中和滴定的终点。某化学小组同学利用该原理在常温时,分别测定NaOH溶液和氨水的物质的量浓度,并得到如图所示曲线。
①待测溶液:100 mL氨水、100 mL NaOH溶液 ②标准溶液:0.40的盐酸。
 下列说法错误的是( )
下列说法错误的是( )
A.滴定NaOH溶液时,所得的曲线是b
B.达到滴定终点时,N点溶液的pH<7,M点溶液的pH=7
C.氨水溶液的物质的量浓度为0.10
D. NaOH溶液的pH=13
高三化学选择题简单题查看答案及解析
已知电导率越大导电能力越强。常温下用0.10 mol·L-1NaOH溶液分别滴定10mL浓度均为0.10 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是
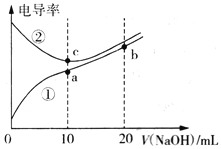
A.曲线①代表滴定盐酸的曲线
B.滴定醋酸的过程应该选择甲基橙作为指示剂
C.a、b、c三点溶液中水的电离程度:c>a>b
D.b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
高三化学单选题困难题查看答案及解析