恒温、恒容的条件下对于N2(g)+3H2(g)2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
A.断开一个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的压强不变
D.N2、H2、NH3分子数之比为1:3 :2的状态
高三化学选择题中等难度题
恒温、恒容的条件下对于N2(g)+3H2(g)2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
A.断开一个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的压强不变
D.N2、H2、NH3分子数之比为1:3 :2的状态
高三化学选择题中等难度题
恒温、恒容的条件下对于N2(g)+3H2(g)2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
A.混合气体的密度不变
B.断开一个N≡N的同时有6个N-H键生成
C.N2、H2、NH3分子数之比为1∶3∶2的状态
D.混合气体的平均相对分子质量不变
高三化学选择题中等难度题查看答案及解析
在某一恒温恒容的密闭容器中发生如下反应:3H2(g)+N2(g) 2NH3(g) △H<0。t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如下图所示。下列说法正确的是
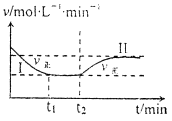
A.I、II两过程达到平衡时,平衡常数:KI<KII
B.I、II两过程达到平衡时,NH3的体积分数:I<II
C.I、II两过程达到平衡的标志:气体密度不再发生变化
D.t2时刻改变的条件可以是向密闭容器中加H2和N2混合气
高三化学选择题困难题查看答案及解析
在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g)2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强 | P1 | P2 | P3 |
| 反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A.2 c1>c3 B.a + b=92.4 C.2P1<P3 D.α1 +α3=1
高三化学单选题困难题查看答案及解析
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下[已知N2(g)十3H2(g)2NH3(g) △H=-92.4kJ/mol];下列说法正确的是( )
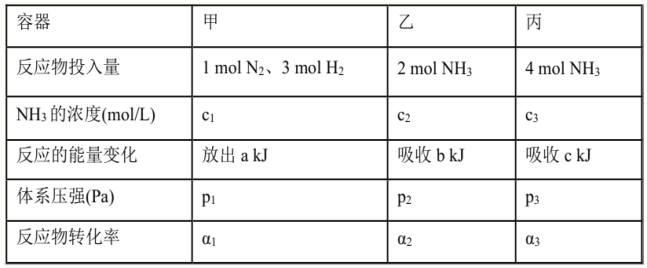
A. 2c1>c3 B. a+b>92.4 C. 2p2<p3 D. α1+α3<1
高三化学单选题困难题查看答案及解析
在3个2 L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下∶
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3 molH2、2 molN2 | 6 molH2、4 molN2 | 2 molNH3 |
| 达到平衡的时间/min | 5 | 8 | |
| 平衡时N2的浓度/ mol·L-1 | c1 | 1.5 | |
| NH3的体积分数 | φ1 | φ2 | |
| 混合气体的密度/g·L-1 | ρ1 | ρ2 |
下列说法不正确的是
A.容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol·L-1·min-1
B.在该温度下甲容器中反应的平衡常数K=
C.2c1<1.5
D.2ρ1=ρ2
高三化学选择题中等难度题查看答案及解析
在3个2 L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:
3H2(g)+N2(g) 2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:

下列说法正确的是
A.容器乙中反应从开始到达平衡的反应速率为v(H2)=1.5mol·L-1·min-1
B.2c1<1.5
C.2ρ1=ρ2
D. 在该温度下甲容器中反应的平衡常数
高三化学选择题困难题查看答案及解析
对于合成氨反应N2(g)+3H2(g)2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和
molH2,经10s达到平衡,平衡后压强为初始压强的
。则下列说法正确的是
A. 若要提高N2的转化率同时加快反应速率,可采取的措施有:缩小体积、充入N2、降低温度
B. 若该反应的平衡常数发生变化,平衡不一定移动
C. 保持温度和压强不变,再向容器中充入2 molN2,此时v正=v逆
D. 10s 内,v(NH3)=2mol/(L·s)
高三化学选择题困难题查看答案及解析
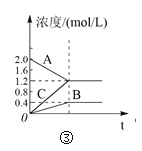
下列叙述与下图对应的是( )
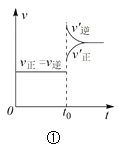
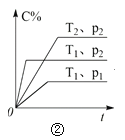

A.对于达到平衡状态的N2(g) + 3H2(g) ⇌ 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动
B.由图②可知,p2 > p1,T1 > T2满足反应:2A(g) + B(g) ⇌ 2C(g) ΔH < 0
C.图③表示的反应方程式为2A = B + 3C
D.对于反应2X(g) + 3Y(g) ⇌ 2Z(g) ΔH < 0,图④y轴可以表示Y的百分含量
高三化学单选题简单题查看答案及解析
(16分)
运用化学反应原理研究氮、氧等元素的单质及其化合物的反应有重要意义。
Ⅰ.(1)一定温度和压强下,反应N2(g) + 3H2(g) 2NH3(g)达到化学平衡状态。若向平衡体系中通入氩气,平衡________(填“向左”、“向右”或“不”)移动;若使用活性更强的催化剂,该反应的ΔH________ (填“增大”、“减小”或“不改变”)。
(2)在一定温度和压强下,已知:
O2 (g) = O2+ (g) + e-;H1= 1175.7 kJ/mol
PtF6 (g) + e- = PtF6- (g);H2= ―771.1 kJ/mol
O2PtF6 (s) = O2+ (g) + PtF6- (g);
H3= 482.2 kJ/mol
则反应O2 (g) + PtF6 (g) = O2PtF6 (s);H=_____________ kJ/mol。
Ⅱ.现有常温下的六种溶液:①0.01 mol/L CH3COOH溶液;②0.01 mol/L HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01 mol/L CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01 mol/L HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)⑤、⑥溶液比较,pH较大的是________。
(2)六种溶液中,水的电离程度相同的是______________。
(3)若②、③混合后所得溶液pH=7,则消耗溶液的体积:②________ ③(选填“>”、“<”或“=”)。
(4)稀释相同倍数后,溶液的pH:①________②,③________④(选填“>”、“<”或“=”)。
高三化学填空题中等难度题查看答案及解析
能够说明N2 + 3H2≒2NH3反应在密闭容器中已达到平衡状态的是( )
① 容器内N2、H2、NH3三者共存
② 容器内N2、H2、NH3三者浓度相等
③ 容器内N2、H2、NH3的浓度比恰为1:3:2
④ t min内生成1molNH3同时消耗0.5molN2
⑤ t min内,生成1molN2同时消耗3mol H2
⑥ 某时间内断裂3molH-H键的同时,断裂6molN-H键
⑦ 容器内质量不随时间的变化而变化
⑧ 容器内压强不随时间的变化而变化
⑨ 容器内密度不再发生变化
⑩ 容器内的平均摩尔质量不再发生变化
高三化学选择题中等难度题查看答案及解析