对于合成氨反应N2(g)+3H2(g)2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和
molH2,经10s达到平衡,平衡后压强为初始压强的
。则下列说法正确的是
A. 若要提高N2的转化率同时加快反应速率,可采取的措施有:缩小体积、充入N2、降低温度
B. 若该反应的平衡常数发生变化,平衡不一定移动
C. 保持温度和压强不变,再向容器中充入2 molN2,此时v正=v逆
D. 10s 内,v(NH3)=2mol/(L·s)
高三化学选择题困难题
对于合成氨反应N2(g)+3H2(g)2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和
molH2,经10s达到平衡,平衡后压强为初始压强的
。则下列说法正确的是
A. 若要提高N2的转化率同时加快反应速率,可采取的措施有:缩小体积、充入N2、降低温度
B. 若该反应的平衡常数发生变化,平衡不一定移动
C. 保持温度和压强不变,再向容器中充入2 molN2,此时v正=v逆
D. 10s 内,v(NH3)=2mol/(L·s)
高三化学选择题困难题
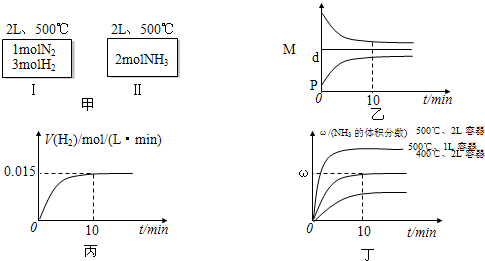
对于合成氨反应N2(g)+3H2(g)2NH3(g),恒温条件下,向某一2L的密闭容器中充入1molN2和
molH2,经10s达到平衡,平衡后压强为初始压强的
。则下列说法正确的是
A. 若要提高N2的转化率同时加快反应速率,可采取的措施有:缩小体积、充入N2、降低温度
B. 若该反应的平衡常数发生变化,平衡不一定移动
C. 保持温度和压强不变,再向容器中充入2 molN2,此时v正=v逆
D. 10s 内,v(NH3)=2mol/(L·s)
高三化学选择题困难题查看答案及解析
高三化学选择题中等难度题查看答案及解析
298K时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)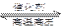 2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1
在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4 kJ是______________________________________________。
高三化学填空题简单题查看答案及解析
已知一定温度下合成氨反应:N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ•mol-1,在恒温恒压的密闭容器中进行如下实验:①通入1molN2和3molH2,达平衡时放出热量为Q1,②通入2molN2和6molH2,达平衡时放出热量为Q2,则下列关系正确的是( )
A.2Q1<Q2 B.Q2=184.8kJ
C.Q1<Q2=184.8kJ D.Q2=2Q1
高三化学单选题困难题查看答案及解析
已知:N2(g)+3H2(g)2NH3(g)△H= —92 kJ/mol,相关数据如下表。一定条件下,在体积为1L的密闭容器中加入1molN2和3molH2充分反应,放出热量Q1kJ,下列说法正确的是( )
| H2(g) | N2(g) | NH3(g) | |
| 1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
A.如图可表示合成氨过程中的能量变化
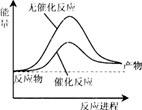
B.a的数值为391
C.Q1的数值为92
D.相同条件下,反应物若为2molN2和6molH2,放出热量Q2>2Q1
高三化学选择题中等难度题查看答案及解析
已知合成氨的热化学方程式为:N2(g)+ 3H2(g) 2NH3(g)△H=-92kJ/mol,下列说法中正确的是
A. 当1molN2与3molH2充分反应,可放出92kJ热量
B. 恒容恒温发生该反应时,向容器中充入少量He,反应速率加快且平衡正向移动
C. 恒压恒温发生该反应时,向容器中充入少量He,反应速率不变且平衡不移动
D. 升高温度时,正、逆反应速率都加快,而逆反应速率增加更多
高三化学单选题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
(10分)(1)可逆反应N2(g)+3H2(g)2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为________ 。
(2)除电解法,工业炼镁还可采用硅热法(Pidgeon法)。即以煅白(CaO·MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:
(CaO·MgO)(s) + Si(s) Ca2SiO4 (l) + 2Mg(g)
①已知还原性:Mg > Si,上述反应仍能发生的原因是______________________________
②由右图,推测上述反应正向为______(填“吸热”或“放热”)反应;平衡后若其他条件不变,将还原炉体积缩小一半,则达到新平衡时Mg(g)的浓度将______(填“升高” 、“降低”或“不变”)。
③若还原炉容积为400m3,原料中煅白质量为9.6 t,5小时后,测得煅白的转化率为50%,
计算这段时间Mg的生成速率 ___________________。
高三化学填空题简单题查看答案及解析
设NA表示阿伏加德罗常数的值,下列说法中正确的
①一定条件下定容容器中充入3molH2(g)和1molN2(g)发生反应:3H2(g)+N2(g)2NH3(g);△H=-QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.25NA
②常温下,21gC3H6和C4H8的混合物中含有的碳原子数为1.5NA
③14.2g硫酸钠固体中含有0.1NA个硫酸钠分子;
④2gD216O中含有的质子数、中子数、电子数均为NA
⑤标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
⑥将100mL0.1mol·L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
A.①③⑥ B.④⑤⑥ C.①②④ D.①⑥
高三化学选择题困难题查看答案及解析
高三化学解答题中等难度题查看答案及解析