-
某实验小组设计了下列装置进行氨的催化氧化实验。
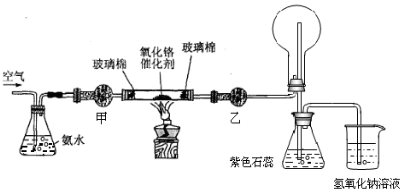
(1)常温下,用5.8 mol/L的氨水时实验现象明显,现用浓氨水配制该浓度的氨水480mL,需要烧杯、玻璃棒,还需要的玻璃仪器有 。
(2)甲处药品的名称为_____________。
(3)实验时,先将催化剂加热至红热,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明反应是_____(填“吸”或“放”)热反应,化学方程式为 ;乙处加入无水氯化钙,烧瓶中发生反应的化学方程式为___ ;锥形瓶中产生的现象为 _。
(4)如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中产生的现象为 。
(5)现用镁与石墨作电极,浓氯化铵溶液作电解液构成原电池,正极的电极反应式为 。
-
某实验小组设计了下列装置进行氨的催化氧化实验。
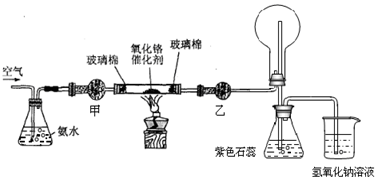
完成下列填空:
(1)常温下,氨水的浓度为1:1.5(28%的浓氨水和水的体积比)时实验现象明显,配制该浓度氨水的玻璃仪器有________。
(2)本实验用的干燥剂是碱石灰和无水氯化钙。则甲处是____________;乙处是___________。
(3)实验时,先将催化剂加热至红热,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明反应是_____(填“吸”或“放”)热反应;化学方程式为 。
(4)实验前,烧杯中盛有200mL 1.000 mol/L的 NaOH溶液,实验后测得烧杯中溶液的pH=13,且溶液质量比反应前增加了7.48g,则NaOH溶液吸收的NO和NO2的物质的量之比
是________(设溶液的体积不变且忽略盐类的水解)。
(5)实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中产生白烟。其原因可用化学方程式表示为:________、________。
(6)已知NH3和N2常压下的沸点分别为:-33.5℃和-195.8℃,据此推测这两种物质中,能做制冷剂的是 ________(填分子式);能用来冷冻物质的是________(填分子式)。
-
(1)氨气是重要的化工原料.实验室可用浓氨水和 来制取氨气.
a.烧碱 b.生石灰 c.氯化铵
(2)某实验小组设计了下列装置进行氨的催化氧化实验.
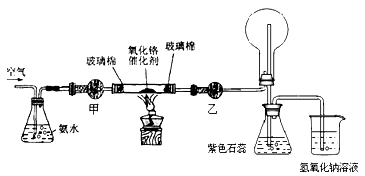
①盛放氨水的实验仪器的名称为 ;在加热条件下,硬质玻璃管中发生反应的化学方程式为 .
②实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中先产生白雾,随即产生白烟,其原因是 .
③烧杯中盛有NaOH溶液的作用是 .
-
氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。
Ⅰ.实验室模拟工业氨催化氧化法制取硝酸,装置如下图所示。
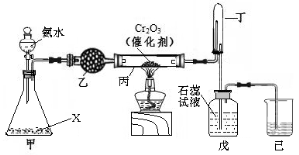
(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有烧杯、玻璃棒、量筒、 、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X的化学式为 。
(3)写出受热时丙装置发生反应的化学方程式 。当戊中观察到石蕊试液变红,则说明已制得硝酸。
Ⅱ.NH3的性质
(4)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),将等浓度、等体积的氨水和硝酸混合,所得溶液中离子浓度从大到小的顺序为 。
(5)已知:氨在纯氧中燃烧生成一种单质和水,利用此原理设计成氨气-氧气燃料电池。在碱性条件下,该电池的负极反应式为 。
-
氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如图1所示的装置。

(1)若分液漏斗中氨水的浓度为9.0mol•L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、玻璃棒、_______________。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为_______________。
(3)乙装置的作用是_______________;写出受热时丙装置发生反应的化学方程式为_______________。
(4)当戊中观察到_______________现象,则说明已制得硝酸.某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因_______________,如何改进装置_______________。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是_______________。
-
(20分)氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置。

(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、玻璃棒、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X的名称为 。
(3)乙装置的作用是 ;写出受热时丙装置发生反应的化学方程式为 。
(4)当戊中观察到 现象,则说明已制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因 。如何改进装置 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是 ;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1 mol·L-1的NaOH溶液滴定。滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是 。
-
氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置。
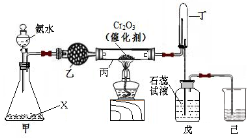
(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为 。
(3)乙装置的作用是 ;写出受热时丙装置发生反应的化学方程式为 。
(4)当戊中观察到 现象,则说明已制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因 。如何改进装置 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是 ;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1 mol·L-1的NaOH溶液滴定。滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是 。
-
氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置:

(1)若分液漏斗中氨水的浓度为9.0mol•L﹣1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、玻璃棒、_____。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X的名称为_____。
(3)乙装置的作用是_____;写出受热时丙装置发生反应的化学方程式为_____。
(4)当戊中观察到_____现象,则说明已制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因__________。如何改进置_________。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是_____。
-
氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置。
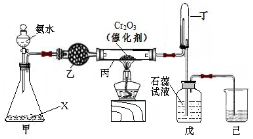
(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为 。
(3)乙装置的作用是 ;写出受热时丙装置发生反应的化学方程式为 。
(4)当戊中观察到 现象,则说明已制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因 。如何改进装置 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是 ;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1 mol·L-1的NaOH溶液滴定。滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是 。
-
常温下,某化学小组探究硝酸银溶液的性质。
| 装置 | 实验序号 | 实验操作 | 实验现象 |
| 
| 实验I | 向试管中滴加2%氨水并不断振荡 | 产生棕褐色沉淀,继续滴加沉淀消失 |
| 实验II | 1.向试管中加入0.1mol·L-lNaOH溶液1mL 2.继续滴加3%H2O2至过量 | 1.产生棕褐色沉淀 2.产生大量无色无味气体,有黑色沉淀生成 |
| 实验III | 1.向试管中滴加1mL0.1mol•L-1KI溶液 2.取少量上层清液于试管甲中,加入淀粉溶液 | 1.产生黄色沉淀 2.溶液无明显变化 |
已知:AgOH是一种白色固体,常温下极不稳定,易分解为棕褐色难溶于水的氧化银固体
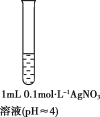
(1)常温下,0.1mo1•L-1AgNO3溶液pH约为4,请用离子方程式解释原因___。
(2)实验I中,反应的化学方程式是___。
(3)实验II中,经检验,黑色沉淀的成分为Ag。有Ag产生的化学方程式是___。经测定,实验产生的气体体积远远大于该反应的理论值,可能的原因是___。
(4)实验中,产生黄色沉淀的离子方程式是___。有同学猜想,I-有还原性,Ag+有氧化性,AgNO3溶液与KI溶液应该可以发生氧化还原反应。他设计了如图原电池,做实验IV证明了猜想成立。其中,在A烧杯中,石墨电极表面变亮,经检测这种光亮的物质为银单质。乙溶液是___,检验B烧杯中产物的操作及现象是___,该氧化还原反应的离子方程式是__。
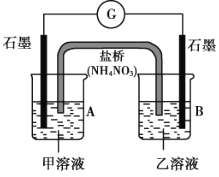
(5)对比实验III和实验IV,实验III无I2生成的可能原因是___(写出两条)。













