-
我国废水三级排放标准规定:废水中苯酚的含量不得超过1.00mg/L。实验室可用一定浓度的溴水测定某废水中苯酚的含量,其原理如下:

(1)请完成相应的实验步骤:
步骤1:准确量取25.00mL待测废水于250mL锥形瓶中。
步骤2:将5.0 mL 0.01mol/L溴水迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中加入过量的0.1mol/L KI溶液,振荡。
步骤4: ,再用0.01 mol/L Na2S2O3标准溶液滴定至终点,消耗 Na2S2O3溶液8.50 mL。(反应原理:I2 + 2Na2S2O3 = 2NaI + Na2S4O6)
(2)该废水中苯酚的含量为 mg/L。
(3)步骤2塞紧瓶塞的原因是 。
(4)步骤3若振荡时间过长,则测得的废水中苯酚的含量 (填“偏高”、“偏低”或“无影响”,下同)。步骤4中若滴定至终点时滴定管尖嘴处出现气泡,而滴定前无气泡,会使测得的废水中苯酚的含量 。
-
空气中的SO2含量和可吸入颗粒的含量(可用g/cm3表示)都是重要的空气质量指标。在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02 mg/L。
(1)为测定某地方的空气中SO2和可吸入颗粒的含量,甲同学设计了如下图所示的实验装置:
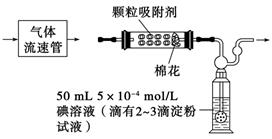
注:气体流速管是用来测量单位时间内通过气体的体积的装置
①应用上述装置测定空气中的SO2含量和可吸入颗粒的含量,除测定气体流速(单位:cm3/min)外,还需要测定___________________________________________________
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度。
请你协助甲同学完成100 mL 5×10-4 mol/L碘溶液的配制:
第一步:准确称取1.27g碘单质加入烧杯中,___________________________
第二步:___________________________________________________________;
第三步:从第二步所得溶液中,取出10.00 mL溶液于100 mL容量瓶中,加水稀释至刻度线。
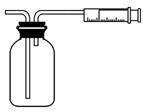
(2)乙同学拟用如图所示简易装置测定空气中的SO2含量:准确移取50 mL 5×10-4 mol/L的碘溶液,注入图中所示广口瓶中,加2~3滴淀粉指示剂,此时溶液呈蓝色。在指定的测定地点抽气,每次抽气100 mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n)。
①假设乙同学的测量是准确的,乙同学抽气的次数至少为________次,方可说明该地空气中的SO2含量符合排放标准。
②如果乙同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,请你对其可能的原因(假设溶液配制、称量或量取及各种读数均无错误)提出两种合理假设:__________________、______________________。
③丙同学认为:乙同学的实验方案需要抽气的次数太多,操作麻烦。与乙讨论后,决定将抽气次数降到100次以下,请你设计合理的改进方案:_________________________。
-
我国生活饮用水水质标准规定锰元素不得超过0.1mg/L.水体中的锰主要以Mn2+存在,可通过放大反应法测定自来水中Mn2+的含量,根据下列测定步骤回答问题.
步骤一:配制500mL0.10mol/L硫代硫酸钠 (Na2S2O3)标准溶液.
(1)需要称取______g硫代硫酸钠固体,配制过程中,必须用到的玻璃仪器有______,下列操作会使所配溶液浓度偏低的是______ (填下列选项的字母序号).
A.称取硫代硫酸钠固体时,将硫代硫酸钠固体放在托盘天平右盘
B.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
C.未将洗涤烧杯内壁的溶液转入容量瓶
D.定容时俯视刻度线
E.定容时,不小心加水超过刻度线,立即用胶头滴管吸出多余的水
步骤二:取50.0mL自来水样品放入锥形瓶中,加入适量H2 SO4酸化,然后加入过量的KIO4,发生反应
2Mn2++5IO4-+3H2O═2MnO4-+5IO3-+6H+多余的KIO4通过加入掩蔽剂来消除干扰.再加入足量的KI溶液,使之与上述反应生成的MnO4-,IO3-反应,制得待测液.
(2)加入足量的KI溶液时,发生反应的离子方程式分别是:2MnO4-+10I-+16H+═2Mn2++5I2+8H2 O、______
步骤三:用稀释至0.0010mol/L的硫代硫酸钠溶液滴定上述待测液,发生反应:I2+2Na2S2O3═2NaI+NaS4O6
达到滴定终点时消耗Na2S2O3溶液12.00mL
(3)滴定操作时,用______作指示剂,达到滴定终点的现象为______,测得自来水样品中锰元素的含量为______mg/L,该自来水不符合我国生活饮用水水质标准.
-
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L。下列措施中能够减少SO2排放量的是:① 用天然气代替煤炭作民用燃料 ② 提高热能利用率 ③燃煤中加入石灰后使用 ④ 在已被酸雨侵害的土壤中洒石灰
A.①② B.②④ C.①③④ D.①②③
-
(15分)
我国规定:室内甲醛含量不得超过0.0 8mg·m-3。某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛(HCHO)的含量。
【查阅资料】KMnO4 ( H+)溶液为强氧化剂,可氧化甲醛和草酸。
4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O
2MnO4―+5H2C2O4+6H+=2Mn2++10CO2 ↑+8H2O
【实验一】
按如图所示装置进行采样
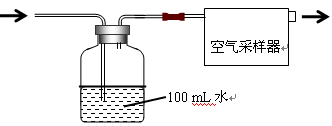
(1)由图可知甲醛的物理性质为________
(2)空气中甲醛采样吸收装置中用到的玻璃仪器为:玻璃导管、________
(3)为了使通过吸收装置的甲醛尽可能被吸收液吸收,可采取的措施是:(只写出一种即可)________。
设置空气采集器为恒定流量0.5 L/min,采集20min。
【实验二】
量取10.00 mL 的甲醛吸收液转移到锥形瓶中,量取12.00 mL 1.00×10-3 mol·L-1 KMnO4溶液于锥形瓶中,并滴入几滴稀H2SO4备用。
(4)用1.00×10-3 mol·L-1标准草酸溶液进行滴定,当
时,达到滴定终点。
(5)记录滴定所消耗的草酸溶液的体积。重复实验2次,消耗草酸溶液的体积分别为10.90 mL、10.02 mL、9.98 mL。计算该居室内空气中甲醛的浓度为________ mg·m-3。
(6)若滴定过程中,发现滴定管下端开始有气泡,滴定后气泡消失,则测定结果将________
(填“偏大”、“无影响”、“偏小”)
【实验三】
环境监测站工作人员采样后,将5.00 mL 的甲醛吸收液注入比色瓶中,再向比色瓶中注入显色试剂0.5 mL,盖紧瓶塞,摇匀,静置显色。当室内环境温度不同时,记录显色时间见下表。
| 环境温度/℃ | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
| 显色时间/min | 45 | 30 | 15 | 13 | 10 | 7 | 5 |
(7)由该表可以得出的结论是________
(8)请用化学反应原理解释________
-
(8分)(2011·西宁模拟)甲醛是世界卫生组织(WHO)确认的致癌物质和致畸物质之一。我国规定:室内甲醛含量不得超过0.08mg·m-3。某研究性学习小组打算利用酸性KMnO4溶液测定新装修房屋内的空气中甲醛的含量,请你参与并协助他们完成相关的学习任务。
测定原理:
酸性KMnO4为强氧化剂,可氧化甲醛和草酸,其反应方程式如下所示:
4MnO4-+5HCHO+12H+===4Mn2++5CO2↑+11H2O
2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
测定装置:
部分装置如下图所示:
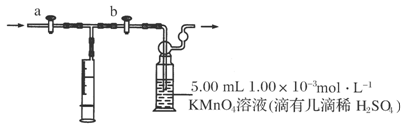
测定步骤:
(1)用______________量取5.00 mL 1.00×10-3mol·L-1KMnO4溶液,注入洗气瓶中,并滴入几滴稀H2SO4,加水20 mL稀释,备用。
(2)将1.00×10-3 mol·L-1的草酸标准溶液置于酸式滴定管中备用。
(3)打开a,关闭b,用注射器抽取100 mL新装修房屋内的空气。关闭________,打开________(填“a”或“b”),再推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。再重复4次。
(4)将洗气瓶中的溶液转移到锥形瓶中(包括洗涤液),再用草酸标准溶液进行滴定,记录滴定所消耗的草酸标准溶液的体积。
(5)再重复实验2次(每次所取的高锰酸钾溶液的体积均为5.00 mL)。3次实验所消耗的草酸标准溶液的体积平均值为12.38 mL。
交流讨论:
(1)计算该新装修房屋内的空气中甲醛的浓度为________mg·m-3,该新装修房屋内的甲醛________(填“是”或“否”)超标;
(2)某同学用该方法测量空气中甲醛的含量时,所测得的数值比实际含量低,请你对其可能的原因(假设称量或量取、溶液配制及滴定实验均无错误)提出合理假设:______________、______________(至少答出两种可能性);
(3)实验结束后,该小组成员在相互交流的过程中一致认为:
①实验原理可以简化
实验中可不用草酸标准溶液滴定,可多次直接抽取新装修房屋内的空气,再推送到洗气瓶中,直至_________________________________________________________;

②实验装置应加以改进
可将插入酸性KMnO4溶液中的导管下端改成具有多孔的球泡(如图所示),有利于提高实验的准确度,其理由是___________________________________________________。
-
电镀废水中常含有NaCN,工业上规定其含量低于0.5 mg/L才可排放,对NaCN超标的废水可用两段氧化法处理:
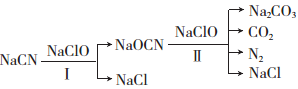
己知:HCN的酸性比碳酸的酸性弱,有剧毒;HCN、HOCN中N元素的化合价相同。
请回答下列问题:
(1)第一次氧化时,溶液的pH应调节为______(填“酸性”、“碱性”或“中性”);原因是___________。反应中,欲使1 mol NaCN变为NaOCN,则需要氧化剂NaClO至少为________mol。
(2)写出第二次氧化时发生反应的离子方程式:_____________________。反应中被氧化的元素是__________。
(3)处理10 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO__________g(实际用量应为理论值的4倍),才能使废水中NaCN含量达到排放标准。
-
下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
| 冷轧含锌 废水水质 | 经处理后的水国 家环保标准值 |
| Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
| pH | 1~5 | 6~9 |
| SO42-浓度/(mg·L-1) | ≤23 000 | ≤150 |
经某一工艺处理后的废水pH=8,常温下,该废水中Zn2+的浓度为 mg·
L-1(常温下,Ksp[Zn(OH)2]=1.2×10-17), (填“符合”或“不符合”)国家环保标准。
-
化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L−1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L−1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v2 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________。
(2)Ⅰ中发生反应的离子方程式是_______________________________。
(3)Ⅲ中发生反应的化学方程式是_________________________________。
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是______________________________。
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是________。
(6)Ⅴ中滴定至终点的现象是_____________________________。
(7)废水中苯酚的含量为___________g·L−1(苯酚摩尔质量:94 g·mol −1)。
(8)由于Br2具有____________性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果偏高。
-
我国工业废水中几种污染物即其最高允许排放浓度如下表。下列说法不正确的是
| 污染物 | 汞 | 镉 | 铬 | 铅 | 砷 | 氰化物 |
| 主要存在形式 | 
| 
| 

| 
| 

| 
|
| 最高允许排放浓度 
| 
| 
| 
| 
| 
| 
|
注:我国规定酸、碱废水pH的最大允许排放标准是大于6、小于
A. 、
、 、
、 是重金属离子
是重金属离子
B.对于 的废水可用中和法处理
的废水可用中和法处理
C.将 转化为
转化为 是用氧化还原的方法
是用氧化还原的方法
D.在含有 的废水中加入
的废水中加入 ,可使转变为沉淀而除去
,可使转变为沉淀而除去




