-
0.1mol/LNa2S2O3溶液与0.1mol/LH2SO4溶液各5mL和10mL水混合,反应速率为v1mol/(L·s);0.2mol/L Na2S2O3溶液与0.2mol/LH2SO4溶液各5mL和20mL水混合,反应速率为v2mol/(L·s);则v1和v2的关系是 ( )
A.大于 B.小于 C.等于 D.不能确定
高三化学选择题中等难度题查看答案及解析
-
0.1 mol·L-1Na2S2O3溶液和0.1 mol·L-1H2SO4溶液各5 mL,与10 mL水混合,反应速率为v1mol·L-1·s-1;0.2 mol·L-1Na2S2O3溶液和0.2 mol·L-1H2SO4溶液各5 mL,与20 mL水混合,反应速率为v2mol·L-1·s-1。则v1和v2的关系是( )
A.v1>v2
B.v1<v2
C.v1=v2
D.不能肯定
高三化学单选题中等难度题查看答案及解析
-
30℃时,将10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/L H2SO4溶液混合,3min后溶液中明显出现浑浊。已知温度每升高10℃,化学反应速率增大到原来的3倍,那么50℃时,同样的反应要同样看到浑浊,需要的时间是 ( )
A.10s B.20s C.30s D.40s
高三化学选择题简单题查看答案及解析
-
已知反应:2H2O2=2H2O+O2↑,下列条件下,反应速率最大的是
A.10℃,5mL 3 %H2O2溶液 B.10℃,5mL 5 %H2O2溶液
C.39℃,5mL 5%H2O2溶液 D.30℃,5mL 5 %H2O2溶液且加入少量MnO2
高三化学选择题简单题查看答案及解析
-
某小组同学对FeCl3与KI的反应进行探究。
(初步探究)室温下进行下表所列实验。
序号
操作
现象
实验Ⅰ
取5mL 0.1mol/L KI溶液,滴加0.1mol/L FeCl3溶液5∼6滴(混合溶液pH=5)
溶液变为棕黄色
实验Ⅱ
取2mL实验Ⅰ反应后的溶液,滴加2滴0.1mol⋅L−1 KSCN溶液
溶液呈红色
(1)证明实验Ⅰ中有Fe2+ 生成,加入的试剂为____________________________。
(2)写出实验Ⅰ反应的离子方程式:_____________________________________。
(3)上述实验现象可以证明Fe3+与I−发生可逆反应,实验Ⅰ在用量上的用意是__________
(4)在实验I的溶液中加入CCl4,实验现象是____________________________,取其上层清液中滴加KSCN溶液,并未看到明显的红色,其原因为(从平衡移动的角度解释)_________________________________________________________。
(深入探究)20min后继续观察实验现象:实验Ⅰ溶液棕黄色变深;实验Ⅱ溶液红色变浅。
(5)已知在酸性较强的条件下,I−可被空气氧化为I2,故甲同学提出假设:该反应条件下空气将I−氧化为I2,使实验Ⅰ中溶液棕黄色变深。甲同学设计实验:____________________________________,20min内溶液不变蓝,证明该假设不成立,导致溶液不变蓝的因素可能是__________________________。
高三化学实验题困难题查看答案及解析
-
NA为阿伏伽德罗常数的值.下列说法正确的是
A.18gD2O和18gH2O中含有的质子数均为10NA
B.2L 0.5mol/LNa2S溶液中含有的S2﹣个数为NA
C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
D.密闭容器中2molSO2与1molO2充分反应,产物的分子数为2NA
高三化学选择题困难题查看答案及解析
-
用惰性电极电解煤浆液的方法制H2的反应为C(s)+2H2O(l)=CO2(g)+2H2(g)。现将一定量的1mol/LH2SO4溶液和适量煤粉充分混合,制成含碳量为0.02g/mL~0.12g/mL的煤浆液,置于如图所示装置中进行电解(两电极均为惰性电极)。下列说法错误的是
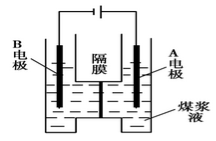
A.A极是阳极,B极为阴极
B.A极的电极反应式为C+2H2O-4e-=CO2↑+4H+
C.B极的电极反应式为2H++2e-=H2↑
D.电解一段时间后,煤浆液的pH增大
高三化学选择题中等难度题查看答案及解析
-
将镁、铝的混合物0.1mol 溶于100mL 2mol/LH2SO4溶液中,然后在得到的溶液中滴加1mol/LNaOH 溶液,请回答:
(1)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好完全沉淀,则加入NaOH溶液的体积是V(NaOH)=________mL。
(2)若在滴加NaOH溶液过程中,沉淀的质量随加入NaOH溶液的体积变化如下图所示。当V1=160mL时,求金属粉末中镁的物质的量和V2的体积?(要求写出解题过程)
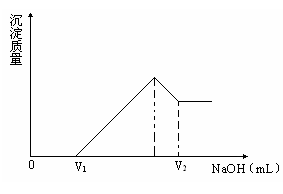
(3)若混合物仍为0.1mol ,其中Mg的物质的量分数为a,用100mL 2mol/L的H2SO4溶解此混合物后,再加入450mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3,则满足此条件的a的取值范围为________。
高三化学填空题中等难度题查看答案及解析
-
1.52g铜镁合金完全溶解于5mL 14mol/L的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g 沉淀.下列说 法不正确的是
A. 该合金中铜与镁的物质的量之比是2:l
B. 得到2.54g 沉淀时,加入NaOH 溶液的体积是600mL
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 与铜镁合金反应的HNO3的物质的量为0.12mol
高三化学单选题困难题查看答案及解析
-
1.52g铜镁合金完全溶解于5mL 14mol/L的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g 沉淀.下列说 法不正确的是
A. 该合金中铜与镁的物质的量之比是2:l
B. 得到2.54g 沉淀时,加入NaOH 溶液的体积是600mL
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 与铜镁合金反应的HNO3的物质的量为0.12mol
高三化学选择题困难题查看答案及解析