-
(16分)工业上硫酸锰铵[(NH4)2Mn(SO4)2]可用于木材防火涂料等。其制备工艺如下: 
已知步骤Ⅰ反应:H2C2O4(aq) +H2SO4(aq) +MnO2(s) MnSO4(aq)+2CO2(g)+2H2O(1) △H
MnSO4(aq)+2CO2(g)+2H2O(1) △H
(1)在步骤I的反应中,氧化剂是 。
(2)步骤Ⅱ中趁热过滤前需向MnSO4溶液中加入少量热水,其目的是____;步骤III所得(NH4)2Mn(SO4)2:晶体需用酒精溶液洗涤,洗去的主要杂质离子有____ 。
(3)下列操作有利于提高产品产率的是____(填序号)。
A.慢慢分次加入二氧化锰 B.趁热过滤
C.冰水浴充分冷却 D.用水代替酒精溶液洗涤
(4)一定条件下,在步骤I的水溶液中l mol MnO2完全反应相相对能量变化如图。则△H=____;催化剂是否参加化学反应? (填“是”或“否”或“不确定”)。

(5)碱性干电池中含大量MnO2可以回收利用,该电池工作时的正极反应式为____ ;若从干电池中回收87 kg MnO2,理论上可以获得(NH4)2Mn( S04)2 _kg。
-
(10分)以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:
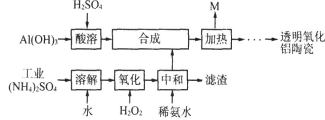
回答下列问题:
(1)写出氧化步骤中发生的主要反应的离子方程式 。
(2)如何检验中和液中的杂质离子已完全除尽? 。
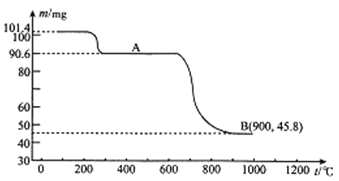
(3)固体NH4Al(SO4)2·12H2O[相对分子质量:453]在加热时,固体残留率随温度的变化如图所示。

633℃时剩余固体的成分化学式为 。
(4)综上分析,流程图中M的主要成分的化学式为 ,M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
用含SO2的硫酸工业尾气联合制备(NH4)2SO4和MnxOy,其工艺流和如下:

(1)反应I的化学方程式为__________;反应II控制温度60℃~70℃之间的原因是________。反应I到反应II的过程中可循环利用的物质是__________________。
(2)反应III中以SO2作___________剂。
(3)MnCO3的作用是除去滤液中的Fe3+,写出除去Fe3+的离子反应方程式___________。
(4)MnS的作用是提供S2-除去Ni2+和Cu2+;当Ni2+恰好完全沉淀时[c(Ni2+)= 1.0×10-5 mol·L -1〕,溶被中Cu2+的浓度是_______ mol·L -1(已知Ksp(CuS)=8.4×10-45, Ksp(NiS)=1.4×10-24,) 。
(5)从MnSO4溶液中获得MnSO4·nH2O的方法是_____________。
(6) “锻烧”时温度与剩余固体质量变化曲线如下图:
该曲线中B点所表示的固体氧化物的化学式为_______________。
-
用含SO2的硫酸工业尾气联合制备(NH4)2SO4和MnxOy,其工艺流和如下:
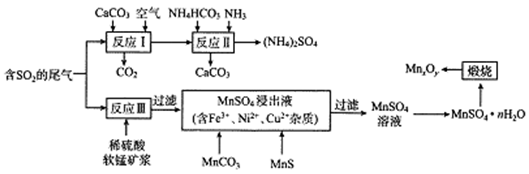
(1)反应I的化学方程式为__________;反应II控制温度60℃~70℃之间的原因是________。反应I到反应II的过程中可循环利用的物质是__________________。
(2)反应III中以SO2作___________剂。
(3)MnCO3的作用是除去滤液中的Fe3+,写出除去Fe3+的离子反应方程式___________。
(4)MnS的作用是提供S2-除去Ni2+和Cu2+;当Ni2+恰好完全沉淀时[c(Ni2+)= 1.0×10-5 mol·L -1〕,溶被中Cu2+的浓度是_______ mol·L -1(已知Ksp(CuS)=8.4×10-45, Ksp(NiS)=1.4×10-24,) 。
(5)从MnSO4溶液中获得MnSO4·nH2O的方法是_____________。
(6) “锻烧”时温度与剩余固体质量变化曲线如下图:
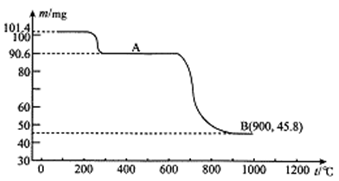
该曲线中B点所表示的固体氧化物的化学式为_______________。
-
工业上以Al(OH)3、H2SO4、(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图所示:
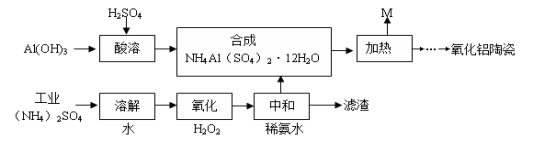
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为 。
(2)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O NH3·H2O+H+,则该反应的平衡常数为 。
NH3·H2O+H+,则该反应的平衡常数为 。
(3)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为 。
(4)固体NH4Al(SO4)2·12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体的成分为 。
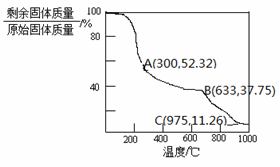
(5)综上分析,流程图中M混合气体的主要成分的化学式为 。M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
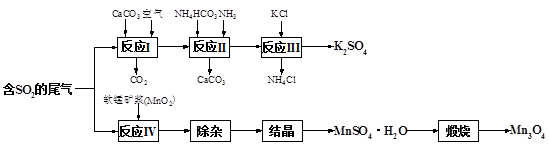
(1)几种盐的溶解度见图。反应III中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、、洗涤、干燥等操作即得K2SO4产品。

(2)检验K2SO4样品是否含有氯化物杂质的实验操作是:________。
(3)反应IV的化学方程式为________________。
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为________________。
(5)下图是煅烧MnSO4•H2O时温度与剩余固体质量变化曲线。

①该曲线中B段所表示物质的化学式为。
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小。试分析产物总锰含量减小的原因:________。
-
K2SO4是无氯优质钾肥,Mn3O4是生产磁性氧体材料的主要原料,以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:

(1)几种盐的溶解度见图2.反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、________、洗涤、干燥等操作即得K2SO4产品。
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是______________________________;
(3)反应Ⅳ的化学方程式为_____________________________;
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为_____________________________;
(5)图3煅烧MnSO4•H2O时温度与剩余固体质量变化曲线。
①该曲线中B段所表示物质的化学式为_______________________;
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小.试分析产物总锰含量减小的原因_______________________。
-
K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
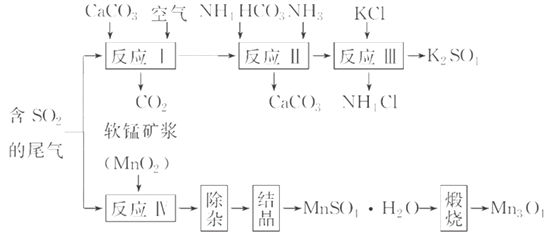

(1)几种盐的溶解度见图1。反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行________、________、洗涤、干燥等操作即得K2SO4产品。
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是:_____________________________________。
(3)反应Ⅳ的化学方程式为______________________________________________。
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为____________________________________________。
(5)图2是煅烧MnSO4·H2O时温度与剩余固体质量变化曲线。
①该曲线中B段所表示物质的化学式为___________________。
②煅烧过程中固体的锰含量随温度的升高而增大,但当温度超过1000 ℃时,再冷却后,测得产物的总锰含量反而减小。试分析产物总锰含量减小的原因:____________________________。
(6)一种新型燃料电池,一极通入空气,另一极通入丁烷;电解质是掺杂Mn3O4的二氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。在熔融电解质中,O2-向________(填“正”或“负”)极移动。电池负极电极反应为________________________。
-
铵明矾(NH4Al(SO4)2•12H2O)是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备。用芒硝(Na2SO4•10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
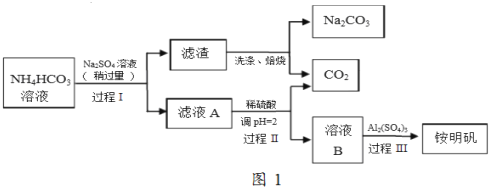
完成下列填空:
(1)铵明矾溶液呈_________性,它可用于净水,原因是_______________;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是__________________。
(2)写出过程Ⅰ的化学反应方程式_______________。
(3)若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是___________。
(4)已知铵明矾的溶解度随温度升高明显增大.加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、___________、过滤洗涤、干燥。
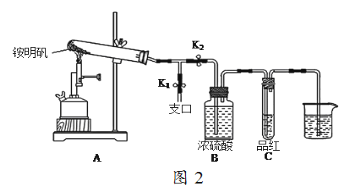
(5)某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份。
①夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是______________;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是___________(任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式_______________。
②该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=_____。
-
铵明矾【NH4Al(SO4)2•12H2O】是常见的食品添加剂,用于焙烤食品,可通过硫酸铝溶液和硫酸铵溶液反应制备.用芒硝(Na2SO4•10H2O)制备纯碱和铵明矾的生产工艺流程图如图1:
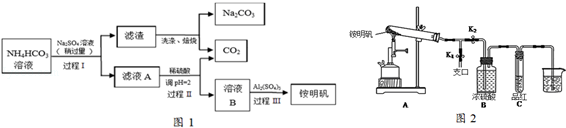
完成下列填空:
(1)铵明矾溶液呈 性,它可用于净水,原因是 ;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是 .
(2)写出过程Ⅰ的化学反应方程式 .
(3)若省略过程Ⅱ,直接将硫酸铝溶液加入滤液A中,铵明矾的产率会明显降低,原因是 .
(4)已知铵明矾的溶解度随温度升高明显增大.加入硫酸铝后,经过程III的系列实验得到铵明矾,该系列的操作是加热浓缩、 、过滤洗涤、干燥.
(5)某同学用图2图示的装置探究铵明矾高温分解后气体的组成成份.
①夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧.实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是 ;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是 (任填一种物质的化学式);另分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式 .
②该同学通过实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)= .

MnSO4(aq)+2CO2(g)+2H2O(1) △H

















