25 ℃时,用0.10 mol·L-1的盐酸分别滴定体积相同且浓度均为0.10 mol·L-1的三种一元碱XOH、YOH 及ZOH,滴定曲线如图所示。下列说法正确的是
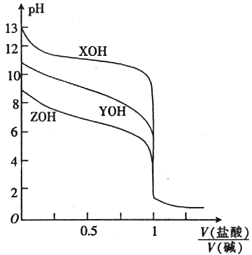
A. YOH 是强碱
B. V(盐酸)/V(碱)=0.5 时,c(Z+)>c(Y+ )>c(X+)
C. X++H2OXOH+H+ 的平衡常数K=10-4
D. 滴定XOH 时可用酚酞作指示剂
高三化学单选题中等难度题
25 ℃时,用0.10 mol·L-1的盐酸分别滴定体积相同且浓度均为0.10 mol·L-1的三种一元碱XOH、YOH 及ZOH,滴定曲线如图所示。下列说法正确的是

A. YOH 是强碱
B. V(盐酸)/V(碱)=0.5 时,c(Z+)>c(Y+ )>c(X+)
C. X++H2OXOH+H+ 的平衡常数K=10-4
D. 滴定XOH 时可用酚酞作指示剂
高三化学单选题中等难度题
25℃时,用0.10mol/L的盐酸分别滴定体积相同且浓度均为0.10mol/L的三种一元碱XOH、YOH及ZOH,滴定曲线如图所示。
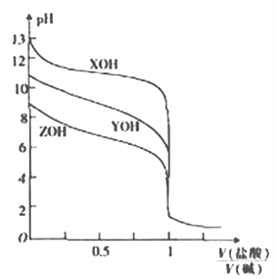
下列说法正确的是
A. 滴定XOH时可用酚酞作指示剂
B. YOH是强碱
C. X++H2OXOH+ H+的平衡常数K=10-4
D. [V(盐酸)/V(碱)]=0.5时,c(Z+)>c(Y+)>c(X+)
高三化学单选题中等难度题查看答案及解析
25 ℃时,用0.10 mol·L-1的盐酸分别滴定体积相同且浓度均为0.10 mol·L-1的三种一元碱XOH、YOH 及ZOH,滴定曲线如图所示。下列说法正确的是

A. YOH 是强碱
B. V(盐酸)/V(碱)=0.5 时,c(Z+)>c(Y+ )>c(X+)
C. X++H2OXOH+H+ 的平衡常数K=10-4
D. 滴定XOH 时可用酚酞作指示剂
高三化学单选题中等难度题查看答案及解析
25℃ 时,用0.10mol·L-1的盐酸分别滴定体积相同且浓度均为0.10mol·L-1的三种一元碱XOH、YOH及ZOH,滴定曲线如图所示。
下列说法正确的是( )
A. YOH是强碱 B. =0.5时,c(Z+)>c(Y+)>c(X+)
C. X++H2OXOH+H+的平衡常数K=10-4 D. 滴定XOH时可用酚酞作指示剂
高三化学单选题困难题查看答案及解析
25℃ 时,用0.10mol·L-1的盐酸分别滴定体积相同且浓度均为0.10mol·L-1的三种一元碱XOH、YOH及ZOH,滴定曲线如图所示。
下列说法正确的是( )
A. YOH是强碱 B. =0.5时,c(Z+)>c(Y+)>c(X+)
C. X++H2OXOH+H+的平衡常数K=10-4 D. 滴定XOH时可用酚酞作指示剂
高三化学单选题困难题查看答案及解析
常温下,XOH、YOH及ZOH三种一元碱的物质的量浓度均为0.100 mol·L-1,体积均为10.00 mL,分别用0.100 mol·L-1的HCl溶液滴定,滴定曲线如图所示。下列说法正确的是
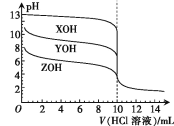
A.均可用酚酞作指示剂
B.电离平衡常数:Kb(YOH)<Kb(ZOH)
C.均滴入10.00 mL HCl溶液时,ZCl溶液中的水解程度最大
D.pH=11的YOH与pH=3的HCl溶液等体积混合:c(Cl-)>c(Y+)>c(H+)>c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下用0. 1000 mol/L的盐酸分别逐滴加入到20.00 mL 0.1000 mol/L的三种一元碱XOH、MOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示。下列叙述错误的是
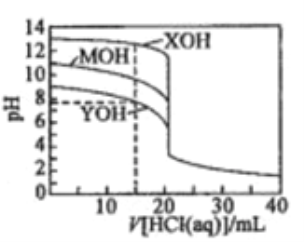
A. XOH为强碱,MOH、YOH均为弱碱
B. V[HCl(aq)]=15.00 mL时,三种溶液中离子总浓度大小顺序:XOH>MOH>YOH
C. V[ HCl(aq)]=20.00 mL时,三种溶液中水的电离程度:XOH> MOH> YOH
D. V[HCl(aq)]=40.00 ml.时,YOH溶液中:c(H+)=c(Y+)+c(OH-)+2c(YOH)
高三化学单选题中等难度题查看答案及解析
常温下用0. 1000 mol/L的盐酸分别逐滴加入到20.00 mL 0.1000 mol/L的三种一元碱XOH、MOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示。下列叙述错误的是
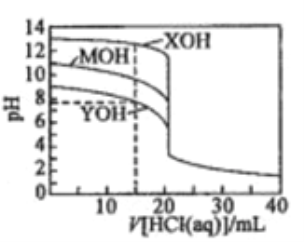
A. XOH为强碱,MOH、YOH均为弱碱
B. V[HCl(aq)]=15.00 mL时,三种溶液中离子总浓度大小顺序:XOH>MOH>YOH
C. V[ HCl(aq)]=20.00 mL时,三种溶液中水的电离程度:XOH> MOH> YOH
D. V[HCl(aq)]=40.00 ml.时,YOH溶液中:c(H+)=c(Y+)+c(OH-)+2c(YOH)
高三化学单选题中等难度题查看答案及解析
常温下用0.1000mol/L的盐酸分别逐滴加入到20.00mL0.1000 mo1/L的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示。 下列说法不正确的是
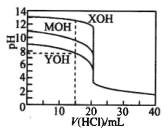
A. XOH为强碱,MOH、YOH均 为弱碱
B. V(HCl)=15.00mL时,三份溶液中离子总浓度大小顺序: XOH>MOH>YOH
C. 当盐酸滴加至20.00 mL时,三条曲线刚好相交
D. 在逐滴加入盐酸至40.00mL的过程中,三份溶液中水的电离程度均先增大后减小
高三化学单选题困难题查看答案及解析
高三化学填空题中等难度题查看答案及解析
常温下,用0.10mol·L-1盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COONa溶液和NaCN溶液,所得滴定曲线如图(忽略体积变化)。下列说法正确的是( )
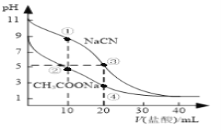
A.溶液中阳离子的物质的量浓度之和:点②等于点③
B.点①所示溶液中:c(CN-)+c(HCN)﹤2c(Cl-)
C.点②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)>c(CH3COOH)
D.点④所示溶液中:c(Na+)+c(CH3COOH)+c(H+)>0.10mol·L-1
高三化学单选题中等难度题查看答案及解析