C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池的电池反应式为:NaMO2+nC⇌Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
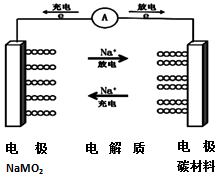
A.电池放电时,溶液中钠离子向负极移动
B.该电池负极的电极反应为:NaMO2-xe-═Na(1-x)MO2+xNa+
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.电池充电时的阳极反应式为:nC+x Na+-xe-═NaxCn
高三化学选择题困难题
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池的电池反应式为:NaMO2+nC⇌Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )

A.电池放电时,溶液中钠离子向负极移动
B.该电池负极的电极反应为:NaMO2-xe-═Na(1-x)MO2+xNa+
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.电池充电时的阳极反应式为:nC+x Na+-xe-═NaxCn
高三化学选择题困难题
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池的电池反应式为:NaMO2 + nCNa(1-x)MO2 + NaxCn ,下列有关该电池的说法正确的是

A. 电池放电时,溶液中钠离子向负极移动
B. 该电池负极的电极反应为NaMO2-xe- Na(1-x)MO2+xNa+
C. 消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D. 电池充电时的阳极反应式为:nC+xNa+-xe- NaxCn
高三化学选择题简单题查看答案及解析
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍,该电池的电池反应式为:NaMO2+nCNa(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )
A. 电池放电时,溶液中钠离子向负极移动
B. 电池充电时的阳极反应式为:nC+Na+-xe-=NaxCn
C. 消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D. 该电池负极的电极反应为:NaMO2-xe-=Na(1-x)MO2+xNa+
高三化学选择题困难题查看答案及解析
C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池的电池反应式为:NaMO2+nC⇌Na(1-x)MO2+NaxCn,下列有关该电池的说法正确的是( )

A.电池放电时,溶液中钠离子向负极移动
B.该电池负极的电极反应为:NaMO2-xe-═Na(1-x)MO2+xNa+
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.电池充电时的阳极反应式为:nC+x Na+-xe-═NaxCn
高三化学选择题困难题查看答案及解析
如图所示的C-NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该电池反应式为:NaMO2+nCNa(1-x)MO2+NaxCn,下列正确的是

A. 充电时,左侧电极为阳极
B. 电解质可以选用无水乙醇
C. 放电时,负极电极反应时为:NaMO2-xe-=Na(1-x)MO2+xNa+
D. 充电时,阳极电极反应式为:nC+xNa-xe-=NaxCn
高三化学单选题困难题查看答案及解析
C﹣NaMO2电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍.该电池的电池反应式为:NaMO2+nC⇌Na(1﹣x)MO2+NaxCn,下列有关该电池的说法正确的是

A.电池放电时,溶液中钠离子向负极移动
B.该电池负极的电极反应为:NaMO2﹣xe﹣═Na(1﹣x)MO2+xNa+
C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用钠时少
D.电池充电时的阳极反应式为:nC+x Na+﹣xe﹣═NaxCn
高三化学选择题困难题查看答案及解析
科学家们已研发出硅负极锂离子电池,在相同体积中,硅负极电池容量比石墨碳电池容量提升25%,反应原理为5LiMn2O4+Si 5Li0.12Mn2O4+Li4.4Si,LiPF6纯液体作电解质,下列有关说法正确的是( )
5Li0.12Mn2O4+Li4.4Si,LiPF6纯液体作电解质,下列有关说法正确的是( )
A.放电时的负极反应为Li﹣e﹣=Li+
B.若用该电池电解水,阴极生成3.52gO2,则该电池负极质量减少0.77g
C.锂离子电池充电时的阴极反应为Si+4.4e-+4.4Li+=Li4.4Si
D.放电时电解质LiPF6水溶液中的Li+移向正极
高三化学多选题中等难度题查看答案及解析
全钒液流电池充电时间短,续航能力强,被誉为“完美电池”。工作原理如图,已知反应的离子方程式:VO2++V3++H2OVO2++V2++2H+。下列叙述错误的是
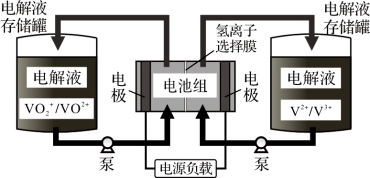
A.放电时,正极电极反应为:VO2++e-+2H+=VO2++H2O
B.充电时,阴极电极反应为:V3++e-=V2+
C.放电时,H+从电池右边移向左边
D.利用该电池电解饱和NaCl溶液(石墨作电极),2 mol VO2+发生氧化反应时,可生成气体44.8 L
高三化学选择题简单题查看答案及解析
我国是全钒液流电池最大生产国,产品出口美、欧、日等发达国家,市 场占有率全球第一。全钒液流电池充电时间短,续航能力强,被誉为“完美电池”,工作原理如图1所示,反应的离子方程式为:VO2++V3++H2O VO2++V2++2H+。以此电池电解Na2SO3溶液(电极材料为石墨),可再生NaOH,同时得到H2SO4,其原理如图2所示。下列说法正确的是
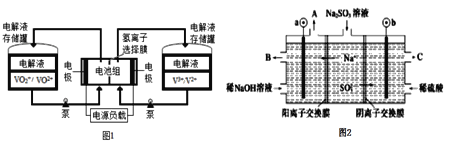
A.电解Na2SO3溶液时,a极与电池负极相连,图1中H+从电池右边移向左边
B.电解时b的电极反应式为SO32-+H2O-2e-=SO42-+2H+
C.电池放电时,负极电解液的pH升高
D.若电解过程中图2所有液体进出口密闭,则消耗12.6gNa2SO3阴极区变化的质量为4.5g
高三化学单选题中等难度题查看答案及解析
全钒液流电池充电时间短,续航能力强,被誉为“完美电池”,工作原理如图1所示,反应的离子方程式为:VO2++V3++H2O VO2++V2+ +2H+。以此电池电解Na2SO3溶液(电极材料为石墨),可再生NaOH,同时得到H2SO4,其原理如图2所示。下列说法错误的是
VO2++V2+ +2H+。以此电池电解Na2SO3溶液(电极材料为石墨),可再生NaOH,同时得到H2SO4,其原理如图2所示。下列说法错误的是
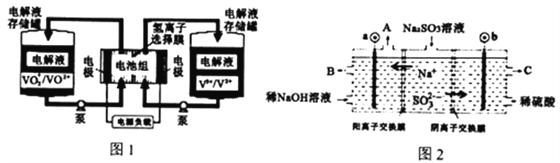
A. 电解Na2SO3溶液时,a极与电池负极相连,图1中H+从电池右边移向左边
B. 电池充电时,正极电极反应为VO2++e-+2H+=VO2++H2O
C. 电解时b的电极反应式为SO32-+H2O-2e- =SO42-+2H+
D. 若电解过程中图2 所有液体进出口密闭,则消耗12.6g Na2SO3,阴极区变化的质量为4.4g
高三化学单选题中等难度题查看答案及解析
全钒液流电池充电时间短,续航能力强,被誉为“完美电池”,工作原理如图1所示,反应的离子方程式为:VO2++V3++H2OVO2++V2++2H+。以此电池电解Na2SO3溶液(电极材料为石墨),可再生NaOH,同时得到H2SO4,其原理如图2所示。下列说法正确的是
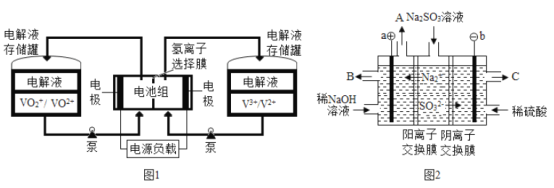
A. 电解Na2SO3溶液时,a极与电池负极相连,图1中H+从电池右边移向左边
B. 电解时b的电极反应式为SO32-+H2O-2e-=SO42-+2H+
C. 电池放电时,负极的电极反应式为VO2++e-+2H+=VO2++H2O
D. 若电解过程中图2所有液体进出口密闭,则消耗12.6gNa2SO3阴极区变化的质量为4.6g
高三化学单选题中等难度题查看答案及解析