-
醋酸是一种常见的弱酸,回答下列问题:
(1)醋酸的电离方程式是 ;
在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:
(2)向醋酸中加入醋酸钠固体,电离平衡 移动(填向左、向右或不变,下同);c(H+) (填增大、减小或不变,下同),pH (填增大、减小或不变,下同)
(3)向醋酸中加入碳酸钙固体,电离平衡向 移动;c(CH3COOH) .
(4)向醋酸中加入大量的水,c(OH﹣) .导电能力 ,电离平衡常数 .
高二化学填空题简单题查看答案及解析
-
醋酸是一种常见的弱酸,回答下列问题:
在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:
(1)向醋酸中加入醋酸钠固体,电离平衡向___________移动(填“正向”、“逆向”或“不移动”,下同);pH __________(填“增大”、“减小”或“不变”,下同)
(2)向醋酸中加入碳酸钙固体,电离平衡向________移动;c(CH3COOH)_________.
(3)向醋酸中加入大量的水,c(OH﹣)_________.导电能力__________.
高二化学填空题简单题查看答案及解析
-
醋酸是一种常见的弱酸,在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:(填“正向”、“逆向”或“不移动”, “增大”、“减小”或“不变”, 填“>”、“<”或“=”)
(1)向醋酸中加入醋酸钠固体,电离平衡向___________移动;pH __________
(2)向醋酸中加入碳酸钙固体,电离平衡向________移动;c(CH3COOH)_________.
(3)向醋酸中加入大量的水,c(OH-)_________.导电能力__________.
(4)体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①_____②;与完全相同的镁条发生反应,开始时的反应速率:①______ ②;中和等量NaOH时消耗的体积:①______②;与足量的Zn反应生成H2的物质的量:①_______②。
高二化学填空题中等难度题查看答案及解析
-
CH3COOH的电离方程式为CH3COOH
CH3COO-+H+。在0.1 mol·L-1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:
(1)向醋酸中加入醋酸钠固体,电离平衡 移动(填“向左”“向右”或“不”,下同);c(H+) (填“增大”“减小”或“不变”,下同),pH 。
(2)向醋酸中加入碳酸钙固体,电离平衡向 移动;c(CH3COOH) 。
(3)向醋酸中加入大量的水,c(OH-) 。导电能力 ,电离平衡常数 。
高二化学填空题中等难度题查看答案及解析
-
醋酸是一种常见的弱酸,请回答:
(1)已知某温度时,醋酸的电离平衡常数Ka=1.6×10-5。
①醋酸的起始浓度为0.010mol/L,平衡时c(H+)=______(提示:醋酸的电离平衡常数很小,平衡时的c(CH3COOH)可近似视为仍等于0.010mol/L
②pH=1的醋酸与pH=l的盐酸等体积混合,混合后溶液中c(CH3COO-)=_______。
(2)日常生活中常用醋酸除水垢,但工业锅炉的水垢中常含有CaSO4,需先用________(填化学式)溶液处理,而后用盐酸去除。
高二化学填空题中等难度题查看答案及解析
-
I.下表是室温下,几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb):

请回答下面问题:
(1)用蒸馏水稀释0.1 mol/L的醋酸溶液,下列选项中一定变小的是_____
A.c(H+) B.c(H+)·c(OH-) C.

(2)CH3COONH4的水溶液呈_______ (选填 酸性”、“中性"或“碱性”)。
(3)浓度为0.10 mol/L柠檬酸氢二钠(Na2HC6H5O7)溶液显酸性,通过计算说明其原因______。
(4)工业中常用碳酸镍制备氧化镍。已知:Ksp(NiCO3)=1.4×10-7,当 Ni,2+恰好完全转化为NiCO3沉淀[即溶液中c(Ni2+)=1×10-5 mol·L-1]时,溶液中c(CO32-)=_____mol/L。
II.(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。
2CO2(g)+6H2(g)
CH3CH2OH (g)+3H2O(g) △H=a kJ/mol
在一定压强下,测得.上述反应的实验数据如下表。
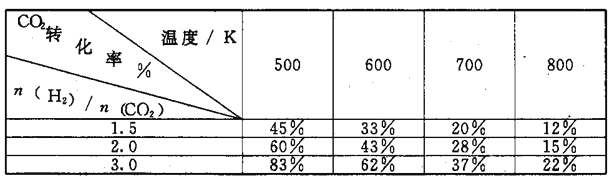
根据表中数据分析:
①上述反应的a_____0(填"大于”或“小于”)。
②在一定温度下.提高氢碳[即
 ]比,平衡常数K值_____(填“增大”、“减小”、或"不变”)。
]比,平衡常数K值_____(填“增大”、“减小”、或"不变”)。(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示;

根据上图,写出反应的热化学方程式为____________。
高二化学综合题中等难度题查看答案及解析
-
向0.1mol/LNaOH溶液中加入等体积的cmol/L醋酸溶液后恰好呈中性(忽略溶液混合时的体积变化)。回答下列问题:
(1)混合溶液中离子浓度大小顺序为:___;
(2)计算CH3COOH的电离常数Ka=___(用含c的代数式表示)。
高二化学计算题简单题查看答案及解析
-
弱电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
醋酸在水溶液中的电离方程式为 ______________________。
(2)用 0.1 mol·L-1 NaOH 溶液分别滴定体积均为 20.00 mL、浓度均为 0.1 mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
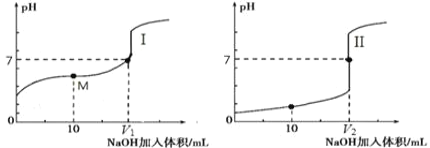
①滴定醋酸的曲线是_______________(填“I”或“II”)。
②室温时,若 0.1 mol·L-1 的醋酸的电离度为 1%,计算这醋酸溶液的 pH 值________。
③滴定开始前,三种溶液中由水电离出的 c(H+)最大的是________________________。
④上述用 0.1 mol·L-1 的 NaOH 溶液滴定 0.1 mol·L-1 的盐酸,下列操作不正确的是____________________________。
A.用标准 NaOH 溶液润洗碱式滴定管后,再装入标准碱溶液
B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
⑤上述滴定绝不能用___________作指示剂,若使用酚酞作指示剂则滴定终点的现象是_______________。
高二化学综合题简单题查看答案及解析
-
(8分)20℃时,醋酸的电离平衡常数为1.6×10-5。
(1)试计算20℃时0.01mol•L-1的醋酸溶液中氢离子浓度。
(2)室温时,向0.2mol•L-1的醋酸溶液中加入等体积的0.1mol•L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________,
②所得溶液中的物料守恒式为:________+________=__________=_________mol•L-1。
③c(CH3COOH)=_____________mol•L-1(写出算式,不做近似计算)
高二化学填空题简单题查看答案及解析
-
下列说法正确的是
A.0.1mol/L醋酸溶液加水稀释,电离平衡正移,电离平衡常数增大
B.0.1mol/L醋酸溶液中加入锌粒,电离平衡正移,c(H+)增大
C.0.1mol/L醋酸钠溶液中加入醋酸钠固体,水解平衡正移,c(OH-)增大
D.在AgCl饱和溶液中加入AgCl固体,沉淀溶解平衡正移,c(Ag+)增大
高二化学选择题中等难度题查看答案及解析