-
该同学用如下装置进行实验,分析影响反应速率的因素。实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示。
| 实验Ⅰ(断开K)1分钟水滴数 | 34 | 59 | 86 | 117 | … | 102 |
| 实验Ⅱ(闭合K)1分钟水滴数 | 58 | 81 | 112 | 139 | … | 78 |

下列说法不正确的是
A.实验Ⅰ中化学能主要转化为热能
B.实验Ⅱ中化学能主要转化为电能
C.反应前期水滴数58>34、81>59,主要原因是实验Ⅱ中形成原电池加快反应速率
D.反应后期水滴数102>78,主要原因是实验Ⅰ溶液温度高于实验Ⅱ
-
该同学用如下装置进行实验,分析影响反应速率的因素:

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示。下列说法不正确的是
| 实验Ⅰ(断开K)1分钟水滴数 | 34 | 59 | 86 | 117 | … | 102 |
| 实验Ⅱ(闭合K))1分钟水滴数 | 58 | 81 | 112 | 139 | … | 78 |
A.实验Ⅰ中化学能主要转化为热能
B.实验Ⅱ中化学能主要转化为电能
C.反应前期水滴数58>34、81>59,主要原因是实验Ⅱ中形成原电池加快反应速率
D.反应后期水滴数102>78,主要原因是实验Ⅰ溶液温度高于实验Ⅱ
-
某同学设计了如下图所示装置(部分夹持装置已略去)进行实验研究。

请回答:
(1)用上述装置探究影响化学反应速率的因素。
①圆底烧瓶中发生反应的离子方程式是________。
②用上述装置进行实验,以生成9.0 mL气体为计时终点,结果为 。
。
| 序号 | V(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
比较实验I和Ⅱ可以得出的实验结论是________。
实验过程中,对量气管的操作是。
③若将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是(填序号)________。
A.石墨 b.银 c.铜d.沙粒(二氧化硅)
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用(填序号)________。
a.NaOH溶液 b.C2H5OH c.NaCl溶液 d.稀硫酸
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是________。
-
(15分) 某同学设计了如下图所示装置(部分夹持装置已略去),该装置可以用来进行多项
实验研究。

请回答:
(1)用上述装置探究影响化学反应速率的因素。
①圆底烧瓶中发生反应的离子方程式是________。
②用上述装置进行实验,以生成9.0 mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
比较实验Ⅰ和Ⅱ可以得出的实验结论是________。
③若将锌片换成含杂质的粗锌片,且控制其他条件使其与上述实验完全一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是(填序号)________。
a.石墨 b.银 c.铜 d.沙粒(二氧化硅)
(2)用上述装置测定粗锌片的纯度。
①连接好装置,检查装置气密性,称量粗锌片mg置于圆底烧瓶中,滴加足量稀硫酸,充分反应直至不再产生气体为止,测得气体体积为VL,则粗锌片的纯度为________。
②本实验在读数前对量气管的操作是________。
③本套装置中若考虑滴入的稀硫酸的体积(假设其它操作都正确),则测得的气体的体积将________。(填“偏大”、“偏小”或“无影响”,)
(3)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用(填序号)________。
a.NH4Cl溶液 b.C2H5OH c.Na2CO3溶液 d.稀硫酸
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是________。
-
甲、乙两个实验小组分别利用KMnO4酸性溶液与H2C2O4溶液反应进行研究外界因素对反应速率的影响。设计实验方案如下:
甲组:通过测定生成CO2气体体积的方法来比较化学反应速率的大小。
实验装置如图,实验时分液漏斗中A溶液一次性放入B溶液中
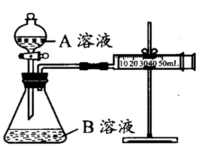
(注:实验中所用KMnO4溶液均已加人相同量H2SO4):
| 序号 | A溶液 | B溶液 |
| ① | 2 mL 0.1mol/LH2C2O4溶液 | 4 mL0.01mol/LKMnO4溶液 |
| ② | 2 mL 0.2mol/LH2C2O4溶液 | 4 mL0.01mol/LKMnO4溶液 |
(1)如何检查该装置的气密性:________。
(2)写出当锥形瓶中加入A溶液后发生的反应的离子方程式(提示:H2C2O4为弱酸):________。
(3)该实验探究的是________对化学反应速率的影响。分析所给实验仪器,实现该实验目的还欠缺的仪器:________。你将如何比较①②组化学反应速率大小?你的操作是________。
乙组:通过测定单位时间内KMnO4溶液浓度变化来判定反应速率快慢。
25℃时,40 mL 0.001mol/LKMnO4与38 mL0.1 mol/LH2C2O4和2 mL2.38mol/LH2SO4混合液共80 mL中KMnO4的浓度及对应时段的平均反应速率数据:
| 时间(min) | 4 | 8 | 12 | 16 | 21 | 22 | 23 | 24 | 25 |
| c(KMnO4)(10-4mol/L) | 4.58 | 4.02 | 3.36 | 2.25 | 0.72 | 0.43 | 0.23 | 0.16 | 0.13 |
| υ(KMnO4) (10-4mol/(L·min) | υ | 0.14 | 0.17 | 0.28 | 0.32 | 0.29 | 0.20 | 0.07 | 0.03 |
(4)完成上表中υ=________×10-4mol/(L·min)。
问题讨论:已知该实验过程中溶液温度几乎不变,但是依据实验数据发现开始阶段速率却在增大。
①你认为引起该反应速率增大的因素是________。
②请设计实验证明你的观点,写出实验步骤及结论:
-
(12分)为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验。
实验一 探究铜和稀硝酸反应的产物。
实验装置如图,气密性已检查。
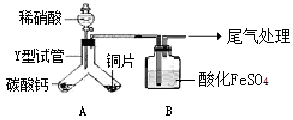
已知:FeSO4+NO=[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
(1)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 。
(2)铜片和稀硝酸反应的化学方程式为 。
(3)本实验A生成的气体中,若有NO2,B的实验现象为 ;若只有NO生成,B的实验现象是 。
实验二 探究铜和稀硝酸反应速率先慢后快的原因
经过实验一,测得硝酸的浓度<6 mol•L-1,只有NO生成。当铜片与5 mol•L-1硝酸反应时,开始时反应非常缓慢,一段时间后反应速率明显加快。为探究此反应的反应速率先慢后快的原因,进行如下探究:
探究一:研究反应过程的温度变化对反应速率的影响,实验所得曲线和现象记录如下图表。
| 时间/min | 现象 |
| 0~15 | 铜表面出现气泡,但速度很慢 |
| 25 | 溶液有很浅的蓝色,气泡生成速度加快 |
| 30 | 气泡生成速度较快,均匀冒出 |
| 45 | 洗气瓶中可见少量淡棕色的物质 |
| 50 | 溶液中蓝色明显变深,洗气瓶中突显明显棕色 |
(4)获得图2数据所需的测量仪器有________________________________。
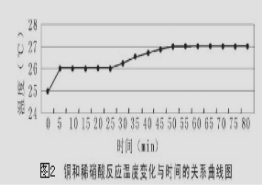
(5)从上述图表分析可得到的结论是 。
| 序号 | 温度 | 铜片/g | 硝酸/mL | 硝酸铜/g |
| 1 | 25℃ | ① | ② | ③ |
| 2 | 25℃ | 5 | 20 | 0.5 |
| 3 | 25℃ | 5 | 20 | 1.0 |
探究二:研究化学反应产物对反应速率的影响
设计了如下实验,利用上图装置测定溶液突显明显棕色的时间。
(6)请将上表中将实验1的实验条件填写完整① ② ③
(7)通过实验发现实验1、2、3的反应速率并无明显变化,为达到实验目的还需要继续进行的实验是 。
-
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5 mol • L-1 H2SO4溶液、2 mol • L-1 H2SO4溶液。甲同学研究的实验报告如下表∶
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol • L-1 的硫酸溶液于三支试管中 ②______________________ | 反应速率∶ 镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
(1) 甲同学表中实验步骤②为______________________。
(2) 甲同学的实验目的是__________________________。
要得出正确的实验结论,还需要控制的实验条件是_____________。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶

(3)乙同学在实验中应该测定的数据是_________________。
(4)乙同学完成该实验应选用的实验药品是________________。
-
某同学为研究电化学原理,使用KCl盐桥设计如图所示实验装置.下列分析不合理的是
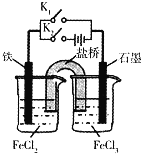
A.闭合 断开
断开 ,左侧烧杯中的
,左侧烧杯中的 向铁电极移动
向铁电极移动
B.无论闭合 ,断开
,断开 ,还是断开
,还是断开 ,闭合
,闭合 ,石墨电极上发生的反应都是
,石墨电极上发生的反应都是
C.闭合 ,断开
,断开 ,电流从石墨电极经过
,电流从石墨电极经过 流向铁电极
流向铁电极
D.闭合 ,断开
,断开 ,左侧烧杯中的溶液pH将逐渐降低
,左侧烧杯中的溶液pH将逐渐降低
-
某同学为研究电化学原理,使用KC1盐桥设计如图所示实验装置。下列分析不合理的是
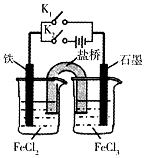
A.闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动
B.无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是
C.闭合K,断开K2,电流从石墨电极经过K.流向铁电极
D.闭合K,断开K2,左侧烧杯中的溶液pH将逐渐降低
-
如图所示,a、b是多孔石墨电极。某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转。下列说法不正确的是( )
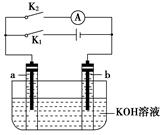
A.断开K2,闭合K1一段时间,溶液的pH变大
B.断开K1,闭合K2时,b极上的电极反应为2H++2e-=H2↑
C.断开K2,闭合K1时,a极上的电极反应为4OH--4e-=O2↑+2H2O
D.断开K1,闭合K2时,OH-向b极移动










