-
利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品“三盐”(3PbO·PbSO4·H2O),主要制备流程如下:
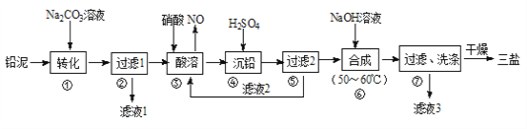
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为 ____________________________。
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为____________(写化学式)。
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为____________________________;滤液2中溶质主要成分为________(写化学式)。
(4)步骤⑥合成三盐的化学方程式为 _______________________________________。
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤干净的方法是 ___________________________________________________________________________。
-
四氧化三铅(Pb3O4,也可写作2PbO·PbO2)俗名“铅丹”或“红丹”,可用作防锈剂。工业上以废旧铅酸电池的铅膏(主要成分是PbSO4和PbO2)为原料制备Pb3O4的流程如下:

(1)“还原”时的化学方程式为________。
(2)已知:Ksp[PbCO3]=1.5×10-13。若使溶液中Pb2+的浓度小于1×10-5 mol·L-1,此时溶液中的c(CO32-) > ________mol·L-1。
(3)为测定某样品四氧化三铅含量,称取样品0.1200g,加入足量的6 mol·L-1HNO3充分溶解,过滤,得到含Pb2+的滤液和PbO2固体。将固体PbO2连同滤纸一并置于另一只锥形瓶中,加入足量的醋酸和醋酸钠混合溶液,再加入过量KI,使PbO2充分氧化I-,以淀粉溶液作指示剂,用0.01000mol·L-1 Na2S2O3溶液滴定,终点时用去30.00 mL。已知:I2 + 2Na2S2O3 = Na2S4O6 + 2NaI。
①所加KI必须过量,原因是________。
②计算试样中Pb3O4的质量分数_____。(写出计算过程)
-
(1)在一定条件下PbO2与Cr3+反应:3PbO2+2Cr3++H2O=Cr2O72-+3Pb2++2H+,
①求氧化10mL 0.2mol/L Cr3+反应需加PbO2固体的质量?____________
②若反应后溶液体积不变,求反应后H+的物质的量浓度。_____________
(2)将57.6g Cu完全溶于适量浓硝酸中,生成气体为氮的氧化物(含NO、N2O4、NO2的混合物)共0.8mol,这些气体恰好能被500mL 2mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液。
①求生成NaNO3的物质的量。_____________
②求氮的氧化物中N2O4物质的量。____________
-
电动自行车由于灵活、快捷、方便,已成为上班族的主要代步工具,其电源常采用铅蓄电池。反应原理为:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)。根据此反应判断下列叙述错误的是( )
2PbSO4(s)+2H2O(l)。根据此反应判断下列叙述错误的是( )
A. 放电时负极反应为:Pb(s)+SO (aq)-2e-===PbSO4(s)
(aq)-2e-===PbSO4(s)
B. 充电时电能转化为化学能
C. 放电时,电解液的密度增大
D. 充电时,电解液的pH减小
-
汽车的启动电源常用铅蓄电池,充电和放电反应按下式进行:
PbO2+Pb+2H2SO4 2PbSO4+2H2O,
2PbSO4+2H2O,
由此可知,该电池放电时的负极是( )
A.Pb B.PbO2 C.H2SO4 D.PbSO4
-
硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工 产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
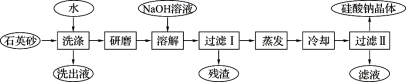
(1)要将洗出液中的溶质析出,采用的方法是 (填“蒸发”、“降温”)结晶;操作时用到的硅酸盐仪器有酒精灯(再填2个仪器) 。
(2)残渣的主要成分为: 。
(3)上述流程中加入NaOH溶液,反应的离子方程式为 。
-
硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
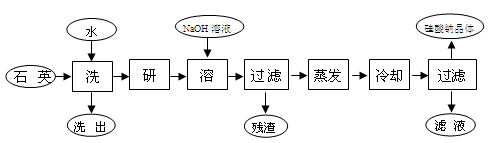
(1)要将洗出液中的溶质析出,采用的方法是 (填:“蒸发”、“降温”)结晶;蒸发时用到的硅酸盐仪器有 、 、 。
(2)上述流程中加入NaOH溶液,反应的离子方程式为 。
(3)用上述残渣中的氧化铁焊接铁轨,其铝热反应的化学方程式为(并在方程式中用“单线桥”标出电子转移方向和数目) 。
-
(9分)硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
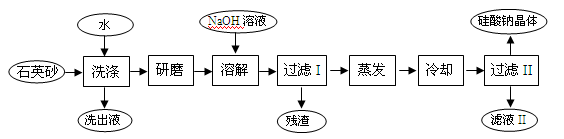
(1)要将洗出液中的溶质析出,采用的方法是 (填:“蒸发”、“降温”)结晶;蒸发时用到的硅酸盐仪器有 、 、 。
(2)上流程中加入NaOH溶液,反应的离子方程式为 。
(3)用上述残渣中的氧化铁焊接铁轨,其铝热反应的化学方程式为(并在方程式中用“单线桥”标出电子转移方向和数目) 。
-
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极:Pb + SO42- → PbSO4 + 2e 正极:PbO2 + 4H+ + SO42- + 2e → PbSO4 + 2H2O若为电解池提供0.1mol电子,这时电池内消耗的H2SO4的物质的量至少是( )
A、0.025mol B、0.050mol C、0.10mol D、0.20mol
-
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极Pb+SO42- ====PbSO4+2e-,正极PbO2+4H++SO42-+2e-===PbSO4+2H2O今若制得Cl2 0.050mol,这时电池内消耗的H2SO4的物质的量至少是( )
A. 0.025 mol B. 0.050 mol C. 0.10 mol D. 0.20 mol


 2PbSO4+2H2O,
2PbSO4+2H2O,

