-
下列说法中正确的是
A. 8NH3(g)+6NO2(g)==7N2(g)+12H2O(g) ΔH<0,则该反应一定能自发进行
B. 铁表面镀铜时,铜与电源的负极相连,铁与电源的正极相连
C. 由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀
D. 7.8g过氧化钠粉末与足量的水反应,转移电子数约为0.1×6.02×1023
高三化学多选题中等难度题查看答案及解析
-
下列说法中正确的是
A. 8NH3(g)+6NO2(g)=7N2(g)+12H2O(g);ΔH<0,则该反应一定能自发进行
B. 提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2效果好
C. 原电池放电过程中,负极质量一定减轻,正极的质量一定增加
D. 由于Ksp(MgCO3)<Ksp[Mg(OH)2],因此水垢中MgCO3会逐渐转化为Mg(OH)2
高三化学选择题中等难度题查看答案及解析
-
下列说法中正确的是
A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<0则该反应一定能自发进行
B.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
C.催化剂可以加快化学反应速率,也能增大化学反应的焓变
D.NH3•H2O溶液加水稀释后,溶液中c(NH3•H2O)/c(NH4+)的值增大
高三化学选择题中等难度题查看答案及解析
-
下列说法中正确的是
A.8NH3(g)+6NO2(g)
7N2(g)+12H2O(g) ΔH<0,则该反应一定能自发进行
B.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
C.催化剂可以加快化学反应速率,也能增大化学反应的焓变
D.NH3·H2O溶液加水稀释后,溶液中的值增大
高三化学选择题简单题查看答案及解析
-
下列说法中正确的是
A.8NH3(g)+6NO2(g)===7N2(g)+12H2O(g);ΔH<0,则该反应一定能自发进行
B.提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2效果好
C.原电池放电过程中,负极质量一定减轻,正极的质量一定增加
D.由于Ksp(MgCO3)<Ksp[Mg(OH)2],因此水垢中MgCO3会逐渐转化为Mg(OH)2
高三化学选择题中等难度题查看答案及解析
-
下列说法中正确的是( )
A.原电池放电过程中,负极质量一定减轻,正极质量一定增加
B.常温下浓硫酸与铝不反应,所以常温下可用铝制贮罐贮运浓硫酸
C.8NH3(g)+6NO2(g)=7N2(g)+12 H2O(g)△H<0该反应一定能自发进行
D.提取海带中的碘元素时,为将I﹣完全氧化为I2,用HNO3作氧化剂比用H2O2效果好
高三化学选择题中等难度题查看答案及解析
-
已知:8NH3(g) +6NO2(g)
7N2(g) +12H2O(1) △H<0。相同条件下,向2 L恒容密闭容器内充入一定量的NH3和NO2,分别选用不同的催化剂进行已知反应(不考虑NO2和N2O4之间的相互转化),反应生成N2的物质的量随时间的变化如图所示。下列说法错误的是( )
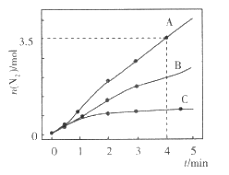
A.在催化剂A的作用下,0 ~4 min 内v(NH3)=1.0mol
L-1
min-1
B.若在恒容绝热的密闭容器中反应,当容器内温度不变时,说明反应已经达到平衡
C.不同催化剂作用下,该反应的活化能由大到小的顺序是Ea(C)> Ea(B)> Ea(A)
D.升高温度可使容器内气体颜色变浅
高三化学多选题中等难度题查看答案及解析
-
下列有关说法正确的是
A.向醋酸钠溶液中加水稀释时,溶液中所有离子浓度都减小
B.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
C.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<0,则该反应一定能自发进行
D.对N2(g)+3H2(g)
2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小
高三化学选择题中等难度题查看答案及解析
-
下列说法中不正确的是
A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<O,则该反应能自发进行
B.pH相等的四种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3 d.NaOH,则四种溶液中溶质的物质的量浓度由小到大顺序为:d<b<c<a
C.pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-)≤c(H+)
D.pH=9的CH3COONa溶液和pH=9的NH3·H2O溶液中水的电离程度相同
高三化学选择题中等难度题查看答案及解析
-
(10分)研究NO2、SO2 、等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为________。利用反应6NO2+ 8NH3
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是________L 。
(2)已知:2SO2(g)+O2(g)
2SO3(g) ΔH = - 196.6 kJ· mol-1
2NO(g)+O2(g)
2NO2(g) ΔH = - 113.0 kJ· mol-1
则反应NO2(g)+SO2(g)
SO3(g)+NO(g)的ΔH =kJ· mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=________。
高三化学填空题简单题查看答案及解析