-
甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整.向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
| 反应过程 | 化学方程式 | 焓变△H(kJ/mol) | 活化能Ea(kJ/mol) |
| 甲烷氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 |
| 蒸汽重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H=______kJ/mol.
(2)在初始阶段,甲烷蒸汽重整的反应速率______甲烷氧化的反应速率(填大于、小于或等于).
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g)⇌CO(g)+3H2(g)的KP=______;随着温度的升高,该平衡常数______(填“增大”、“减小”或“不变”).
(4)从能量角度分析,甲烷自热重整方法的先进之处在于______.
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如图1、图2:
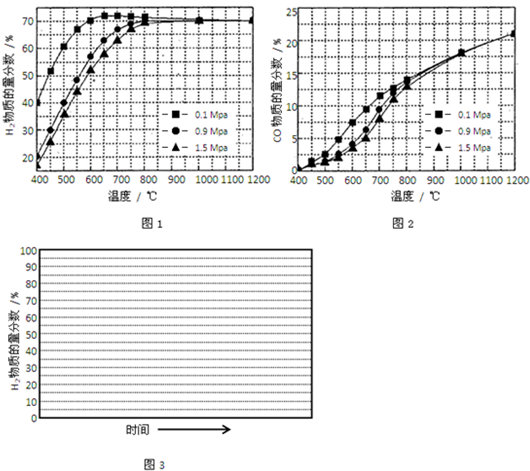
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是______.
A.600℃,0.9MpaB.700℃,0.9MPaC.800℃,1.5MpaD.1000℃,1.5MPa
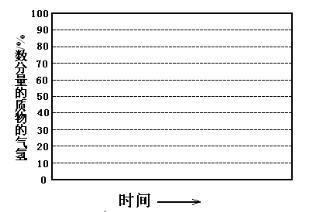
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图(如图3):
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是______.
-
甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
| 反应 过程 | 化学方程式 | 焓变△H (kJ/mol) | 正反应活化能Ea (kJ/mol) |
| 甲烷 氧化[ | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 |
| 蒸汽 重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H= kJ/mol。
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g) CO(g)+3H2(g)KP的表达式为 ;随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
CO(g)+3H2(g)KP的表达式为 ;随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量角度分析,甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
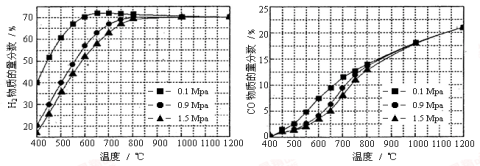
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
A.600℃,0.9Mpa B.700℃,0.9Mpa C.800℃,1.5Mpa D.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是 。
-
[15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
| 反应过程 | 化学方程式 | 焓变△H (kJ/mol) | 活化能Ea (kJ/mol) |
| 甲烷氧化 | CH4(g)+2O2(g) CO2(g)+2H2O(g) CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g) CO2(g)+2H2(g) CO2(g)+2H2(g) | -322.0 | 172.5 |
| 蒸汽重整 | CH4(g)+H2O(g) CO(g)+3H2(g) CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g) CO2(g)+4H2(g) CO2(g)+4H2(g) | 165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g) CO2(g)+H2(g)的△H= kJ/mol。
CO2(g)+H2(g)的△H= kJ/mol。
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以平衡常数(记作KP),则反应CH4(g)+H2O(g) CO(g)+3H2(g)的KP= ;
CO(g)+3H2(g)的KP= ;
随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量阶段分析,甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
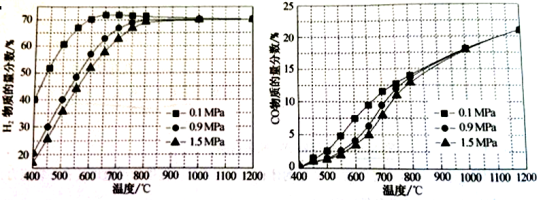
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
A.600℃,0.9Mpa B.700℃,0.9MPa C.800℃,1.5Mpa D.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始即时)
的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是 。
-
(13分)
甲烷自热重整是先进的制氢方法, 包含甲烷氧化和蒸气重整。向反应系统同时通入甲烷、氧气和水蒸气, 发生的主要化学反应有:
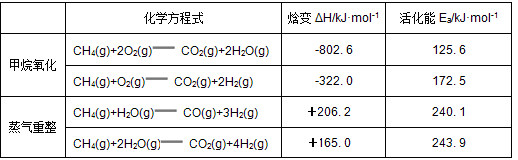
回答下列问题:
(1)反应CO(g)+H2O(g)  CO2(g)+H2(g)的ΔH= kJ·mol-1。
CO2(g)+H2(g)的ΔH= kJ·mol-1。
(2)在初始阶段, 甲烷蒸气重整的反应速率 甲烷氧化的反应速率(填“大于”、“小于”或“等于”)。
(3)对于气相反应, 用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp), 则反应CH4(g)+H2O(g) CO(g)+3H2(g)的Kp= 随着温度的升高, 该平衡常数 (填“增大”、“减小”或“不变”)。
CO(g)+3H2(g)的Kp= 随着温度的升高, 该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量角度分析, 甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下, 温度、压强对H2和CO物质的量分数的影响如下图:
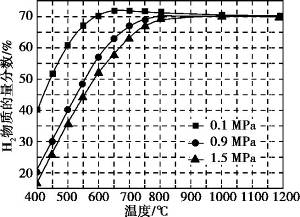
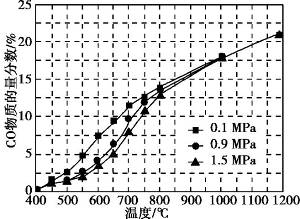
①若要达到H2物质的量分数>65%、CO物质的量分数<10%, 以下条件中最合适的是 。
A.600 ℃, 0.9 MPa B.700 ℃, 0.9 Mpa
C.800 ℃, 1.5 MPa D.1 000 ℃, 1.5 MPa
②画出600 ℃, 0.1 MPa条件下, 系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
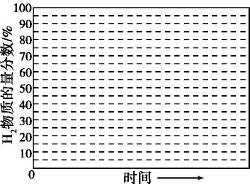
(6)如果进料中氧气量过大, 最终导致H2物质的量分数降低, 原因是 。
-
我国在南海北部神弧海域进行的可燃冰试采成功,这标志着我国成为全球第一个实现了在海域可燃冰试开采中获得连续稳定产气的国家。可燃冰主要成分是甲烷,可以用作燃料和制氢原料。甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸气重整两个过程。发生的主要反应如下:
| 化学方程式 | 焓变ΔH/(kJ·mol-1) | 活化能Ea/(kJ·mol-1) |
| 甲烷氧化 | CH4(g)+2O2(g) CO2(g)+2H2O(g) CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g) CO2(g)+2H2(g) CO2(g)+2H2(g) | -322.0 | 172.5 |
| 蒸气重整 | Ⅰ.CH4(g)+H2O(g) CO(g)+3H2(g) CO(g)+3H2(g) | +206.2 | 240.1 |
| Ⅱ.CH4(g)+2H2O(g) CO2(g)+4H2(g) CO2(g)+4H2(g) | +165 | 243.9 |
下列说法不正确的是
A.CO(g)+H2O(g) CO2(g)+H2(g) ΔH=+41.2kJ·mol-1
CO2(g)+H2(g) ΔH=+41.2kJ·mol-1
B.反应Ⅱ逆反应活化能Ea=78.9kJ·mol-1
C.初始阶段:甲烷氧化的速率大于甲烷蒸气重整的速率
D.甲烷自热重整方法的突出优点是能量循环利用
-
目前“低碳经济”正成为科学家研究的主要课题。请回答下列问题:
Ⅰ.甲烷自热重整是一种先进的制氢方法,其反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)阅读下图,计算上述反应的反应热ΔH=________kJ·mol-1。
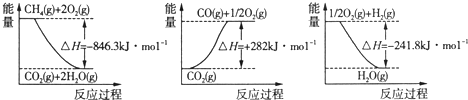
Ⅱ.用CH4或其他有机物、O2为原料可设计成燃料电池。
(2)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为________________________________________________________________________。
(3)以CH4、O2为原料,100mL0.15mol·L-1NaOH溶液为电解质设计成燃料电池,若放电时参与反应的氧气体积为448mL(标准状况),产生的气体全部被溶液吸收,则所得溶液中溶质的成分及物质的量之比为________________________,各离子浓度由大到小的顺序为________________________________________________________________________。
Ⅲ.利用I2O5消除CO污染的反应为5CO(g)+I2O5(s) 5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
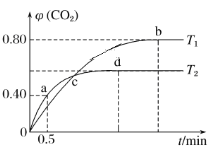
(4)T2时,0~0.5min内的反应速率v(CO)=________________。
(5)T1时化学平衡常数K=________。
(6)下列说法不正确的是________(填标号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
-
一定条件下,向容器中同时通入甲烷、氧气和水蒸气三种气体,发生的化学反应有:
| 反应过程 | 化学方程式 | 焓变 
| 活化能 
|
| 甲烷氧化 | 
| 
| 
|
| 
| 
| 
|
| 蒸汽重整 | 
| 
| 
|
| 
| 
| 
|
(1)已知: ,则
,则 燃烧热
燃烧热 _____。
_____。
(2)在初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率,原因可能是______。
(3)恒温恒压体系(温度为 ,压强为
,压强为 ),反应
),反应 达到平衡时,各气体的物质的量均为
达到平衡时,各气体的物质的量均为 ,用某气体组分
,用某气体组分 的平衡分压(分压=总压×物质的量分数)代替物质的量浓度
的平衡分压(分压=总压×物质的量分数)代替物质的量浓度 也可表示平衡常数(记作
也可表示平衡常数(记作 )。则:
)。则:
①平衡常数 ___。
___。
②再向容器中瞬时同时充入 、
、 、
、 、
、 ,此时
,此时 (正)____
(正)____ (逆)(填“>”“<”或“=”)
(逆)(填“>”“<”或“=”)
③恒温恒容条件下,将 、
、 、
、 、
、 按照体积比
按照体积比 投料,能判断反应
投料,能判断反应 达到平衡状态的是____。
达到平衡状态的是____。
A 密度保持不变 B  体积分数保持不变
体积分数保持不变
C 平均摩尔质量保持不变 D  和
和 的比保持不变
的比保持不变
E  断裂的同时,有
断裂的同时,有 断裂
断裂
(4)向绝热恒容密闭容器中通入 和
和 使反应
使反应 达到平衡,正反应速率随时间变化的示意图如图所示。图中
达到平衡,正反应速率随时间变化的示意图如图所示。图中 点反应是否达到平衡,说明理由_____。
点反应是否达到平衡,说明理由_____。

(5)利用重整反应 ,设计一种熔融碳酸盐燃料电池,原理示意图,电极
,设计一种熔融碳酸盐燃料电池,原理示意图,电极 上发生的电极反应为______。
上发生的电极反应为______。

-
(14分)目前“低碳经济”正成为科学家研究的主要课题。请回答 下列问题
I.甲烷自热重整是一种先进的制氢方法其反应方程式为:CH4(g) + H2O(g) =CO(g) + 3H2(g)
(1)阅读下图计算该反应的反应热ΔH = __________kJ/mol。

II.用CH4或其他有机物、O2为原料可设计成燃料电池。
(2)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池则负极的电极反应式为___________。
(3)以CH4、O2为原料,100 mL 0.15 mol/L NaOH溶液为电解质设计成燃料电池,若放电时参与反应的氧气体积为448 mL(标准状况),产生的气体全部被溶液吸收,则所得溶液中溶质的成分及物质的量之比为_____,各离子浓度由大到小的顺序为_______________。
III.利用I2O5消除CO污染的反应为:5CO(g) + I2O5(s) =5CO2(g) + I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数随时间t变化曲线如图。
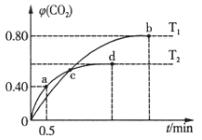
请回答:
(4)T2时,0 ~ 0.5 min内的反应速率v(CO) = ____________________。
(5)T1时化学平衡常数K = ____________________。
(6)下列说法不正确的是____________________填字母序号)。
A.容器内气体密度不变表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb < Kd
-
(14分)
目前“低碳经济”正成为科学家研究的主要课题。请回答下列问题:
I.甲烷自热重整是一种先进的制氢方法,其反应方程式为:
CH4(g) + H2O(g)  CO(g) + 3H2(g)
CO(g) + 3H2(g)
(1)阅读下图,计算该反应的反应热ΔH = __________kJ/mol。
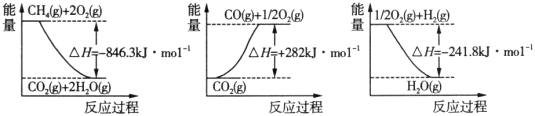
II.用CH4或其他有机物、O2为原料可设计成燃料电池。
(2)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为______________________________________________________________________。
(3)以CH4、O2为原料,100 mL 0.15 mol/L NaOH溶液为电解质设计成燃料电池,若放电时参与反应的氧气体积为448 mL(标准状况),产生的气体全部被溶液吸收,则所得溶液中溶质的成分及物质的量之比为____________________,各离子浓度由大到小的顺序为______________________________。
III.利用I2O5消除CO污染的反应为:5CO(g) + I2O5(s)  5CO2(g) + I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数随时间t变化曲线如图。请回答:
5CO2(g) + I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数随时间t变化曲线如图。请回答:
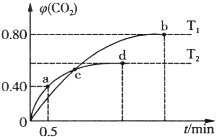
(4)T2时,0 ~ 0.5 min内的反应速率v(CO) = ____________________。
(5)T1时化学平衡常数K = ____________________。
(6)下列说法不正确的是___________(填字母序号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb < Kd
-
(15分)目前“低碳经济”正成为科学家研究的主要课题。请回答下列问题:
I.甲烷自热重整是一种先进的制氢方法,其反应方程式为:CH4(g) + H2O(g) CO(g) + 3H2(g)
CO(g) + 3H2(g)
(1)阅读下图,计算该反应的反应热ΔH = _______________kJ/mol。
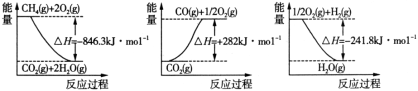
II.用CH4或其他有机物、O2为原料可设计成燃料电池。
(2)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为______________。
(3)以CH4、O2为原料,100 mL 0.15 mol/L NaOH溶液为电解质设计成燃料电池,若放电时参与反应的氧气体积为448 mL(标准状况),产生的气体全部被溶液吸收,则所得溶液中溶质的成分及物质的量之比为____________________,各离子浓度由大到小的顺序为________________________________________。
III.利用I2O5消除CO污染的反应为:5CO(g) + I2O5(s) 5CO2(g) + I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数随时间t变化曲线如图。请回答:
5CO2(g) + I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数随时间t变化曲线如图。请回答:
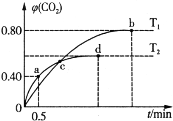
(4)T2时,0 ~ 0.5 min内的反应速率v(CO) = ____________________。
(5)T1时化学平衡常数K = _________________________。
(6)下列说法不正确的是____________________(填字母序号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb < Kd
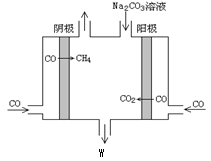
IV.(7)电解CO制备CH4和W,工作原理如图所示,其原理用电解总离子方程式解释是_____________。

CO2(g)+H2(g)的ΔH= kJ·mol-1。
CO(g)+3H2(g)的Kp= 随着温度的升高, 该平衡常数 (填“增大”、“减小”或“不变”)。


















