(10分)实验室常用二氧化锰和浓盐酸反应制备氯气,用下图装置可制备纯净、干燥的氯气,并验证其部分性质。
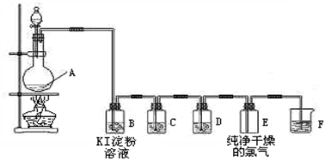
试回答下列问题:
(1)A中发生反应的化学方程式是 。
(2)C、D中所用试剂分别是:C ;D 。
(3)B中出现的现象是 。
(4)请用离子方程式表示F中NaOH溶液的作用 。
(5)若想制得标准状况下2.24L氯气,理论上被氧化的HCl的物质的量是 mol。
高一化学实验题困难题
(10分)实验室常用二氧化锰和浓盐酸反应制备氯气,用下图装置可制备纯净、干燥的氯气,并验证其部分性质。

试回答下列问题:
(1)A中发生反应的化学方程式是 。
(2)C、D中所用试剂分别是:C ;D 。
(3)B中出现的现象是 。
(4)请用离子方程式表示F中NaOH溶液的作用 。
(5)若想制得标准状况下2.24L氯气,理论上被氧化的HCl的物质的量是 mol。
高一化学实验题困难题
(10分)实验室常用二氧化锰和浓盐酸反应制备氯气,用下图装置可制备纯净、干燥的氯气,并验证其部分性质。

试回答下列问题:
(1)A中发生反应的化学方程式是 。
(2)C、D中所用试剂分别是:C ;D 。
(3)B中出现的现象是 。
(4)请用离子方程式表示F中NaOH溶液的作用 。
(5)若想制得标准状况下2.24L氯气,理论上被氧化的HCl的物质的量是 mol。
高一化学实验题困难题查看答案及解析
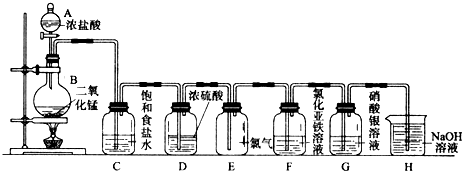
实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验,请回答下列问题:

(1)A中盛有浓盐酸,B中盛有MnO,则烧瓶中发生反应的化学方程式为:______。
(2)C中盛有饱和食盐水,其作用是_________,装置D的作用_________。
(3)装置E中气体的颜色为_______,E中Cl能使湿润的红色布条褪色的原因是________。
(4)F中是FeCl溶液,现象是________,发生反应的离子方程式为__________。
(5)G中是AgNO溶液,现象是___________,有关化学反应的离子方程式为_________。
(6)H中盛有NaOH溶液,其作用是_______,发生反应的化学方程式为_________。
高一化学实验题中等难度题查看答案及解析
实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验,请回答下列问题:
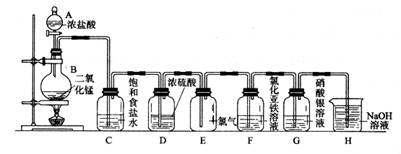
(1)A中盛有浓盐酸,B中盛有MnO,则烧瓶中发生反应的化学方程式为:
(2)C中盛有饱和食盐水,其作用是________,
D中浓硫酸的作用是________.
(3)E中盛有的Cl的颜色是________,Cl
能使湿润的红色布条褪色的原因是
(4)F中是FeCl溶液,现象是
发生反应的化学方程式为
(5)G中是AgNO溶液,现象是
有关化学反应的离子方程式为
(6)H中盛有NaOH溶液,其作用是
发生反应的化学方程式为
高一化学实验题简单题查看答案及解析
实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验。请回答下列问题:

(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的化学方程式为:
________
(2)C中盛有饱和食盐水,其作用是________,D中浓硫酸的作用是________。
(3)F中是FeCl2溶液,F中发生反应的离子方程式为________
(4)G中是AgNO溶液,现象是________
(5)H中盛有Na0H溶液,其作用是________。
高一化学实验题简单题查看答案及解析
实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验。请回答下列问题:
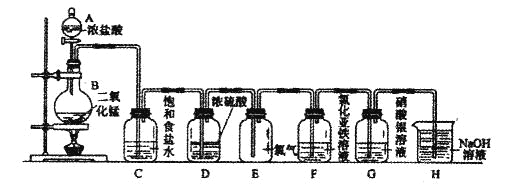
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的化学方程式为:
_________________________________________________________
(2)C中盛有饱和食盐水,其作用是________________________________,D中浓硫酸的作用是___________________________________。
(3)F中是FeCl2溶液,F中发生反应的离子方程式为___________________
(4)G中是AgNO溶液,现象是______________________________
(5)H中盛有Na0H溶液,其作用是_____________________________。
高一化学实验题中等难度题查看答案及解析
(10分)下图是实验室制取、提纯氯气及研究氯气性质的装置图。请回答:

(1)上图实验室制备氯气的化学反应方程式为 。
(2)通常用向上排空气法或者排饱和食盐水法收集氯气,若要利用C瓶收集到干燥纯净的氯气,B瓶所装的试剂是 。(填名称)
(3)若D瓶中装有硝酸银溶液,则观察到的现象是 。
(4)E装置用来 ,写出E装置中发生化学反应的离子方程式 。
高一化学实验题中等难度题查看答案及解析
(10分)下图是实验室制取、提纯氯气及研究氯气性质的装置图。请回答:
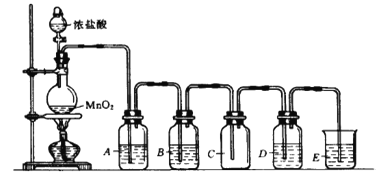
(1)上图实验室制备氯气的化学反应方程式为 。
(2)通常用向上排空气法或者排饱和食盐水法收集氯气,若要利用C瓶收集到干燥纯净的氯气,B瓶所装的试剂是 。(填名称)
(3)若D瓶中装有硝酸银溶液,则观察到的现象是 。
(4)E装置用来 ,写出E装置中发生化学反应的离子方程式 。
高一化学实验题中等难度题查看答案及解析
高一化学解答题中等难度题查看答案及解析
工业上将纯净干燥的氯气通入到0.5 mol·L-1 NaOH溶液中得到漂白水。某同学想在实验室探究Cl2性质并模拟制备漂白水,下图是部分实验装置。已知KMnO4与浓盐酸反应可以制取Cl2。(注:装置D中布条为红色)

(1)用装置A制备Cl2,该同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未顺利流下,你认为原因可能是:__________________。
(2)配平KMnO4与盐酸反应的化学方程式:
KMnO4+ HCl(浓) = KCl + MnCl2+ Cl2↑+ H2O ,该反应中氧化剂和还原剂的物质的量之比为________。
(3)饱和食盐水的作用是______________,浓硫酸的作用_____________,装置E的作用是_______________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_________________________。
(5)配制450 mL物质的量浓度为0.4 mol·L-1 NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ,需用托盘天平称量NaOH的质量是 。
高一化学实验题困难题查看答案及解析
(12分)工业上将纯净干燥的氯气通入到0.5 mol·L-1NaOH溶液中得到漂白水。某同学想在实验室探究Cl2性质并模拟制备漂白水,下图是部分实验装置。已知KMnO4与浓盐酸反应可以制取Cl2。(装置D中纸条为红色)
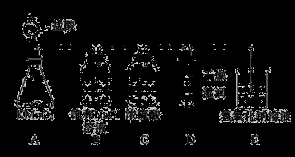
(1)配平KMnO4与盐酸反应的化学方程式:
KMnO4+ HCl(浓) = KCl + MnCl2+ Cl2↑+ H2O
(2)如果反应中转移0.5mol电子,则生成Cl2的物质的量为____________。
(3)浓硫酸的作用是 。
(4)实验时装置D中的现象是 。
(5)装置E中发生化学反应的离子方程式为 。
(6)配制480 mL物质的量浓度为0.5 mol·L-1NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ,需称量的NaOH的质量是 。
高一化学填空题中等难度题查看答案及解析