-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:
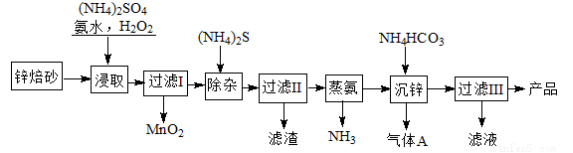
请回答下列问题:
(1) (NH4)2SO4与NH3·H2O组成的混合溶液工业上称为缓冲溶液,向该溶液中加入少量强酸或强碱,溶液的PH都不会有明显变化,请分别用离子方程式说明原因_________________________________。
(2)“浸取”时为了加快锌的浸出速率,可采取的措施有__________________________(任写两种);
(3)“浸取”时加入的NH3 • H2O过量,写出生成MnO2的离子方程式_______________________;
(4)适量S2-能将Cu2+转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?_______________;
用计算说明原因:______________________________;
[已知:Ksp(ZnS)=1.6×l0-24 ,Ksp(CuS)=1.3×l0-36
(5)“沉锌”的离子方程式是________________________________________;
(6)该过程中,蒸氨所得氨气可循环利用,“过滤III”所得滤液也可循环使用,其主要成分的化学式是___________________________。
-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:下列说法不正确的是()

A. 当(NH4)2SO4,NH3·H2O的混合溶液呈中性时,c(NH4+) = 2c(SO42-)
B. “浸取”时为了提高锌的浸出率,可采取的措施是搅拌、适当加热
C. “浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为Mn2++H2O2+2NH3·H2O=MnO2+2NH4++2H2O
D. “过滤Ⅲ”所得滤液可循环使用,其主要成分的化学式是NH4HCO3
-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:
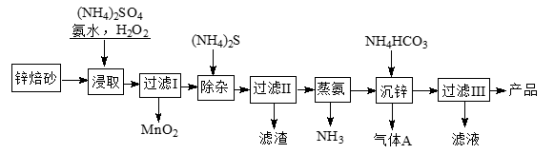
请回答下列问题:
(1)当(NH4)2SO4、NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42)时,溶液呈 (填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是 (任写两种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为 。
(4)适量S2能将Cu2+硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: 。
[已知:Ksp(ZnS)=1.6×1024,Ksp(CuS)=1.3×1036;一般认为反应的平衡常数K>105,该反应进行基本完全。]
(5)“沉锌”的离子方程式为___________________。
(6)上述流程中多次需要过滤,实验室进行过滤操作需要用到的玻璃仪器有__________。“过滤III”所得滤液可循环使用,产品需洗涤干燥后备用,检验产品洗涤干净的操作和现象是_______________。
-
2Zn(OH)2•ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2、Mn2+等离子)为原料制备2Zn(OH)2•ZnCO3的工艺流程如下:
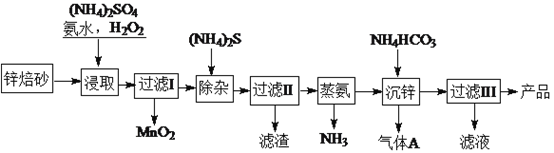
请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42)时,溶液呈______(填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是_____________(任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为____________________。
(4)“沉锌”的离子方程式为____________________________。
(5)“过滤III”所得滤液可循环使用,其主要成分的化学式是___________
(6)已知:HCN的电离常数Ka=4.9×10-10,H2S的电离常数Ka1=1.3×10―7, Ka2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为___________________________________。在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______。[已知:Ksp(MnS)=1.4×10―15]
-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:
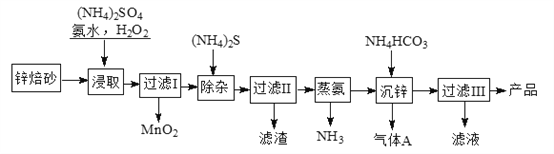
请回答下列问题:
(1)当(NH4)2SO4、NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42)时,溶液呈______________(填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是_____________(任写两种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为________________________。
(4)适量S2能将Cu2+转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因:________________________。
[已知:Ksp(ZnS)=1.6×1024,Ksp(CuS)=1.3×1036;一般认为反应的平衡常数K>105,该反应进行基本完全。]
(5)“沉锌”的离子方程式为___________________。
(6)上述流程中多次需要过滤,实验室进行过滤操作需要用到的玻璃仪器有__________。“过滤III”所得滤液可循环使用,产品需洗涤干燥后备用,检验产品洗涤干净的操作和现象是_______________。
-
2Zn(OH)2•ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2•ZnCO3的工艺流程如下:
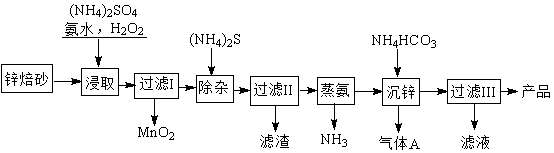
请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42 - )时,溶液呈 (填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是 (任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为 。
(4)适量S2-能将Cu2+等离子转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: 。
[已知:Ksp(ZnS)=1.6×10-24,Ksp(CuS)=1.3×10-36]
(5)“沉锌”的离子方程式为 。
(6)“过滤3”所得滤液可循环使用,其主要成分的化学式是 。
-
2Zn(OH)2•ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2、Mn2+等离子)为原料制备2Zn(OH)2•ZnCO3的工艺流程如下:
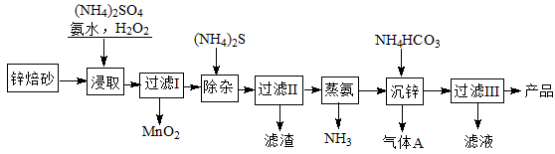
请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液呈中性时, c(NH4+) 2c(SO42-)(填“<”、“>”或“=”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是 (任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为 。
(4)适量S2能将Cu2+等离子转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: 。
[已知:Ksp(ZnS)=1.6×1024,Ksp(CuS)=1.3×1036+;K﹥105化学反应完全]
(5)“沉锌”的离子方程式为 。
(6)“过滤3”所得滤液可循环使用,其主要成分的化学式是 。
-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:
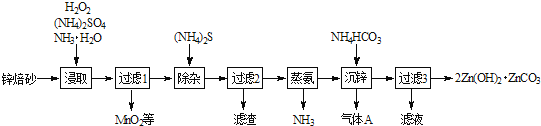
(1)用(NH4)2SO4与NH3·H2O的混合溶液浸取锌焙砂生成[Zn(NH3)4]2+的过程中加入H2O2的目的是________。
(2)加入(NH4)2S除杂过程中的主要离子方程式为________。
(3)过滤3所得滤液可循环使用,其主要成分的化学式是_______。
(4)检验2Zn(OH)2·ZnCO3沉淀是否洗涤干净的方法是________。
(5)写出沉锌步骤中发生反应的化学方程式________。
-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:
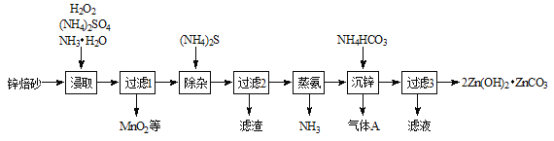
(1)用(NH4)2SO4与NH3·H2O物质的量之比为1∶2的混合溶液浸取锌焙砂时,生成[Zn(NH3)4]2+,该反应的离子方程式是 。浸取过程加入H2O2的目的是 。
(2)适量S2-能将Cu2+等离子转化为硫化物沉淀而除去,若选择置换的方法除杂,则应加入的物质为 。
(3)气体A的化学式是 。
(4)过滤3所得滤液可循环使用,其主要成分的化学式是 。证明2Zn(OH)2·ZnCO3沉淀洗涤完全的方法是 。
(5)为实现循环生产,下列物质中可以用来代替(NH4)2S完成除杂的是 。(填字母)
a.Na2S b.K2S c.BaS
-
2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:

(1)用(NH4)2SO4与NH3·H2O物质的量之比为1∶2 的混合溶液浸取锌焙砂时,生成[Zn(NH3)4]2+,该反应的离子方程式是 。浸取过程加入H2O2的目的是 。
(2)适量S2-能将Cu2+等离子转化为硫化物沉淀而除去,若选择置换的方法除杂,则应加入的物质为 。
(3)气体A的化学式是 。
(4)过滤3所得滤液可循环使用,其主要成分的化学式是 。证明2Zn(OH)2·ZnCO3沉淀洗涤完全的方法是 。
(5)为实现循环生产,下列物质中可以用来代替(NH4)2S完成除杂的是 。(填字母)
a.Na2S b.K2S c.BaS









