-
分短周期主族元素A、B、D、E的原子序数依次增大;A2为气态绿色燃料,常温下BA3分子是碱性气体,D是短周期元素中原子半径最大的,E的最高价氧化物对应的水化物酸性比硫酸强,请回答下列问题:
(1)D原子的原子结构示意图为 。
(2)B元素的气态氢化物与其最高价氧化物的水化物可化合为物质X,物质X中含有的化学键类型是 ,X的水溶液呈酸性,用离子方程式解释呈酸性的原因: ,检验物质X中阳离子的方法是 。
(3) BE3(该分子中B元素显负价)常用作漂白剂,工业上过量的BA3和E2反应制备,BE3分子的电子式为 ,工业上制备BE3的化学方程式为 。
(4)加热条件下,BE3和NaClO2溶液反应可制备二氧化氯气体,同时生成BA3和只含一种钠盐的强碱溶液,该反应的离子方程式为 ,若制备6.75Kg二氧化氯,则消耗还原剂的物质的量为 mol。
高三化学推断题困难题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期主族元素,其原子半径依X、Z、Y、W的顺序增大。已知Y的气态氢化物水溶液显碱性、Z是地壳中含量最高的元素,W的原子半径在同周期中最小(稀有气体除外)。下列说法正确的是( )
A.
的酸性强于
,所以W的非金属性比Y强
B.X、Y分别与Z按原子个数比2∶1形成的化合物都是弱电解质
C.由Y和Z元素形成的氧化物最多可有5种
D.由X、Y、Z元素组成的化合物均为共价化合物
高三化学单选题中等难度题查看答案及解析
-
己知X、Y、Z、Q、R是原子序数依次增大的短周期元素,X和Q位于同主族,Y、Z、R在元素周期表中的相对位置如图所示,其中Q与R属于同周期.且R的单质常温下是一种黄绿色气体,X2Z2分子和R-离子具有相同的电子数,请回答:
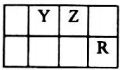
(1)Y元素位于周期表中的第__________族,
(2)化合物Q2Z2中含有的化学键类型有__________。
(3)用电子式表示化合物QR的形成过程:__________。
(4)Y2X4与AgNO3溶液反应可生成Ag、Y2和硝酸,写出该反应的化学方程式:__________。
高三化学填空题中等难度题查看答案及解析
-
W、X、Y、Z是原子序数依次增大的四种短周期非金属主族元素,q、r、s、h 是这些元素形成的物质,其中h 是离子化合物,q是制太阳能电池的主要原料,s常温下呈气态且其水溶液显碱性,r为二元化合物,其浓溶液在空气中易形成白雾。下列说法正确的是( )
A. Y 与X属于同一主族,与Z属于同一周期 B. 单质的沸点:X>Z
C. 常温常压下,W的氧化物为液态 D. X的氧化物均能用向上排空气法收集
高三化学单选题困难题查看答案及解析
-
W、X、Y、Z是原子序数依次增大的四种短周期非金属主族元素,q、r、s、h 是这些元素形成的物质,其中h 是离子化合物,q是制太阳能电池的主要原料,s常温下呈气态且其水溶液显碱性,r为二元化合物,其浓溶液在空气中易形成白雾。下列说法正确的是( )
A. Y 与X属于同一主族,与Z属于同一周期
B. 单质的沸点:X>Z
C. 常温常压下,W的氧化物为液态
D. X的氧化物均能用向上排空气法收集
高三化学单选题困难题查看答案及解析
-
W、X、Y、Z是原子序数依次增大的四种短周期非金属主族元素,q、r、s、h 是这些元素形成的物质,其中h 是离子化合物,q是制太阳能电池的主要原料,s常温下呈气态且其水溶液显碱性,r为二元化合物,其浓溶液在空气中易形成白雾。下列说法正确的是( )
A. Y 与X属于同一主族,与Z属于同一周期 B. 单质的沸点:X>Z
C. 常温常压下,W的氧化物为液态 D. X的氧化物均能用向上排空气法收集
高三化学单选题困难题查看答案及解析
-
W、X、Y、Z是原子序数依次增大的四种短周期非金属主族元素,q、r、s、h是这些元素形成的物质,其中h是离子化合物,q是制太阳能电池的主要原料,s常温下呈气态且其水溶液显碱性,r为二元化合物,其浓溶液在空气中易形成白雾。下列说法正确的是
A. 常温常压下,W的氧化物为液态
B. 单质的沸点:X>Z
C. X与Y属于同一主族,与Z属于同一周期
D. X的氧化物均能用向上排空气法收集
高三化学单选题中等难度题查看答案及解析
-
短周期主族元素M、T、X、Y、Z的原子序数依次增大,M的气态氢化物极易溶于T的简单氢化物中,且所得溶液显碱性;常温下,X的单质能溶于Y的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法错误的是( )
A.原子半径的大小顺序为Y>Z>X>M>T
B.元素M的气态氢化物与Z的气态氢化物相遇会产生白烟
C.元素Y、Z的最高价氧化物的水化物酸性比较,Z的更强
D.仅由M、T两种元素组成的化合物有多种
高三化学单选题中等难度题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置 如右表所示;X的单质在氧气中燃烧能生成两种无色气体, Y的最简单气态氢化物的水溶液显碱性。
回答下列问题:
(1)元素X在周期表中位于________族;W和Z的气态氢化物稳定性比较,其较强的是_______(填化学式)。
(2)W的单质与水反应生成的含氧酸的电子式为_____________。
(3)在BaCl2溶液中加入少量Y的最高价氧化物对应水化物溶液,再通入ZO2气体,能生成无色气体YO和白色沉淀___________(填化学式);ZO2和YO还原性比较,其较强的是___________(填化学式)。
高三化学推断题困难题查看答案及解析
-
W、X、Y、Z为原子序数依次增大的短周期主族元素,它们分别位于三个不同的周期。常温下,元素W与X可形成两种液态物质;Y、Z两种元素可组成二聚气态分子(如图所示),其中Y原子的最外层电子数等于其电子层数。下列叙述不正确的是( )
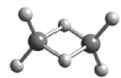
A.W与Z具有相同的负化合价
B.四种元素的简单离子半径由大到小的顺序:Z>Y>X>W
C.Y2Z6分子中所有原子的最外层均满足8电子稳定结构
D.工业上可电解X与Y形成的熔融化合物制取Y的单质
高三化学单选题中等难度题查看答案及解析